Marktübersicht
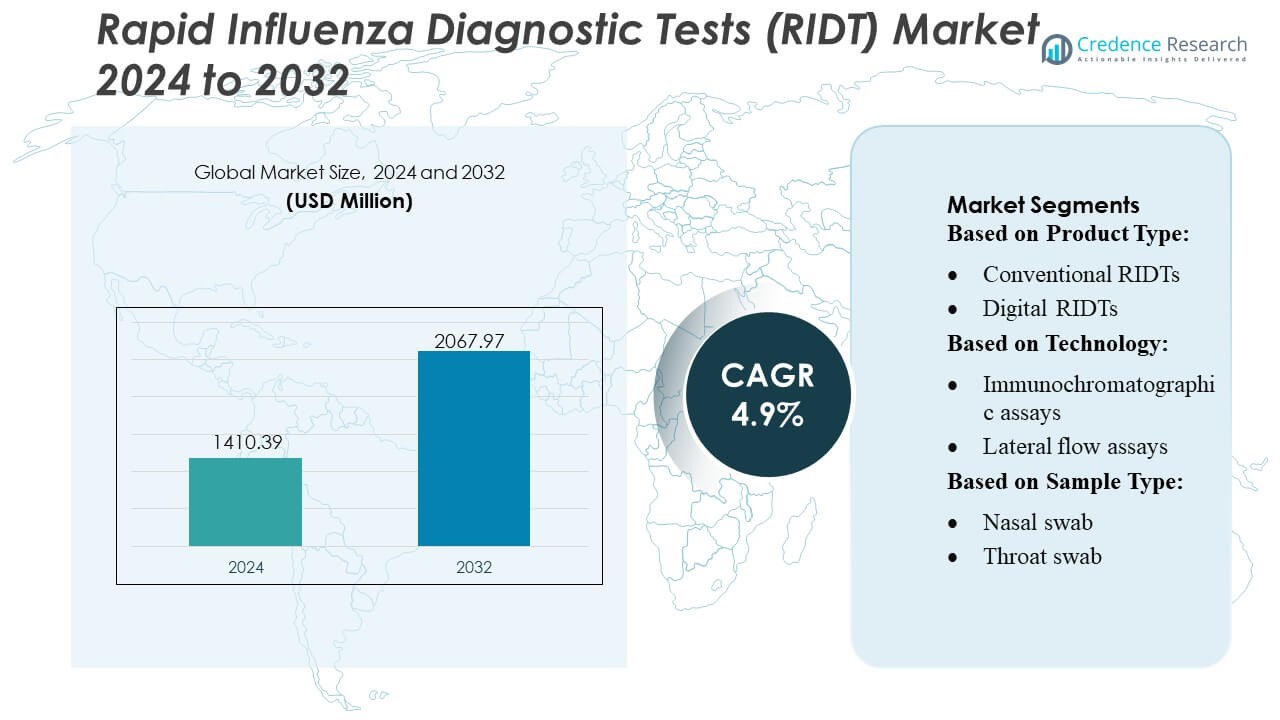
Der Markt für schnelle Influenza-Diagnosetests (RIDT) wurde im Jahr 2024 auf 1410,39 Millionen USD geschätzt und soll bis 2032 2067,97 Millionen USD erreichen, mit einer jährlichen Wachstumsrate (CAGR) von 4,9 % während des Prognosezeitraums.
| BERICHTSATTRIBUT |
DETAILS |
| Historischer Zeitraum |
2020-2023 |
| Basisjahr |
2024 |
| Prognosezeitraum |
2025-2032 |
| Marktgröße für schnelle Influenza-Diagnosetests (RIDT) 2024 |
USD 1410,39 Millionen |
| Markt für schnelle Influenza-Diagnosetests (RIDT), CAGR |
4,9% |
| Marktgröße für schnelle Influenza-Diagnosetests (RIDT) 2032 |
USD 2067,97 Millionen |
Der Markt für schnelle Influenza-Diagnosetests (RIDT) zeichnet sich durch starken Wettbewerb unter führenden Diagnostikherstellern aus, die sich auf Technologien zur schnellen Antigenerkennung, plattformbasierte digitale Leser und dezentrale Testlösungen konzentrieren. Diese Unternehmen stärken ihre Portfolios durch hochsensitive Tests, Multiplex-Respirationspanels und Point-of-Care-Kits, die für Krankenhäuser, Einzelhandelskliniken und Heimtests entwickelt wurden. Kontinuierliche Investitionen in Forschung und Entwicklung, behördliche Zulassungen und erweiterte Vertriebsnetze stärken ihre Marktpräsenz. Nordamerika führt den globalen RIDT-Markt mit einem genauen Anteil von 38 % an, unterstützt durch fortschrittliche Gesundheitsinfrastrukturen, hohe Testvolumina und starke Akzeptanz vernetzter Diagnosesysteme, die die Influenza-Überwachung und klinische Entscheidungsfindung verbessern.
Access crucial information at unmatched prices!
Request your sample report today & start making informed decisions powered by Credence Research Inc.!
Download Sample
Markteinblicke
- Der Markt wurde im Jahr 2024 auf 1410,39 Millionen USD geschätzt und soll bis 2032 2067,97 Millionen USD erreichen, mit einer jährlichen Wachstumsrate (CAGR) von 4,9 % während des Prognosezeitraums.
- Das Marktwachstum wird durch die steigende Influenza-Inzidenz, die starke Akzeptanz von Point-of-Care-Screenings und die steigende Nachfrage nach schnellen, hochgenauen Antigenerkennungskits in Krankenhäusern und Einzelhandelskliniken angetrieben.
- Zu den wichtigsten Trends gehören die Erweiterung digitaler Leser-basierter RIDTs, die Entwicklung von Multiplex-Respirationspanels und die breitere Verfügbarkeit von Heim- und OTC-Schnelltests für Influenza.
- Der Wettbewerb intensiviert sich, da Unternehmen die Empfindlichkeit der Tests verbessern, behördliche Zulassungen anstreben und Vertriebsnetze für dezentrale Testumgebungen erweitern.
- Nordamerika führt mit einem Anteil von 38 %, während digitale Schnelltests weltweit einen wachsenden Segmentanteil erobern; Asien-Pazifik folgt mit steigender Akzeptanz, unterstützt durch den Ausbau der Diagnostikinfrastruktur und den Bedarf an saisonalem Ausbruchsmanagement.
 Marktsegmentierungsanalyse:
Marktsegmentierungsanalyse:
Nach Produkttyp
Der Markt für schnelle Influenza-Diagnosetests (RIDT) wird von konventionellen RIDTs angeführt, die einen geschätzten Marktanteil von 58% einnehmen, da sie kostengünstig sind, breit klinisch angenommen werden und in der Lage sind, Ergebnisse innerhalb von 10–15 Minuten in Point-of-Care-Umgebungen zu liefern. Krankenhäuser und Notfallzentren bevorzugen diese Kits für hochvolumige saisonale Tests, was ihre anhaltende Dominanz unterstützt. Digitale RIDTs gewinnen an Bedeutung, da integrierte Leser die Ergebnisgenauigkeit verbessern und benutzerabhängige Interpretationsfehler reduzieren. Die Akzeptanz steigt in Kliniken, die mit Konnektivität ausgestattete Geräte implementieren, die die Integration elektronischer Gesundheitsakten und die Fernüberwachung von Infektionskrankheiten unterstützen, aber ihre höheren Kosten begrenzen die sofortige großflächige Einführung.
- Zum Beispiel integriert der Accula™ Flu A/Flu B-Test von Thermo Fisher Scientific die RT-PCR-Technologie in eine tragbare, handflächengroße Plattform und liefert in der Regel bestätigte Ergebnisse in 30 Minuten, während seine Instrumentierung automatisierte Onboard-Kontrollen und digitale Ausgaben unterstützt, die die manuelle Variabilität, die mit visuellen Interpretationstests verbunden ist, erheblich reduzieren.
Nach Technologie
Immunochromatographische Assays dominieren den Markt mit einem ungefähren Marktanteil von 52%, angetrieben durch ihre schnelle Durchlaufzeit, vereinfachte Arbeitsabläufe und Kompatibilität mit dezentralen Testumgebungen. Diese Assays bleiben der Standard für die Influenza-Erstuntersuchung in kommunalen Gesundheitszentren. Lateral-Flow-Assays expandieren in der ambulanten und apothekenbasierten Testung aufgrund ihrer Benutzerfreundlichkeit, während PCR-basierte RIDTs stark wachsen, da molekulare Plattformen schnellere Bearbeitungszeiten unter 20 Minuten mit höherer Empfindlichkeit erreichen. Die verstärkte Entwicklung von Multiplex-Molekularpanels und automatisierten kartuschenbasierten Systemen beschleunigt die Einführung in hochakuten Versorgungseinrichtungen weiter.
- Zum Beispiel ist der OSOM® Ultra Flu A&B-Test von SEKISUI Diagnostics ein instrumentenfreier, schneller Immunoassay, der visuelle Ergebnisse in 10 Minuten liefert und ein proprietäres monoklonales Antikörpersystem integriert, das die Antigenbindungsaffinität verbessern soll.
Nach Probentyp
Nasentupfer halten die führende Position mit einem nahezu Marktanteil von 64%, unterstützt durch höhere Virenlast-Rückgewinnung, bessere diagnostische Empfindlichkeit und weit verbreitete klinische Richtlinienempfehlungen für Influenza-Tests. Ihre nicht-invasive Sammlungsmethode macht sie in pädiatrischen und erwachsenen Populationen bevorzugt, was eine konstante Nachfrage in Krankenhäusern und ambulanten Zentren antreibt. Rachentupfer bleiben in Nischenanwendungen, stehen jedoch vor Einschränkungen in der Empfindlichkeit, was eine breitere Akzeptanz begrenzt. Andere Probentypen, einschließlich nasopharyngealer Aspirate und Waschungen, bleiben in spezialisierten Diagnoselabors relevant, wo eine verbesserte Erkennungsgenauigkeit erforderlich ist, insbesondere bei schweren Infektionen oder Beurteilungen von immungeschwächten Patienten.
Wichtige Wachstumsfaktoren
- Steigende globale Influenza-Belastung und Nachfrage nach schneller Erkennung
Die zunehmende Inzidenz von saisonaler und pandemischer Influenza treibt die Nachfrage nach schnellen Influenza-Diagnosetests (RIDTs) stark an, da Gesundheitsdienstleister die Früherkennung priorisieren, um Übertragung und Komplikationen zu reduzieren. Hoher Patientenzustrom in ambulanten Kliniken, Notfallzentren und Notaufnahmen beschleunigt die Einführung schneller Point-of-Care-Screenings. Klare Vorteile wie schnelle Durchlaufzeit, vereinfachte Probenahme und sofortige klinische Entscheidungsfindung verbessern die Marktdurchdringung. Von der Regierung geführte Influenza-Überwachungsprogramme und Impfkampagnen verstärken weiter die Notwendigkeit schneller, zuverlässiger Diagnosetools zur Bewältigung jährlicher Influenza-Spitzen.
- Zum Beispiel berichtet F. Hoffmann-La Roche Ltd, dass ihr cobas® Liat® Influenza A/B-Test vollautomatisierte RT-PCR-Ergebnisse in 20 Minuten liefert, mit einem integrierten Probenvorbereitungssystem, das Abstrichproben mit einer geschlossenen Röhrenarchitektur verarbeitet, die das Kontaminationsrisiko minimiert und eine Hands-on-Zeit von weniger als 1 Minute unterstützt.
- Technologische Fortschritte zur Verbesserung der diagnostischen Genauigkeit
Fortschritte in immunochromatographischen Tests, digitalen Lesegeräten und molekularen Amplifikationstechnologien verbessern die Sensitivität und Spezifität von RIDTs erheblich. Hersteller konzentrieren sich auf die Entwicklung von Plattformen, die eine Genauigkeit nahe der PCR bieten und gleichzeitig die Benutzerfreundlichkeit am Point-of-Care beibehalten, was eine bessere Identifizierung von Influenza A- und B-Stämmen ermöglicht. Die Integration digitaler Analysatoren minimiert menschliche Interpretationsfehler und unterstützt die Datenkonnektivität für die klinische Entscheidungsunterstützung. Kontinuierliche F&E-Investitionen, verbesserte Antigennachweismaterialien und erhöhte Reagenzienstabilität stärken das klinische Vertrauen in RIDTs und fördern eine breitere Akzeptanz in Krankenhäusern, Apotheken und dezentralen Testeinrichtungen.
- Zum Beispiel berichtet Abbott Laboratories, dass ihr ID NOW™ Influenza A & B 2-Test isothermale Nukleinsäureamplifikation verwendet, um bestätigte Ergebnisse in 13 Minuten zu liefern, wobei positive Nachweise oft in weniger als 6 Minuten gekennzeichnet werden, und dass ihr tragbares Instrument bei jedem Durchlauf automatisierte interne Kontrollprüfungen durchführt, um die analytische Integrität zu gewährleisten.
- Erweiterung dezentraler und häuslicher Tests
Die zunehmende Akzeptanz dezentraler Testmodelle treibt den Markt voran, da Patienten zunehmend auf Schnelltests außerhalb traditioneller Gesundheitseinrichtungen angewiesen sind. Die Erweiterung von Einzelhandelskliniken, häuslichen Diagnosen und der Verfügbarkeit von OTC-Tests stärkt die Zugänglichkeit und fördert ein frühes Testverhalten. Das steigende Bewusstsein der Verbraucher für Selbstscreening nach COVID-19 unterstützt die Akzeptanz intuitiver RIDTs mit einfachen Probennahmemethoden. Hersteller entwickeln kompakte, benutzerfreundliche Kits, die sofortige Ergebnisse liefern und regulatorische Standards erfüllen, was das Marktwachstum beschleunigt. Dieser Wandel hin zu bequemen, verteilten Testökosystemen ergänzt Telemedizin-Dienste und steigert den Gesamtverbrauch von RIDTs.
Wichtige Trends & Chancen
- Steigende Integration digitaler und vernetzter Diagnoseplattformen
Ein wichtiger Trend konzentriert sich auf die Entwicklung digital vernetzter RIDT-Systeme, die diagnostische Daten in Echtzeit erfassen, speichern und übertragen. Diese Plattformen unterstützen die automatisierte Ergebnisinterpretation, verbessern die klinische Genauigkeit und ermöglichen gleichzeitig die Fernüberwachung und Influenzabeobachtung. Die Konnektivität mit elektronischen Gesundheitsakten und öffentlichen Gesundheitsdatenbanken verbessert die Ausbruchserfassung und Ressourcenallokation. Der Trend bietet Herstellern die Möglichkeit, künstliche Intelligenz, smartphone-basierte Lesegeräte und cloud-verbundene Lösungen zu integrieren, wodurch die Rolle von RIDTs in der präzisen Diagnostik und der Überwachung von Infektionen auf Bevölkerungsebene gestärkt wird.
- Zum Beispiel bietet Meridian Bioscience, Inc. die Alethia®-Molekularplattform an, die die Daten der Testläufe digital archiviert und Influenza A/B-Ergebnisse in etwa 1 Stunde über die loopvermittelte isotherme Amplifikation (LAMP) liefert.
- Wachsendes Potenzial in Apotheken und Einzelhandelskliniken
Die rasche Expansion der Einzelhandelsgesundheitsinfrastruktur schafft starke kommerzielle Chancen für RIDTs. Apotheken und Walk-in-Kliniken bieten zunehmend Influenza-Screenings als Teil der Point-of-Care-Diagnosedienste an. Ihre hohe Zugänglichkeit, erweiterten Öffnungszeiten und niedrigeren Beratungskosten ziehen Patienten an, die sofortige Tests suchen. Da die Regulierungsbehörden weiterhin diagnostische Protokolle unter der Leitung von Apothekern unterstützen, steigt die Nachfrage nach kompakten, schnell ablesbaren RIDTs. Dieser Wandel eröffnet Herstellern Möglichkeiten zur Zusammenarbeit mit Einzelhandelsketten, zur gemeinsamen Entwicklung von workflow-optimierten Testkits und zur Erweiterung der Marktreichweite in städtischen und vorstädtischen Gebieten.
- Zum Beispiel bietet Hologic, Inc. den Panther Fusion® Flu A/B/RSV-Assay an, der Proben mit vollautomatisierter PCR in 2,5 Stunden verarbeitet und kontinuierliches Probenladen von bis zu 120 Proben ermöglicht, sodass Apotheken und Kliniknetzwerke die Influenza-Testkapazität skalieren können, während eine nachvollziehbare digitale Berichterstattung über vernetzte Standorte hinweg aufrechterhalten wird.
- Entwicklung von Multiplex- und Multi-Pathogen-Testpanels
Eine Schlüsselchance ergibt sich aus der steigenden Nachfrage nach Multiplex-Assays, die Influenza zusammen mit RSV, SARS-CoV-2 und anderen Atemwegserregern in einem einzigen Test nachweisen können. Gesundheitssysteme bevorzugen diese Panels wegen ihrer Effizienz, umfassenden diagnostischen Ergebnisse und reduzierten Ressourcenbelastung. Die Kombination mehrerer Analyten verbessert die Genauigkeit der klinischen Entscheidungsfindung und passt sich der Variabilität der Atemwegssaison an. Hersteller, die in kompakte, multi-target RIDTs investieren, können sich einen erheblichen Wettbewerbsvorteil verschaffen, insbesondere in Akutpflegeeinrichtungen und Umgebungen mit hohem Testvolumen.
Wichtige Herausforderungen
- Begrenzte Sensitivität im Vergleich zu molekularen Diagnostiken
Trotz Verbesserungen weisen viele konventionelle RIDTs immer noch eine geringere Sensitivität im Vergleich zu molekularen Assays auf, insbesondere in frühen Infektionsstadien oder bei niedrigen Viruslastbedingungen. Diese Einschränkung erhöht das Risiko von falsch-negativen Ergebnissen, was die Genauigkeit klinischer Entscheidungen beeinträchtigt und einige Institutionen dazu veranlasst, sich auf bestätigende PCR-Tests zu verlassen. Die Variabilität der Probenentnahmequalität beeinflusst ebenfalls die Testleistung. Diese Herausforderungen schränken die Akzeptanz von RIDTs in risikoreichen klinischen Umgebungen ein und zwingen Hersteller, in verbesserte Reagenzienchemie, digitale Leser und hybride Plattformen zu investieren, um die diagnostische Zuverlässigkeit zu verbessern.
- Regulatorische Compliance und Leistungsstandarddruck
Die Stärkung globaler regulatorischer Rahmenbedingungen, einschließlich strengerer Genauigkeitsanforderungen und Qualitätsvalidierungsprotokolle, stellt für Hersteller Herausforderungen dar. Die Einhaltung aktualisierter Leistungsbenchmarks, Notfallzulassungen und Anforderungen an die Marktüberwachung erhöht die Entwicklungskosten und -zeiten. Kleinere Unternehmen stehen vor größeren Hürden bei der Erfüllung analytischer Sensitivitätsstandards und der Sicherstellung der Konsistenz über Produktionschargen hinweg. Darüber hinaus erfordert die rasche technologische Entwicklung kontinuierliche Upgrades, um die regulatorische Ausrichtung aufrechtzuerhalten. Diese Druckfaktoren erschweren den Markteintritt und die langfristige Wettbewerbsfähigkeit, insbesondere für neue Akteure im Diagnosetest-Ökosystem.
Regionale Analyse
Nordamerika
Nordamerika hält die dominierende Position im Markt für schnelle Influenza-Diagnosetests (RIDT) mit einem geschätzten Marktanteil von 38%, unterstützt durch eine fortschrittliche Gesundheitsinfrastruktur, starke Akzeptanz dezentraler Tests und robuste Influenza-Überwachungsprogramme. Hohe Testvolumina in Krankenhäusern, Notfallzentren und Einzelhandelskliniken verstärken die Nachfrage nach Produkten, während günstige Erstattungsstrukturen die weitverbreitete klinische Nutzung fördern. Die Region profitiert von starker behördlicher Aufsicht, schneller Technologieübernahme und anhaltenden F&E-Investitionen, die die diagnostische Genauigkeit verbessern. Steigendes Bewusstsein für Selbsttests und die Integration von digitalen Lesegerät-basierten Schnellkits stärken die Marktexpansion in den Vereinigten Staaten und Kanada weiter.
Europa
Europa macht etwa 27% des RIDT-Marktes aus, angetrieben durch koordinierte öffentliche Gesundheitspolitiken, hohe Influenza-Impfabdeckung und starken Fokus auf die frühzeitige Erkennung von Atemwegsinfektionen. Länder wie Deutschland, das Vereinigte Königreich und Frankreich führen die Akzeptanz aufgrund gut etablierter Diagnosenetzwerke und zunehmender Verbreitung digitaler Schnelltestplattformen an. Saisonale Grippeausbrüche und alternde Bevölkerungen tragen zu einer erhöhten Testnachfrage bei. Der Fokus der Region auf leistungsstarke Diagnostik und strenge Qualitätsstandards treibt die Innovation der Hersteller an. Erweiterte, apothekengeführte Point-of-Care-Testprogramme und verbesserte Erstattungspfade unterstützen das kontinuierliche Marktwachstum in West- und Osteuropa.
Asien-Pazifik
Asien-Pazifik erfasst nahezu 24% des RIDT-Marktes, unterstützt durch steigende Influenza-Prävalenz, Ausbau der diagnostischen Infrastruktur und schnelle Urbanisierung. Große Märkte wie China, Japan, Südkorea und Indien investieren stark in Schnelltestplattformen, um der hohen Bevölkerungsdichte und den Risiken saisonaler Ausbrüche zu begegnen. Wachsende Sensibilisierung für frühzeitige Diagnosen, erhöhte Gesundheitsausgaben und Regierungsüberwachungsprogramme beschleunigen die Akzeptanz in der Primärversorgung und in gemeindenahen Einrichtungen. Hersteller profitieren von der starken Nachfrage nach kostengünstigen, hochdurchsatzfähigen RIDTs, die auf unterschiedliche klinische Umgebungen zugeschnitten sind. Die große Patientenbasis der Region und sich entwickelnde Modelle von Einzelhandelskliniken erweitern weiterhin die Marktdurchdringung.
Lateinamerika
Lateinamerika repräsentiert etwa 7% des RIDT-Marktes, angetrieben durch einen zunehmenden Fokus auf das Management von Infektionskrankheiten und steigende Influenza-Testquoten in Brasilien, Mexiko, Argentinien und Chile. Das Wachstum beschleunigt sich, da Regierungen die Überwachung von Atemwegserkrankungen stärken und den Zugang zu Diagnosen in öffentlichen und privaten Gesundheitseinrichtungen verbessern. Städtische Krankenhäuser führen die Akzeptanz an, während Gemeindekliniken allmählich die Nutzung von schnellen immunochromatographischen Tests ausweiten. Begrenzte Laborinfrastruktur in ländlichen Gebieten erhöht die Abhängigkeit von erschwinglichen Point-of-Care-RIDTs. Wirtschaftliche Einschränkungen bleiben eine Herausforderung, doch erweiterte Beschaffungsprogramme und Partnerschaften mit internationalen Diagnostikunternehmen unterstützen die stetige Marktentwicklung.
Mittlerer Osten & Afrika
Die Region Mittlerer Osten & Afrika macht schätzungsweise 4% des Marktanteils aus, was allmähliche Verbesserungen der Gesundheitskapazität und ein wachsendes Bewusstsein für Influenza-Screening widerspiegelt. Golfstaaten wie Saudi-Arabien und die VAE investieren in fortschrittliche Diagnosetechnologien und erweitern die Schnelltestkapazitäten in Krankenhäusern, Flughäfen und Einrichtungen des betrieblichen Gesundheitswesens. In Afrika wird die Nachfrage durch den Bedarf an erschwinglichen, einfach zu verwendenden RIDTs aufgrund begrenzter molekularer Testinfrastruktur angetrieben. Internationale Gesundheitsinitiativen unterstützen die Verteilung in Primärkliniken, während zunehmende Investitionen des privaten Sektors die Akzeptanz beschleunigen. Budgetbeschränkungen und Inkonsistenzen in der Lieferkette moderieren jedoch das allgemeine Marktwachstum.
Marktsegmentierungen:
Nach Produkttyp:
- Konventionelle RIDTs
- Digitale RIDTs
Nach Technologie:
- Immunochromatographische Tests
- Lateral-Flow-Tests
Nach Probentyp:
- Nasenabstrich
- Rachenabstrich
Nach Geografie
- Nordamerika
- Europa
- Deutschland
- Frankreich
- Vereinigtes Königreich
- Italien
- Spanien
- Rest von Europa
- Asien-Pazifik
- China
- Japan
- Indien
- Südkorea
- Südostasien
- Rest von Asien-Pazifik
- Lateinamerika
- Brasilien
- Argentinien
- Rest von Lateinamerika
- Mittlerer Osten & Afrika
- GCC-Länder
- Südafrika
- Rest des Mittleren Ostens und Afrikas
Wettbewerbslandschaft
Die Wettbewerbslandschaft des Marktes für schnelle Influenza-Diagnosetests (RIDT) umfasst Akteure wie Thermo Fisher Scientific, Inc., SEKISUI Diagnostics, F. Hoffmann-La Roche Ltd, Abbott Laboratories, Meridian Bioscience, Inc., Hologic, Inc., Quidel Corporation, SA Scientific Ltd, Becton, Dickinson and Company (BD) und 3M Company. Der Markt für schnelle Influenza-Diagnosetests (RIDT) wird durch kontinuierliche Fortschritte in der schnellen Antigennachweistechnologie, erweiterte Point-of-Care-Testmöglichkeiten und die zunehmende Integration digitaler Diagnoseplattformen definiert. Unternehmen konzentrieren sich darauf, die Testempfindlichkeit zu verbessern, schnellere klinische Entscheidungen zu ermöglichen und groß angelegte Influenza-Überwachungsprogramme zu unterstützen. Die Produktdifferenzierung konzentriert sich auf verbesserte Assay-Genauigkeit, benutzerfreundliche Formate und Kompatibilität mit dezentralen Testumgebungen wie Apotheken, Notfallzentren und häuslichen Umgebungen. Starke F&E-Investitionen, regulatorische Zulassungen für die nächste Generation von Schnellkits und strategische Kooperationen mit Gesundheitsdienstleistern stärken die Marktpositionierung. Da sich das Management von Atemwegserkrankungen weiterentwickelt, priorisieren Hersteller skalierbare Produktion, erweiterte Vertriebskanäle und datengestützte Lösungen, um die weltweite Nachfrage zu decken.
Analyse der Hauptakteure
- Thermo Fisher Scientific, Inc.
- SEKISUI Diagnostics
- Hoffmann-La Roche Ltd
- Abbott Laboratories
- Meridian Bioscience, Inc.
- Hologic, Inc.
- Quidel Corporation
- SA Scientific Ltd
- Becton, Dickinson and Company (BD)
- 3M Company
Neueste Entwicklungen
- Im Oktober 2024 genehmigte die FDA den Healgen Rapid Check COVID-19/Flu A&B Antigen Test für den Markt. Dieser Heimtest, der einen Nasenabstrich verwendet, kann sowohl COVID-19 als auch Influenza A & B nachweisen. Er ist rezeptfrei erhältlich und liefert Ergebnisse in nur 15 Minuten. Dies ist der erste rezeptfreie Grippetest, der eine Marktzulassung außerhalb der Notfallverwendung erhält.
- Im Juni 2024 arbeitete das NIH im Rahmen seines RADx Tech Independent Test Assessment Program (ITAP) mit Diagnostikherstellern zusammen, um die Überprüfung und Genehmigung von Multiplex-Tests zu beschleunigen, die sowohl COVID-19 als auch Grippe A/B nachweisen. Diese Bemühung zielt darauf ab, die Verfügbarkeit von schnellen Point-of-Care (POC)- und Heimtests zu erhöhen, die für eine schnelle Diagnose und Behandlung unerlässlich sind.
- Im Mai 2024 arbeitete Danaher mit der Johns Hopkins University zusammen, um neue Methoden zur Diagnose von Schädel-Hirn-Traumata zu entwickeln. Die Wissenschaftler der Johns Hopkins University konzentrieren sich auf die Bewertung neuer blutbasierter Biomarker unter Nutzung hochsensibler Technologie von Beckmann Coulter.
- Im März 2024 erhielt das Joint Venture von Co-Diagnostics, Inc., CoSara, die Genehmigung der indischen Regulierungsbehörden für seinen Influenza Multiplex PCR Test. Dieser Test kann mehrere Influenzastämme gleichzeitig nachweisen und ist somit ein effizienteres Diagnosewerkzeug für Gesundheitsdienstleister. Diese Genehmigung ist ein bedeutender Schritt zur Verbesserung des Zugangs zu fortschrittlichen Diagnosetests in Indien.
Shape Your Report to Specific Countries or Regions & Enjoy 30% Off!
Berichtsabdeckung
Der Forschungsbericht bietet eine eingehende Analyse basierend auf Produkttyp, Technologie, Probentyp und Geografie. Er beschreibt führende Marktteilnehmer und bietet einen Überblick über ihr Geschäft, ihre Produktangebote, Investitionen, Einnahmequellen und wichtige Anwendungen. Darüber hinaus enthält der Bericht Einblicke in das Wettbewerbsumfeld, SWOT-Analyse, aktuelle Markttrends sowie die wichtigsten Treiber und Einschränkungen. Des Weiteren werden verschiedene Faktoren erörtert, die das Marktwachstum in den letzten Jahren vorangetrieben haben. Der Bericht untersucht auch Marktdynamiken, regulatorische Szenarien und technologische Fortschritte, die die Branche prägen. Er bewertet die Auswirkungen externer Faktoren und globaler wirtschaftlicher Veränderungen auf das Marktwachstum. Schließlich bietet er strategische Empfehlungen für Neueinsteiger und etablierte Unternehmen, um die Komplexitäten des Marktes zu navigieren.
Zukunftsausblick
- Der Markt wird sich erweitern, da Gesundheitssysteme die schnelle und genaue Erkennung von saisonaler und pandemischer Influenza priorisieren.
- Die Einführung von digitalen und leserbasierten RIDTs wird zunehmen, um die Interpretationsgenauigkeit und Datenkonnektivität zu verbessern.
- Multiplex-Respirationspanels werden an Bedeutung gewinnen, da Kliniker die Einzelnachweis von mehreren Erregern bevorzugen.
- Heim- und OTC-Schnelltests für Influenza werden ein starkes Wachstum verzeichnen, angetrieben durch steigende Trends zur Selbstdiagnose.
- Apotheken und Einzelhandelskliniken werden durch die Erweiterung der Point-of-Care-Tests eine größere Rolle bei der Influenza-Testung spielen.
- Hersteller werden in Tests mit höherer Sensitivität investieren, um mit molekularen Testalternativen zu konkurrieren.
- Regierungen werden Influenza-Überwachungsprogramme stärken, was zu höheren Beschaffungsvolumina von Tests führt.
- Schwellenmärkte werden die Einführung beschleunigen, da sich die diagnostische Infrastruktur und das Bewusstsein verbessern.
- Strategische Kooperationen zwischen Diagnostikentwicklern und Gesundheitsnetzwerken werden zunehmen.
- Nachhaltigkeit und kosteneffiziente Produktion werden wichtig, da die Nachfrage sich auf Massenmarkt-Schnellkits verlagert.

 Marktsegmentierungsanalyse:
Marktsegmentierungsanalyse:

