Markedsoversigt:
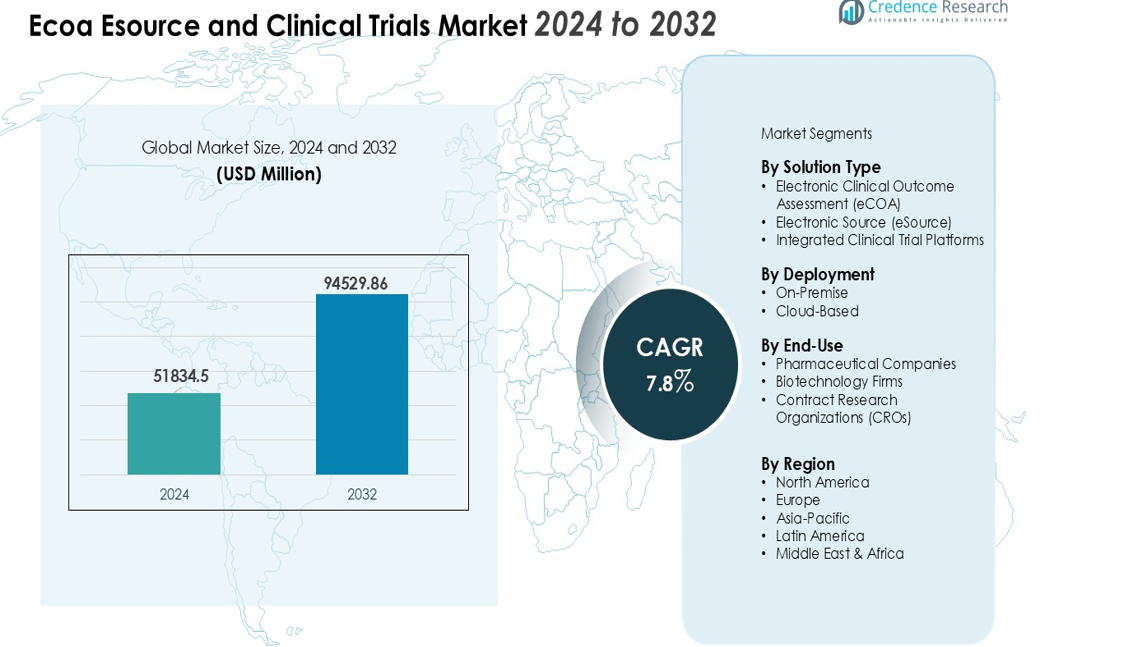
Størrelsen på Ecoa Esource og Clinical Trials-markedet blev vurderet til USD 51834,5 millioner i 2024 og forventes at nå USD 94529,86 millioner i 2032, med en CAGR på 7,8% i prognoseperioden (2024-2032).
| RAPPORT ATTRIBUTE |
DETALJER |
| Historisk periode |
2020-2023 |
| Basisår |
2024 |
| Prognoseperiode |
2025-2032 |
| eCOA, eSource og Clinical Trials Markedsstørrelse 2024 |
USD 51834,5 millioner |
| eCOA, eSource og Clinical Trials Marked, CAGR |
7,8% |
| eCOA, eSource og Clinical Trials Markedsstørrelse 2032 |
USD 94529,86 millioner |
Vigtige markedsdrivere inkluderer det stigende volumen og kompleksitet af kliniske forsøg verden over, hvilket kræver strømlinet elektronisk dataindsamling, realtidsmonitorering og sikker datastyring. Skiftet mod decentraliserede og patientcentrerede kliniske forsøg, muliggjort af fjernovervågning, bærbare enheder, mobile sundhedsapplikationer og cloud-baserede elektroniske platforme, har yderligere accelereret adoptionen af eCOA og eSource-løsninger. Derudover styrker regulatorisk opmuntring til elektroniske kliniske resultatvurderinger og det voksende behov for dataintegritet, gennemsigtighed og effektivitet markedsudvidelsen.
Regionalt fører Nordamerika markedet, støttet af avanceret farmaceutisk F&U-infrastruktur, tidlig teknologiadoption og gunstige regulatoriske rammer. I mellemtiden er Asien-Stillehavsområdet ved at blive den hurtigst voksende region på grund af stigende kliniske forskningsaktiviteter, outsourcing af forsøg og adoption af digitale forsøgsstyringsløsninger, hvilket præsenterer betydelige vækstmuligheder for markedet.
Markedsindsigt:
- Ecoa Esource og Clinical Trials Market blev vurderet til USD 51.834,5 millioner i 2024 og forventes at nå USD 94.529,86 millioner i 2032, med en vækst på CAGR på 7,8%.
- Den stigende kompleksitet og mængde af globale kliniske forsøg driver efterspørgslen efter digitale løsninger, der muliggør realtidsdatafangst, reducerer fejl og sikrer overholdelse af protokoller.
- Decentraliserede og patientcentrerede forsøg fremskynder adoptionen af eCOA og eSource-løsninger, understøttet af bærbare enheder, mobile sundhedsapps og fjernovervågningsplatforme.
- Regulatorisk støtte til elektroniske kliniske resultatvurderinger forbedrer markedsadoptionen og muliggør præcise, sporbare og reviderbare forsøgsdata.
- Fokus på dataintegritet, gennemsigtighed og operationel effektivitet motiverer farmaceutiske og bioteknologiske virksomheder til at adoptere integrerede digitale forsøgsstyringsplatforme.
- Høje implementeringsomkostninger, kompleks integration med ældre systemer og strenge databeskyttelseskrav udgør udfordringer for udbredt adoption.
- Regionalt fører Nordamerika med 42% markedsandel på grund af avanceret F&U-infrastruktur, Europa har 28% understøttet af regulatorisk harmonisering, og Asien-Stillehavsområdet repræsenterer 20% og vokser hurtigst på grund af stigende kliniske forskningsaktiviteter og outsourcing.
Access crucial information at unmatched prices!
Request your sample report today & start making informed decisions powered by Credence Research Inc.!
Download Sample
Markedsdrivere:
Stigende kompleksitet og volumen af kliniske forsøg driver adoption af digitale løsninger
Den stigende kompleksitet og volumen af kliniske forsøg globalt har skabt et stærkt behov for digitale løsninger. Sponsorer kræver præcis, realtids dataindsamling for at sikre forsøgets effektivitet og patientsikkerhed. Ecoa, eSource og Clinical Trials Market drager fordel af sin evne til at strømline datastyring på tværs af flere steder. Det reducerer fejl i dataindtastning og fremskynder overholdelse af protokoller. Denne effektivitet hjælper organisationer med at opfylde regulatoriske krav, mens de håndterer større og mere komplekse studier.
- For eksempel integrerer Medable, en pioner inden for decentraliserede kliniske forsøg, telemedicin, ePRO og fjernovervågningsteknologier, hvilket muliggør realtids dataadgang og samarbejde på tværs af steder, hvilket hjalp med at reducere sitebesøg med 30% i nylige studier.
Skift mod decentraliserede og patientcentrerede kliniske forsøg øger markedsdemanden
Kliniske forsøg bevæger sig mod decentraliserede modeller, med fokus på patientkomfort og fjernadgang. Det muliggør datafangst fra bærbare enheder, mobile sundhedsapplikationer og hjemmebaserede overvågningssystemer. Ecoa, eSource og Clinical Trials Market understøtter denne transformation ved at tilbyde sikker, realtidsadgang til patientrapporterede resultater. Organisationer opnår fleksibilitet og bedre engagement med deltagere. Denne trend øger efterspørgslen efter digitale kliniske forsøgsplatforme, der er i stand til fjernovervågning.
- For eksempel gjorde Science 37’s løsning til patientrekruttering det muligt for kunder at tilmelde 42% af en forsøgsgruppe på otte uger til en undersøgelse af en sjælden sygdom. Virksomheden rapporterer også, at dens teknologiplatform accelererer tilmeldingen op til 15 gange hurtigere end traditionelle metoder, hvilket leverer 100% medicinsk kvalificerede henvisninger.
Regulatorisk opmuntring til elektroniske kliniske resultatvurderinger driver implementering
Reguleringsmyndigheder støtter i stigende grad elektroniske metoder til kliniske resultatvurderinger. Det forbedrer nøjagtigheden, sporbarheden og reviderbarheden af forsøgsdata. Overholdelse af disse regler er afgørende for globale forsøgs godkendelser. eCOA, eSource og Clinical Trials Market leverer standardiserede elektroniske løsninger til at opfylde disse krav. Virksomheder drager fordel af hurtigere regulatorisk gennemgang og reduceret risiko for datadiscrepans.
Stigende fokus på dataintegritet, gennemsigtighed og operationel effektivitet
Farmaceutiske og bioteknologiske virksomheder prioriterer dataintegritet og operationel effektivitet i kliniske forsøg. Det sikrer pålidelige resultater og opretholder sponsorens troværdighed. eCOA, eSource og Clinical Trials Market muliggør konsekvent datainfangst, sikker opbevaring og strømlinet rapportering. Organisationer reducerer manuelle fejl og sparer tid under analysen. Dette fokus på høj kvalitet, gennemsigtige data fortsætter med at drive adoptionen af digitale forsøgsstyringsløsninger.
Markedstendenser:
Integration af avancerede digitale teknologier forbedrer effektiviteten af kliniske forsøg
eCOA, eSource og Clinical Trials Market viser en stærk tendens mod integration af avancerede digitale teknologier, herunder cloud computing, kunstig intelligens og maskinlæring. Det gør det muligt for sponsorer at analysere store mængder kliniske data i realtid og identificere mønstre, der understøtter hurtigere beslutningstagning. Fjernovervågningsenheder og mobilapplikationer leverer kontinuerlige datastrømme direkte til forsøgsdatabaser. Det reducerer operationelle forsinkelser og forbedrer protokoloverholdelse på tværs af flere undersøgelsessteder. Organisationer stoler i stigende grad på disse teknologier for at forbedre forsøgs kvalitet og minimere omkostninger. Datavisualiseringsværktøjer og automatiserede rapporteringsfunktioner hjælper interessenter med effektivt at overvåge forsøgsfremskridt.
- For eksempel gør WeTrials-platformen det muligt for patienter at få fjernadgang og leverer uddannelsesressourcer og personlig vejledning for at hjælpe deltagere med at finde og navigere i kliniske forsøg, hvilket demonstrerer en indsats for at forbedre patientengagement og strømline operationer i studier med flere steder.
Udvidelse af decentraliserede forsøg og fokus på patientcentrerede tilgange
Decentraliserede kliniske forsøg fortsætter med at vinde frem, med vægt på patientbekvemmelighed og fjern deltagelse. eCOA, eSource og Clinical Trials Market understøtter disse forsøg ved at levere sikre elektroniske datafangst- og styringsløsninger. Det muliggør direkte patientinput gennem mobile enheder, bærbare sensorer og hjemmebaseret overvågning, hvilket sikrer realtidsadgang for forskere. Denne tilgang forbedrer patientengagement og fastholdelse, mens dataintegriteten opretholdes. Sponsorer adopterer platforme, der tillader integration af flere datakilder for et holistisk syn på forsøgsresultater. Digitale forsøgsplatforme letter hurtigere rekruttering og udvider adgangen til forskellige patientpopulationer. Markedstendensen afspejler en vedvarende bevægelse mod mere fleksible, teknologidrevne og patientfokuserede kliniske forskningsstrategier.
- For eksempel bygger Science 37 globale decentraliserede forsøgsnetværk, der letter diversificeret patientrekruttering, hvilket fører til bredere adgang og forbedret resultatrobusthed.
Analyse af Markedsudfordringer:
Høje Implementeringsomkostninger og Kompleks Integration Hæmmer Adoptering
Markedet for eCOA, eSource og Kliniske Forsøg står over for udfordringer fra høje implementeringsomkostninger og kompleksiteten ved at integrere digitale løsninger i eksisterende kliniske arbejdsgange. Det kræver betydelige investeringer i teknologiinfrastruktur, medarbejderuddannelse og løbende vedligeholdelse. Mindre organisationer finder ofte adoption økonomisk belastende. Datamigrering fra ældre systemer kan forsinke implementering og forstyrre igangværende forsøg. Kompatibilitetsproblemer med forskellige elektroniske systemer kan påvirke problemfri dataflow. Disse barrierer bremser udbredt adoption på trods af fordelene ved forbedret effektivitet og data nøjagtighed.
Bekymringer om Databeskyttelse, Regulatorisk Overholdelse og Sikkerhed Begrænser Vækst
Databeskyttelse og regulatorisk overholdelse forbliver kritiske udfordringer for markedet for eCOA, eSource og Kliniske Forsøg. Det skal overholde strenge standarder for patientfortrolighed, databeskyttelse og grænseoverskridende informationsoverførsel. Enhver sikkerhedsbrist kan underminere tilliden og føre til regulatoriske sanktioner. Variationer i regler på tværs af regioner komplicerer forsøgsstyring for multinationale studier. Organisationer skal investere i robuste cybersikkerhedsforanstaltninger og overholdelsesprotokoller. Håndtering af store mængder følsomme kliniske data, samtidig med at nøjagtighed og tilgængelighed opretholdes, tilføjer operationel kompleksitet. Disse udfordringer begrænser markedsvækst og kræver strategisk planlægning for sikker og overholdende implementering.
Markedsmuligheder:
Udvidelse af Decentraliserede og Fjernkliniske Forsøg Skaber Vækstpotentiale
Markedet for eCOA, eSource og Kliniske Forsøg præsenterer betydelige muligheder gennem udvidelsen af decentraliserede og fjernkliniske forsøg. Det gør det muligt for sponsorer at nå bredere patientpopulationer og reducere geografiske barrierer i forsøgsrekruttering. Digitale platforme understøtter realtidsdatafangst fra bærbare enheder, mobilapps og hjemmebaserede overvågningssystemer. Organisationer kan forbedre patientengagement og fastholdelse, samtidig med at de opretholder høj datakvalitet. Integration af flere datakilder muliggør omfattende analyse af forsøgsresultater. Den voksende efterspørgsel efter fleksible, patientcentrerede forsøgsdesign tilbyder vedvarende markedspotentiale.
Adoption af Avanceret Analyse og Kunstig Intelligens Forbedrer Markedsudsigter
Stigende adoption af avanceret analyse, kunstig intelligens og maskinlæring tilbyder yderligere muligheder for markedet for eCOA, eSource og Kliniske Forsøg. Det muliggør effektiv behandling af store mængder kliniske data og identifikation af forudsigelige indsigter. Sponsorer kan optimere forsøgsdesign, overvåge patientsikkerhed og fremskynde beslutningstagning. Automatisering af rapportering og risikostyring forbedrer operationel effektivitet. Den voksende interesse for virkelighedsbaseret evidens og digitale biomarkører understøtter yderligere teknologiintegration. Disse fremskridt positionerer markedet for fortsat vækst og innovation inden for klinisk forskning.
Analyse af Markedssegmentering:
Efter Løsningstype
Markedet for eCOA, eSource og kliniske forsøg er segmenteret efter løsningstype i elektronisk klinisk resultatvurdering (eCOA), elektronisk kilde (eSource) og integrerede kliniske forsøgsplatforme. Det giver organisationer mulighed for at vælge løsninger baseret på forsøgets kompleksitet og datakrav. eCOA-løsninger dominerer adoptionen på grund af deres evne til effektivt at indfange patientrapporterede resultater og opretholde dataintegritet. eSource-platforme understøtter direkte datafangst fra elektroniske medicinske journaler, hvilket reducerer manuelle fejl og fremskynder forsøgsforløb. Integrerede platforme tilbyder end-to-end forsøgsstyring, der kombinerer dataindsamling, overvågning og rapportering i et samlet system. Disse løsninger forbedrer operationel effektivitet og forbedrer den overordnede forsøgs kvalitet.
- For eksempel integrerer ICON Digital Platform eConsent, eCOA, eSource og telebesøgsmoduler for at lette decentraliserede kliniske forsøg, hvilket resulterer i en rapporteret 20% forbedring i patientengagement og en 15% reduktion i forsøgets operationelle kompleksiteter.
Efter Implementeringsmetode
Implementering i markedet for eCOA, eSource og kliniske forsøg inkluderer on-premise og cloud-baserede løsninger. Det tilbyder fleksibilitet til at imødekomme de specifikke infrastruktur- og sikkerhedsbehov hos forskellige organisationer. Cloud-baseret implementering leder markedet på grund af dens skalerbarhed, fjernadgang og reducerede IT-administrationsomkostninger. On-premise implementering forbliver relevant for organisationer, der kræver fuld kontrol over datalagring og interne systemer. Begge implementeringstyper muliggør adgang til data i realtid og understøtter decentraliserede forsøgsmodeller. Adoption afhænger af forsøgsstørrelse, datasensitivitet og organisatoriske IT-kapaciteter.
- For eksempel opnår Castor eCOA-platformen 90% af brugeraccepttestens færdiggørelse inden for 4 uger, mens den opretholder robust validering i et moderne, cloud-native miljø.
Efter Slutanvendelse
Slutanvendelsessegmenter inkluderer medicinalvirksomheder, bioteknologiske firmaer og kontraktforskningsorganisationer (CRO’er). Det hjælper sponsorer med at håndtere komplekse forsøg, sikre overholdelse af regler og fremskynde lægemiddeludvikling. Medicinalvirksomheder har den største andel på grund af høje F&U-investeringer og behovet for effektive digitale løsninger. CRO’er adopterer i stigende grad disse platforme for at levere skalerbare tjenester til flere sponsorer. Bioteknologiske firmaer udnytter eCOA- og eSource-løsninger til at forbedre patientcentrerede forsøg og forbedre datanøjagtighed. Markedets vækst er i tråd med udvidede kliniske forskningsaktiviteter på tværs af disse slutbrugere.
Segmenteringer:
Efter Løsningstype
- Elektronisk Klinisk Resultatvurdering (eCOA)
- Elektronisk Kilde (eSource)
- Integrerede Kliniske Forsøgsplatforme
Efter Implementering
Efter Slutanvendelse
- Medicinalvirksomheder
- Bioteknologiske Firmaer
- Kontraktforskningsorganisationer (CRO’er)
Region
- Nordamerika
- Europa
- Tyskland
- Frankrig
- Storbritannien
- Italien
- Spanien
- Resten af Europa
- Asien og Stillehavsområdet
- Kina
- Japan
- Indien
- Sydkorea
- Sydøstasien
- Resten af Asien og Stillehavsområdet
- Latinamerika
- Brasilien
- Argentina
- Resten af Latinamerika
- Mellemøsten & Afrika
- GCC-lande
- Sydafrika
- Resten af Mellemøsten og Afrika
Regional Analyse:
Nordamerika Leder Adoptering på Grund af Avanceret Farmaceutisk Infrastruktur
Nordamerika står for 42% af det globale eCOA, eSource og Kliniske Forsøgsmarked, hvilket afspejler dets lederskab inden for klinisk forskning og digitale forsøgs teknologier. Regionen opretholder en stærk tilstedeværelse af store farmaceutiske virksomheder og teknologileverandører. Den drager fordel af veletableret forskningsinfrastruktur og regulatoriske rammer, der fremmer elektroniske kliniske resultatvurderinger. Det muliggør effektiv datafangst, lagring og rapportering på tværs af flere forsøgssteder. Høje investeringer i klinisk forskning og tidlig vedtagelse af innovative forsøgsplatforme styrker dens markedsposition. Sponsorer stoler på disse løsninger for at sikre overholdelse, forbedre patientengagement og øge operationel effektivitet.
Europa Driver Vækst Gennem Regulatorisk Støtte og Teknologiintegration
Europa udgør 28% af det globale eCOA, eSource og Kliniske Forsøgsmarked, understøttet af harmoniserede regulatoriske standarder og stigende vedtagelse af digitale kliniske løsninger. Regionen letter grænseoverskridende samarbejde for multinationale studier og fremmer standardiserede elektroniske platforme. Det tillader sponsorer at integrere fjernovervågning af patienter, realtidsrapportering og centraliseret datastyring. Investeringer i patientcentrerede og decentraliserede forsøg forbedrer yderligere operationel effektivitet. Det styrker forsøgs kvalitet, fremskynder studietidslinjer og understøtter forskellige terapeutiske områder på tværs af kontinentet.
Asien og Stillehavsområdet Fremstår som den Hurtigst Voksende Region med Udvidet Klinisk Forskning
Asien og Stillehavsområdet repræsenterer 20% af det globale eCOA, eSource og Kliniske Forsøgsmarked og viser den højeste vækstrate blandt alle regioner. Hurtig ekspansion af klinisk forskning, outsourcing af forsøg og stigende farmaceutisk produktion driver vedtagelsen. Det giver adgang til store og forskellige patientpopulationer, hvilket muliggør omkostningseffektiv forsøgsudførelse. Digitale platforme understøtter realtidsdataindsamling, fjernovervågning og strømlinet rapportering. Regeringsinitiativer, der fremmer teknologiadoption og datasikkerhed, styrker markedsudviklingen. Regionen tilbyder betydelige muligheder for langsigtet vækst og innovation i kliniske forsøg.
Shape Your Report to Specific Countries or Regions & Enjoy 30% Off!
Nøglespilleranalyse:
- Medidata Solutions, Inc.
- Oracle Corporation
- Veeva Systems Inc.
- Parexel International Corporation
- CRF Health (nu en del af Medidata)
- BioClinica, Inc.
- ERT (eResearchTechnology)
- ICON plc
- IQVIA Holdings, Inc.
- Signant Health
- YPrime, LLC
- ClinOne
Konkurrenceanalyse:
Markedet for eCOA, eSource og kliniske forsøg er meget konkurrencepræget, drevet af tilstedeværelsen af etablerede teknologileverandører og kontraktforskningsorganisationer, der tilbyder avancerede digitale løsninger. Nøglespillere fokuserer på produktinnovation, strategiske partnerskaber og geografisk ekspansion for at styrke markedspositionerne. Der lægges vægt på integration af cloud-baserede platforme, AI-drevne analyser og patientcentrerede værktøjer for at differentiere tilbuddene. Virksomheder investerer i skalerbare løsninger, der understøtter decentraliserede forsøg, realtidsdatafangst og overholdelse af lovgivning. Konkurrencestrategier inkluderer opkøb, samarbejder med farmaceutiske sponsorer og forbedring af serviceporteføljer for at tilbyde end-to-end forsøgsstyring. Markedsledere prioriterer kundesupport og træning for at sikre problemfri adoption af deres platforme. Mindre virksomheder udnytter nicheløsninger eller specialiserede tjenester til at fange målrettede markedssegmenter. Overordnet set opmuntrer konkurrencen til kontinuerlig innovation, forbedret operationel effektivitet og forbedret forsøgs kvalitet på tværs af det globale marked.
Seneste udviklinger:
- I oktober 2025 udvidede Medidata Solutions, Inc. sit partnerskab med Sanofi for at uddybe samarbejdet om AI-aktiveret klinisk udvikling.
- I marts 2025 indgik ICON plc et partnerskab med Mural Health Technologies, Inc. for at forbedre oplevelsen for deltagere og steder i kliniske forsøg ved at bruge Mural Link’s platform til betalinger, rejsekoordinering og kommunikation, hvilket letter patientcentreret forsøgsstyring og reducerer deltagelsesbarrierer.
Rapportdækning:
Forskningsrapporten tilbyder en dybdegående analyse baseret på Løsningstype, Implementering, Slutanvendelse og Region. Den beskriver førende markedsaktører og giver et overblik over deres forretning, produkttilbud, investeringer, indtægtsstrømme og nøgleapplikationer. Derudover inkluderer rapporten indsigt i det konkurrenceprægede miljø, SWOT-analyse, aktuelle markedstendenser samt de primære drivkræfter og begrænsninger. Endvidere diskuterer den forskellige faktorer, der har drevet markedsudvidelse i de seneste år. Rapporten udforsker også markedsdynamikker, regulatoriske scenarier og teknologiske fremskridt, der former industrien. Den vurderer virkningen af eksterne faktorer og økonomiske ændringer i ITALIEN på markedsvækst. Endelig giver den strategiske anbefalinger til nye aktører og etablerede virksomheder for at navigere i markedets kompleksitet.
Fremtidsperspektiv:
- Øget anvendelse af decentraliserede og patientcentrerede kliniske forsøg vil udvide markedsvæksten.
- Integration af kunstig intelligens og avanceret analyse vil forbedre datadrevet beslutningstagning.
- Cloud-baserede platforme vil dominere implementeringen på grund af skalerbarhed, fleksibilitet og fjernadgang.
- Udvidelse til nye markeder, især i Asien-Stillehavsområdet, vil skabe nye vækstmuligheder.
- Regulatorisk støtte til elektroniske kliniske resultatvurderinger vil fremskynde adoptionen af digitale løsninger.
- Øget fokus på realtidsmonitorering og dataintegritet vil drive investering i eCOA- og eSource-løsninger.
- Samarbejde mellem teknologileverandører og medicinalvirksomheder vil forbedre forsøgets effektivitet.
- Stigende efterspørgsel efter bærbare enheder og mobile sundhedsapplikationer vil styrke digitale forsøgsfunktioner.
- Udvikling af integrerede platforme, der tilbyder end-to-end forsøgsstyring, vil få momentum.
- Kontinuerlig innovation inden for automatisering, rapportering og overholdelsesværktøjer vil opretholde langsigtet markedsudvidelse.




