Visión General del Mercado
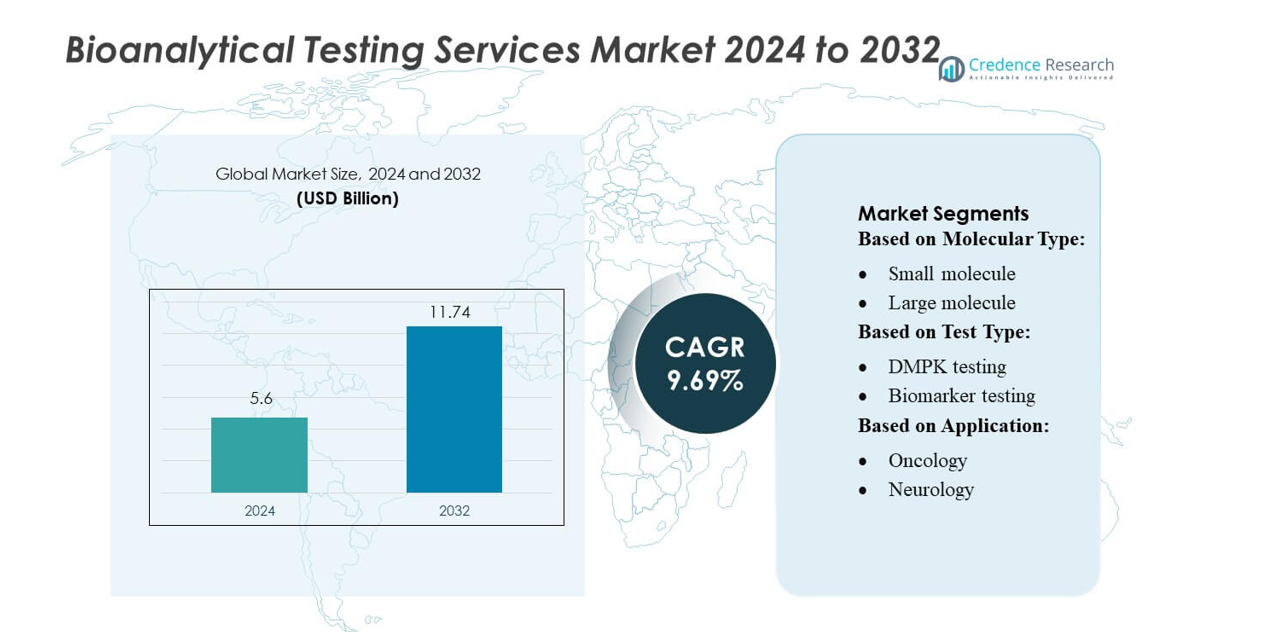
El tamaño del mercado de Servicios de Pruebas Bioanalíticas fue valorado en 5.6 mil millones de USD en 2024 y se anticipa que alcanzará los 11.74 mil millones de USD para 2032, con un CAGR del 9.69% durante el período de pronóstico.
| ATRIBUTO DEL INFORME |
DETALLES |
| Período Histórico |
2020-2023 |
| Año Base |
2024 |
| Período de Pronóstico |
2025-2032 |
| Tamaño del Mercado de Servicios de Pruebas Bioanalíticas 2024 |
5.6 mil millones de USD |
| Mercado de Servicios de Pruebas Bioanalíticas, CAGR |
9.69% |
| Tamaño del Mercado de Servicios de Pruebas Bioanalíticas 2032 |
11.74 mil millones de USD |
El mercado de Servicios de Pruebas Bioanalíticas está conformado por organizaciones de investigación por contrato especializadas y laboratorios globales que ofrecen soluciones avanzadas de pruebas de farmacocinética, inmunogenicidad, biomarcadores y virología. Los principales proveedores incluyen empresas de servicios científicos bien establecidas, reconocidas por su infraestructura conforme a GLP/GCP, plataformas LC-MS/MS de alta sensibilidad y flujos de trabajo de laboratorio impulsados por la automatización que apoyan grandes líneas de investigación clínica en programas de biológicos y moléculas pequeñas. Estos actores compiten ampliando las capacidades de desarrollo de ensayos, mejorando los sistemas de integridad de datos y fortaleciendo las redes de entrega globales. América del Norte lidera el mercado con más del 40% de participación de mercado, respaldada por una fuerte actividad de I+D biofarmacéutica, extensos ensayos clínicos y alta adopción de servicios analíticos externalizados.
Perspectivas del Mercado
- El mercado de Servicios de Pruebas Bioanalíticas alcanzó los 5.6 mil millones de USD en 2024 y crecerá hasta los 11.74 mil millones de USD para 2032 a un CAGR del 9.69%, impulsado por el creciente desarrollo de biológicos y la creciente adopción de soporte analítico externalizado.
- La fuerte demanda de pruebas de farmacocinética, inmunogenicidad, biomarcadores y virología continúa acelerando la expansión del mercado, respaldada por un alto volumen de ensayos clínicos en oncología, enfermedades infecciosas y neurología.
- La actividad competitiva se intensifica a medida que las CRO globales mejoran las instalaciones conformes a GLP/GCP, integran plataformas LC-MS/MS de alta sensibilidad y adoptan la automatización para mejorar la eficiencia, la integridad de los datos y los tiempos de respuesta.
- El mercado enfrenta restricciones vinculadas a los complejos requisitos de validación de ensayos, las expectativas regulatorias en evolución y la disponibilidad limitada de talento especializado para flujos de trabajo analíticos de grandes moléculas y basados en células.
- América del Norte lidera con más del 40% de participación, seguida por Europa con aproximadamente el 28%, mientras que las pequeñas moléculas siguen siendo el segmento dominante con más del 55% de participación, respaldado por extensas líneas de genéricos y una fuerte demanda de pruebas de bioequivalencia.
Access crucial information at unmatched prices!
Request your sample report today & start making informed decisions powered by Credence Research Inc.!
Download Sample
Análisis de Segmentación del Mercado:
Por Tipo de Molécula
Las pequeñas moléculas ocupan la posición dominante en el mercado de servicios de pruebas bioanalíticas, representando más del 55% del total debido a su uso extensivo en genéricos, nuevos tratamientos y formulaciones complejas combinadas. Sus vías analíticas bien establecidas, ciclos de desarrollo más cortos y alta demanda de estudios farmacocinéticos y de bioequivalencia continúan fortaleciendo su liderazgo. Las grandes moléculas muestran un crecimiento constante a medida que los biológicos, las terapias celulares y las proteínas recombinantes se expanden en las líneas clínicas. Esta categoría se beneficia de las crecientes inversiones en ingeniería de anticuerpos y la creciente necesidad de ensayos sensibles para validar la seguridad y el rendimiento terapéutico.
- Por ejemplo, la plataforma propietaria de Qualitest liderada por IA, Qualisense, apoya la validación rápida de sistemas de software complejos y se informó que acelera el tiempo de lanzamiento en aproximadamente 6× en proyectos relevantes.
Por Tipo de Prueba
Las pruebas DMPK emergen como la categoría de prueba líder, capturando alrededor del 30% del mercado, respaldadas por el aumento de los requisitos para el perfil de absorción, distribución, metabolismo y excreción (ADME) a lo largo del desarrollo temprano de medicamentos. El segmento se beneficia de la creciente complejidad de los candidatos terapéuticos y la necesidad de predecir el comportamiento in-vivo con mayor precisión. Las pruebas de biomarcadores y de inmunogenicidad siguen debido a la fuerte adopción en la medicina de precisión y el desarrollo de biológicos. Las pruebas de virología, incluidas in-vivo e in-vitro, continúan expandiéndose con la creciente investigación de enfermedades infecciosas, el desarrollo de vacunas y el enfoque regulatorio en la evaluación de seguridad viral en la fabricación biofarmacéutica.
- Por ejemplo, Accenture trabajó con una firma biofarmacéutica global para implementar su marco Digital Thread for Life Sciences: esto redujo el ciclo de transferencia de tecnología en la fabricación de 12 semanas a 7–8 semanas.
Por Aplicación
La oncología sigue siendo el área de aplicación dominante, contribuyendo con más del 40% del mercado, ya que los tratamientos contra el cáncer dependen cada vez más de la validación bioanalítica para terapias dirigidas, inmunoterapias y desarrollo de medicamentos impulsados por biomarcadores. Las extensas líneas de oncología, la alta actividad de ensayos clínicos y la demanda de diagnósticos complementarios refuerzan este liderazgo. Las enfermedades infecciosas forman el siguiente segmento importante debido al desarrollo continuo de antivirales, vacunas y biológicos. Las aplicaciones en neurología, cardiología y gastroenterología continúan ganando impulso a medida que las enfermedades complejas requieren ensayos especializados para caracterizar la eficacia terapéutica, los perfiles de seguridad y las respuestas a tratamientos a largo plazo.
Principales Impulsores del Crecimiento
Expansión de las Líneas de Biológicos y Terapias Avanzadas
El mercado de servicios de pruebas bioanalíticas crece fuertemente a medida que las empresas biofarmacéuticas aceleran las inversiones en anticuerpos monoclonales, terapias génicas, tratamientos basados en células y proteínas recombinantes. Estas modalidades complejas requieren ensayos altamente sensibles para farmacocinética, inmunogenicidad y cuantificación de biomarcadores, impulsando la subcontratación a laboratorios especializados con plataformas avanzadas como LC-MS/MS y tecnologías de unión de ligandos. El aumento del escrutinio regulatorio sobre la seguridad de los biológicos, el incremento de las presentaciones globales y la expansión de los ensayos clínicos fortalecen la demanda de métodos analíticos validados, asegurando una caracterización precisa del rendimiento terapéutico a lo largo de las fases de desarrollo.
- Por ejemplo, las iniciativas de IA generativa de IBM Consulting en ciencias de la vida aprovechan la experiencia y tecnología de su brazo consultor. La empresa ha desarrollado flujos de trabajo automatizados por IA para procesos específicos, como reducir el trabajo manual en la generación de narrativas de eventos adversos en aproximadamente un 50%.
Aumento del Volumen de Ensayos Clínicos y el Impulso de la Externalización
La creciente actividad de ensayos clínicos en oncología, enfermedades infecciosas, neurología y trastornos raros impulsa una demanda significativa de apoyo integral en pruebas bioanalíticas. Las empresas farmacéuticas externalizan cada vez más estas funciones a CROs para reducir los costos internos de laboratorio, acelerar los plazos y acceder a instrumentación especializada. La externalización también mejora la escalabilidad para estudios multicéntricos globales que requieren procesamiento de grandes muestras y protocolos de ensayo armonizados. El cambio hacia estructuras internas de I+D más ágiles y una mayor dependencia de la experiencia externa acelera la adopción de soluciones bioanalíticas de extremo a extremo, fortaleciendo el crecimiento del mercado en las etapas preclínicas y clínicas.
- Por ejemplo, el informe de la Plataforma de IA y Soluciones de Software para Ciencias de la Vida de DXC indica que su suite de automatización regulatoria ha apoyado más de 76,000 presentaciones regulatorias y abarca 250,000 usuarios globales en flujos de trabajo farmacéuticos.
Mayor Énfasis Regulatorio en la Validación Analítica Estandarizada
Las autoridades regulatorias exigen una validación analítica rigurosa para garantizar la seguridad terapéutica, la reproducibilidad y la relevancia clínica, reforzando la importancia de marcos de pruebas bioanalíticas robustos. Agencias como la FDA y la EMA continúan actualizando la guía para ensayos de unión de ligandos, biomarcadores y metodologías PK/PD, impulsando a las empresas a adoptar entornos de alta conformidad y flujos de trabajo estandarizados. El creciente enfoque en las vías de aprobación de biosimilares, la detección de impurezas traza y las evaluaciones de seguridad viral también amplía la demanda de capacidades de prueba especializadas. Estos requisitos cada vez más estrictos alientan a los desarrolladores farmacéuticos a confiar en proveedores de servicios expertos con infraestructura establecida conforme a GLP.
Tendencias y Oportunidades Clave
Adopción de Plataformas de Alta Sensibilidad y Automatización
El mercado observa una rápida integración de tecnologías analíticas de alta sensibilidad, incluyendo LC-MS/MS de próxima generación, inmunoensayos multiplex y sistemas automatizados de preparación de muestras. La automatización reduce el error humano, mejora la precisión y acelera los tiempos de respuesta para grandes cohortes de ensayos clínicos. El creciente uso de detección de ultra alta sensibilidad apoya biológicos complejos, biomarcadores de baja concentración y diseños clínicos basados en micro-muestreo. Los proveedores que adoptan robótica, gestión digital de datos y sistemas integrados de información de laboratorio (LIMS) obtienen una ventaja competitiva a medida que los clientes priorizan la fiabilidad, la escalabilidad y los flujos de trabajo listos para la regulación.
- Por ejemplo, la plataforma Atos Polaris AI, que ofrece agentes de IA autónomos preconstruidos que pueden reducir el esfuerzo de desarrollo en un 40-50 %, el tiempo de espera de control de calidad en un 50-60 % y el ciclo de revisión de contratos en un 30-40 %.
Aumento de la Demanda de Estudios Centrándose en Biomarcadores y Medicina de Precisión
El desarrollo clínico impulsado por biomarcadores crea grandes oportunidades, particularmente en oncología, neurología e inmunología. Las compañías farmacéuticas requieren cada vez más paneles multi-análisis, marcadores genómicos y perfiles longitudinales de biomarcadores para apoyar la estratificación de pacientes y el monitoreo de la respuesta terapéutica. Esta tendencia acelera el crecimiento en servicios de desarrollo y validación de ensayos a medida. El cambio hacia la medicina de precisión fortalece las colaboraciones entre las CROs y las compañías biofarmacéuticas para crear plataformas especializadas de biomarcadores capaces de apoyar la detección temprana, estudios de mecanismo de acción y diseños de ensayos adaptativos, mejorando el valor científico y comercial.
- Por ejemplo, Charles River Laboratories amplió sus capacidades de descubrimiento de biomarcadores a través de la adquisición de SAMDI Tech, permitiendo flujos de trabajo de espectrometría de masas de alta capacidad y sin etiquetas capaces de examinar más de 100,000 compuestos por día utilizando su plataforma patentada SAMDI® MS.
Expansión de Capacidades de Desarrollo de Virología y Vacunas
El creciente enfoque global en terapias antivirales, preparación para pandemias e I+D de vacunas impulsa la expansión continua de las capacidades de pruebas de virología. Los ensayos virales in vitro, la cuantificación de carga viral, los estudios de neutralización y las pruebas serológicas ganan mayor demanda en las líneas de desarrollo biofarmacéuticas. Las oportunidades crecen para proveedores que ofrecen instalaciones de alto nivel de bioseguridad, análisis virales automatizados y experiencia en desarrollo rápido de ensayos. La necesidad de validación de eliminación viral en la fabricación de biológicos fortalece aún más la demanda, posicionando a la virología como uno de los segmentos de más rápida evolución dentro de la subcontratación bioanalítica.
Desafíos Clave
Alta Complejidad de Ensayos de Moléculas Grandes y Basados en Células
Las pruebas bioanalíticas para moléculas grandes, terapias celulares y tratamientos basados en genes presentan desafíos metodológicos significativos debido a la complejidad estructural, problemas de estabilidad e interferencia de matriz. Desarrollar ensayos sensibles para inmunogenicidad, bioactividad y caracterización de vectores virales requiere habilidades especializadas, plataformas avanzadas y extensos tiempos de validación. La variabilidad en la expresión de biomarcadores entre poblaciones de pacientes complica aún más la estandarización de ensayos. Estas limitaciones técnicas aumentan los costos de desarrollo y prolongan los tiempos clínicos, limitando la capacidad de algunas organizaciones para cumplir con los objetivos regulatorios y de comercialización acelerados.
Carga de Cumplimiento Estricto y Expectativas Regulatorias en Evolución
Los proveedores de servicios enfrentan desafíos para mantener el cumplimiento GLP/GCP a medida que los organismos reguladores introducen actualizaciones continuas relacionadas con la validación de ensayos, la calificación de biomarcadores y la integridad de los datos bioanalíticos. Cumplir con estos requisitos demanda una inversión significativa en documentación, capacitación, calibración de instrumentos y preparación para auditorías. Los estudios globales agregan complejidad debido a las diferentes expectativas regulatorias regionales para el manejo de muestras, formatos de informes y criterios de aceptación. Estas crecientes obligaciones de cumplimiento tensionan a los laboratorios más pequeños y aumentan los costos operativos, creando barreras para una rápida expansión y diferenciación competitiva.
Análisis Regional
Norteamérica
Norteamérica lidera el mercado de servicios de pruebas bioanalíticas con más del 40% de la cuota de mercado, impulsada por un ecosistema biofarmacéutico maduro, una actividad avanzada de ensayos clínicos y un fuerte énfasis regulatorio en procesos analíticos validados. La región se beneficia de extensas inversiones en biológicos, biosimilares y terapias génicas, que requieren pruebas de farmacocinética, inmunogenicidad y biomarcadores de alta precisión. Las principales CROs y laboratorios especializados mantienen grandes instalaciones compatibles con GLP e integran plataformas LC-MS/MS de alta sensibilidad, flujos de trabajo automatizados y sistemas de datos digitales. Las directrices de apoyo de la FDA, la creciente preferencia por la externalización y una sólida cartera de ensayos de oncología y enfermedades raras continúan reforzando el liderazgo regional.
Europa
Europa posee alrededor del 28% de la cuota de mercado, respaldada por fuertes clústeres de I+D farmacéutica en Alemania, el Reino Unido, Francia y Suiza. La región se beneficia de la creciente adopción de biológicos, productos terapéuticos avanzados y programas complejos de biosimilares que requieren una extensa validación analítica y estudios de estabilidad a largo plazo. La evolución de las guías de la EMA sobre biomarcadores e inmunogenicidad refuerza la necesidad de flujos de trabajo estandarizados y soporte bioanalítico de alta calidad. El crecimiento se ve impulsado además por la expansión de ensayos clínicos en oncología, neurología y enfermedades infecciosas. El aumento de la colaboración entre CROs y centros de investigación académica acelera el desarrollo de capacidades de prueba de próxima generación en todo el mercado europeo.
Asia-Pacífico
Asia-Pacífico representa casi el 22% de la cuota de mercado y es la región de más rápido crecimiento debido a la expansión de la fabricación farmacéutica, el aumento de la producción de biológicos y la creciente actividad de ensayos clínicos multinacionales. China, India, Corea del Sur y Japón invierten fuertemente en infraestructura bioanalítica, incluidos sistemas LC-MS/MS de alto rendimiento, plataformas de inmunoensayo e instalaciones de pruebas de virología. La externalización rentable, la rápida modernización regulatoria y el creciente desarrollo de biotecnología local fortalecen la posición competitiva de la región. El aumento de la inversión de CROs globales y las asociaciones con innovadores regionales mejoran la capacidad de servicio, particularmente en programas de desarrollo de oncología, enfermedades infecciosas y biosimilares, impulsando una aceleración sostenida del mercado.
América Latina
América Latina contribuye con aproximadamente el 6% de la cuota de mercado, respaldada por el aumento de la externalización farmacéutica y la expansión de redes de ensayos clínicos en Brasil, México y Argentina. La región experimenta una creciente demanda de pruebas bioanalíticas en enfermedades infecciosas, oncología y trastornos metabólicos, impulsada por la creciente innovación terapéutica y los requisitos de salud pública. Los proveedores mejoran las capacidades de servicio adoptando inmunoensayos validados, paneles de biomarcadores y marcos de pruebas farmacocinéticas. Los esfuerzos de armonización regulatoria y las colaboraciones con CROs globales mejoran los estándares de cumplimiento y la calidad científica. A pesar de las limitaciones de infraestructura, la expansión de la actividad biotecnológica local y el interés de patrocinadores multinacionales impulsan la adopción constante de servicios de pruebas especializadas.
Oriente Medio & África
La región de Oriente Medio & África posee alrededor del 4% de la cuota de mercado, reflejando un mercado en desarrollo pero en constante expansión, respaldado por inversiones en la modernización de la atención médica y capacidades de investigación clínica. Países como los EAU, Arabia Saudita y Sudáfrica fomentan el crecimiento a través de la mejora de la infraestructura de laboratorios, el aumento de la participación en ensayos clínicos y la creciente disponibilidad de servicios analíticos conformes con BPL. La demanda de pruebas bioanalíticas está impulsada por la expansión de la investigación de enfermedades infecciosas y el creciente interés en biológicos y vacunas. Aunque la capacidad sigue siendo limitada en comparación con las principales regiones, las asociaciones internacionales y las iniciativas de I+D respaldadas por el gobierno apoyan el avance gradual del mercado.
Segmentaciones del Mercado:
Por Tipo Molecular:
- Molécula pequeña
- Molécula grande
Por Tipo de Prueba:
- Pruebas DMPK
- Pruebas de biomarcadores
Por Aplicación:
Por Geografía
- América del Norte
- Europa
- Alemania
- Francia
- Reino Unido
- Italia
- España
- Resto de Europa
- Asia Pacífico
- China
- Japón
- India
- Corea del Sur
- Sudeste Asiático
- Resto de Asia Pacífico
- América Latina
- Brasil
- Argentina
- Resto de América Latina
- Oriente Medio & África
- Países del CCG
- Sudáfrica
- Resto de Oriente Medio y África
Panorama Competitivo
El mercado de servicios de pruebas bioanalíticas presenta un panorama competitivo conformado por líderes globales en tecnología y consultoría como Infosys Limited, Capgemini, Qualitest Group, Accenture, Deloitte Touche Tohmatsu Limited, DeviQA Solutions, IBM Corporation, DXC Technology Company, TATA Consultancy Services Limited y Atos SE. El mercado de servicios de pruebas bioanalíticas se define por un creciente enfoque en la precisión científica, el cumplimiento normativo y la transformación digital en las operaciones de laboratorio. Los principales proveedores de servicios se diferencian al expandir plataformas analíticas de alta sensibilidad, fortalecer la infraestructura GLP/GCP e integrar la automatización para apoyar los flujos de trabajo de ensayos clínicos a gran escala. El mercado continúa desplazándose hacia capacidades especializadas en farmacocinética, inmunogenicidad, cuantificación de biomarcadores y pruebas de virología, impulsado por la creciente complejidad de los biológicos y las terapias avanzadas. Las empresas invierten fuertemente en sistemas de integridad de datos, digitalización de flujos de trabajo y herramientas analíticas habilitadas por IA para mejorar la precisión, acelerar los tiempos de respuesta y apoyar las presentaciones multirregionales. Las asociaciones entre CROs, innovadores biofarmacéuticos y proveedores de tecnología mejoran aún más la escalabilidad operativa y la entrega de servicios globales.
Shape Your Report to Specific Countries or Regions & Enjoy 30% Off!
Análisis de Jugadores Clave
- Infosys Limited
- Capgemini
- Qualitest Group
- Accenture
- Deloitte Touche Tohmatsu Limited
- DeviQA Solutions
- IBM Corporation
- DXC Technology Company
- TATA Consultancy Services Limited
- Atos SE
Desarrollos Recientes
- En junio de 2024, SGS SA anunció la incorporación de nuevos estudios de estabilidad, incluyendo instalaciones de almacenamiento de muestras, a sus servicios biofarmacéuticos en su laboratorio de Birsfelden en Suiza. Esta expansión amplió la cartera de servicios de la empresa y mejoró su alcance al cliente en el mercado suizo, proporcionando servicios críticos para productos biofarmacéuticos.
- En enero de 2024, Frontage Laboratories completó la adquisición de los negocios de Bioanálisis y Metabolismo de Fármacos & Farmacocinética (DMPK) de Accelera S.r.l. Este movimiento estratégico se llevó a cabo a través de la subsidiaria de propiedad total de Frontage, Frontage Europe S.r.l., lo que expandió la presencia de mercado de la empresa.
- En enero de 2024, Capgemini SE y Orange introdujeron sus servicios de “nube confiable”. Esta plataforma tiene como objetivo proporcionar las necesidades específicas de la nube del Estado francés, agencias públicas, hospitales, autoridades regionales, Operadores de Importancia Vital (OIV) y Operadores de Servicios Esenciales (OSE), permitiéndoles utilizar los servicios de Microsoft 365 y Microsoft Azure dentro de un entorno soberano y altamente seguro.
Cobertura del Informe
El informe de investigación ofrece un análisis profundo basado en Tipo Molecular, Tipo de Prueba, Aplicación y Geografía. Detalla a los principales actores del mercado, proporcionando una visión general de su negocio, ofertas de productos, inversiones, fuentes de ingresos y aplicaciones clave. Además, el informe incluye información sobre el entorno competitivo, análisis FODA, tendencias actuales del mercado, así como los principales impulsores y restricciones. Además, discute varios factores que han impulsado la expansión del mercado en los últimos años. El informe también explora la dinámica del mercado, escenarios regulatorios y avances tecnológicos que están moldeando la industria. Evalúa el impacto de factores externos y cambios económicos globales en el crecimiento del mercado. Por último, proporciona recomendaciones estratégicas para nuevos entrantes y empresas establecidas para navegar por las complejidades del mercado.
Perspectivas Futuras
- El mercado se expandirá de manera constante a medida que los biológicos, las terapias celulares y las terapias génicas aumenten en los pipelines de desarrollo global.
- La demanda de ensayos de alta sensibilidad aumentará con el creciente énfasis en la medicina de precisión y los diseños clínicos impulsados por biomarcadores.
- La automatización y los sistemas de laboratorio digitales se volverán centrales para mejorar la integridad de los datos, la eficiencia y la preparación regulatoria.
- Las plataformas avanzadas de LC-MS/MS y los inmunoensayos multiplex ganarán una adopción más amplia en flujos de trabajo analíticos complejos.
- La capacidad de pruebas de virología y serología se expandirá a medida que el desarrollo de vacunas y la investigación antiviral continúen fortaleciéndose.
- Las colaboraciones globales de CRO se intensificarán para apoyar ensayos multicéntricos y la validación armonizada de ensayos.
- El impulso de la subcontratación se acelerará a medida que las empresas biofarmacéuticas optimicen las estructuras internas de I+D.
- El análisis de datos, las herramientas de IA y los modelos de interpretación impulsados por aprendizaje automático mejorarán la toma de decisiones en estudios de PK/PD.
- Las expectativas regulatorias para la validación estandarizada de ensayos darán forma a los marcos de calidad y a las prioridades de inversión.
- Los mercados emergentes fortalecerán su posición como centros bioanalíticos regionales con infraestructura mejorada y capacidades especializadas.




