Aperçu du marché de la fermentation biopharmaceutique :
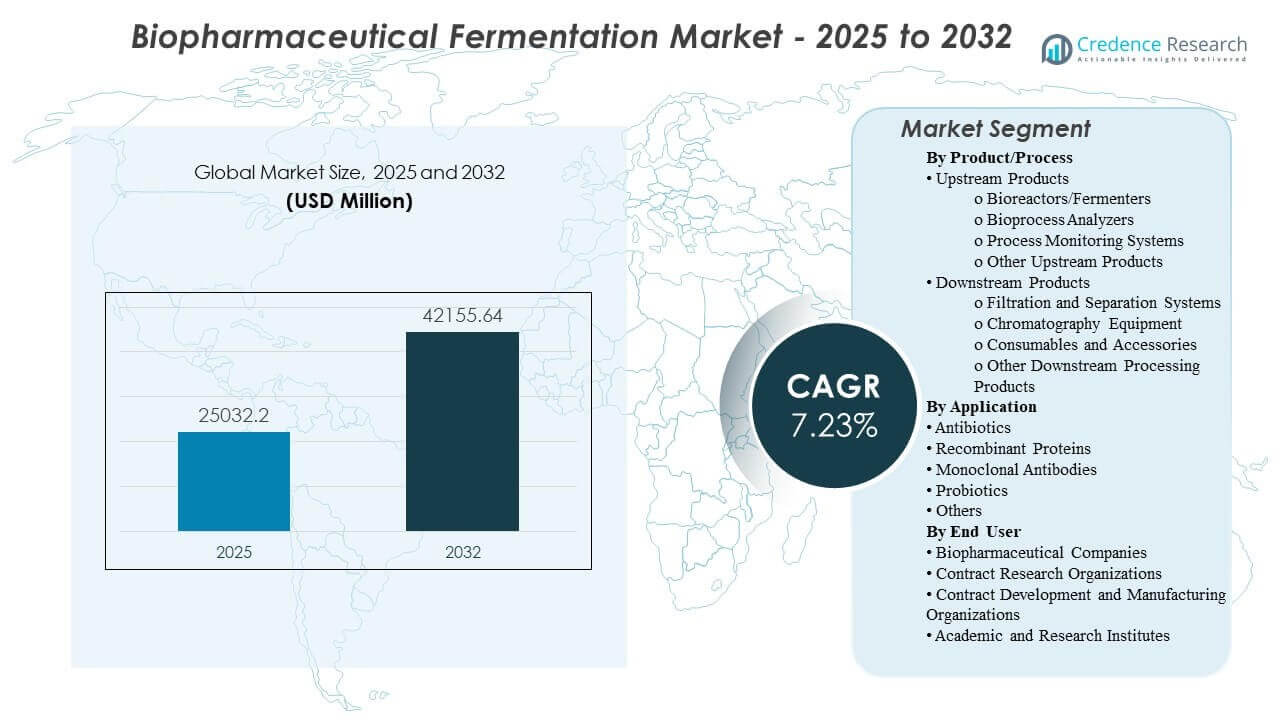
La taille du marché mondial de la fermentation biopharmaceutique était estimée à 25 032,2 millions USD en 2025 et devrait atteindre 42 155,64 millions USD d’ici 2032, avec un TCAC de 7,73 % de 2025 à 2032. La demande est principalement stimulée par l’augmentation des pipelines de produits biologiques nécessitant des rendements plus élevés et plus reproductibles ainsi qu’un contrôle de processus plus strict, de la phase de développement à la fabrication commerciale. Les extensions de capacité et la standardisation des processus dans les principaux pôles biopharmaceutiques continuent de renforcer les dépenses en systèmes de fermentation, en outils de surveillance et de purification.
| ATTRIBUT DU RAPPORT |
DÉTAILS |
| Période Historique |
2020-2024 |
| Année de Base |
2025 |
| Période de Prévision |
2026-2032 |
| Taille du Marché de la Fermentation Biopharmaceutique 2025 |
25 032,2 millions USD |
| Marché de la Fermentation Biopharmaceutique, TCAC |
7,73% |
| Taille du Marché de la Fermentation Biopharmaceutique 2032 |
42 155,64 millions USD |
Tendances et Perspectives Clés du Marché
- Le marché devrait passer de 25 032,2 millions USD (2025) à 42 155,64 millions USD (2032) avec un TCAC de 7,73 % (2025–2032).
- L’Amérique du Nord représentait 43,6 % en 2025, reflétant sa concentration de fabrication commerciale de produits biologiques et de capacité de développement de processus.
- L’Europe détenait une part de 27,4 % en 2025, soutenue par une forte innovation en bioprocédés et des réseaux de production de produits biologiques établis.
- L’Asie-Pacifique a atteint une part de 17,8 % en 2025, soutenue par des ajouts de capacité et des programmes de fabrication localisés sur des marchés clés.
- Les produits en aval ont dominé avec une part de 46,4 % (2025), montrant que la purification et la séparation sont les plus grandes zones de dépense dans le flux de travail de fermentation.
Analyse des Segments
L’achat de fermentation biopharmaceutique est influencé par la performance dans des conditions réelles d’exploitation, en particulier la répétabilité des rendements, le contrôle de la contamination et la capacité à évoluer sans dérive de processus. Les acheteurs privilégient de plus en plus la préparation à la validation, la profondeur de la documentation et la réactivité du service car les étapes de fermentation doivent s’intégrer étroitement avec les systèmes de purification et de qualité en aval. Les décisions de coût total de possession tendent à considérer l’utilisation des consommables, le temps de changement et la probabilité de succès des lots en plus du prix de l’équipement.
Le flux de travail continue de se polariser entre l’exécution en amont évolutive et la gestion des goulots d’étranglement en aval, car les produits biologiques à plus forte valeur ajoutée augmentent la complexité de la purification et les contraintes de débit. Les plateformes standardisées et les modèles opérationnels harmonisés à travers les sites soutiennent une production répétable et un transfert technologique plus rapide. En conséquence, la demande est renforcée pour des chaînes d’outils intégrées couvrant les bioréacteurs, l’analytique, la surveillance des processus, la filtration, la chromatographie et les consommables associés.
Access crucial information at unmatched prices!
Request your sample report today & start making informed decisions powered by Credence Research Inc.!
Download Sample
Par Aperçu Produit/Processus
Les produits en aval représentaient la plus grande part de 46,4% en 2025. Ce leadership reflète comment les étapes de purification, de séparation et de polissage déterminent souvent le débit de bout en bout et la performance de la qualité des produits biologiques. Les acheteurs privilégient des performances robustes de filtration et de chromatographie pour gérer les impuretés et garantir des attributs de qualité critiques constants à grande échelle. La nature récurrente de l’utilisation des consommables et des accessoires renforce également la part de revenus en aval, en particulier dans les installations multi-produits avec des changements de campagne fréquents.
Par Aperçu Application
Les protéines recombinantes représentaient la plus grande part de 43,0% en 2025. Le segment bénéficie d’une pertinence thérapeutique et industrielle large, soutenant une demande constante pour la capacité de fermentation à travers les étapes de développement et de fabrication. Les fabricants mettent l’accent sur la reproductibilité et la performance des processus évolutifs, ce qui augmente l’attrait pour les systèmes de surveillance et d’analyse qui contrôlent les paramètres critiques du processus. Les efforts d’optimisation continue pour améliorer le rendement et la qualité soutiennent davantage les mises à niveau et les cycles de remplacement en cours sur les plateformes de fermentation de base.
Par Aperçu Utilisateur Final
Les entreprises biopharmaceutiques représentaient la plus grande part de 41,6% en 2025. Les grands fabricants soutiennent une demande récurrente grâce à l’expansion de la capacité interne, aux programmes d’amélioration des processus et aux initiatives de standardisation multi-sites. Les stratégies internes favorisent généralement les plateformes validées et les systèmes de qualité des fournisseurs éprouvés pour minimiser les risques opérationnels et de conformité. Ces organisations investissent également dans des ensembles intégrés de l’amont à l’aval pour réduire le temps de cycle et améliorer les taux de réussite des lots à travers les campagnes de production de routine.
Moteurs du Marché de la Fermentation Biopharmaceutique
Augmentation de l’Échelle du Pipeline de Biologiques et Expansion de la Fabrication Commerciale
Les pipelines biopharmaceutiques continuent de s’étendre à travers plusieurs modalités, augmentant le besoin de capacité de fermentation évolutive et de performance de processus reproductible. Les fabricants investissent dans des plateformes qui soutiennent une montée en échelle robuste du développement aux volumes commerciaux avec un minimum de dérive de processus. La forte demande pour des flux de travail validés augmente l’adoption d’équipements standardisés, de solutions de surveillance et d’analyse. À mesure que les installations exécutent plus de campagnes, l’effet d’entraînement renforce la demande pour les consommables, la maintenance et les services de cycle de vie.
- Par exemple, Samsung Biologics a annoncé l’usine 5 comme une installation de fabrication de 180 000 litres dans le cadre d’une expansion du Bio Campus II de 96 000 m2, que la société a déclaré porterait sa capacité totale sur site à 784 000 litres une fois terminée, soulignant comment les acteurs de grande envergure des biologiques quantifient l’expansion de la fabrication commerciale.
Contrôle des Processus, Surveillance et Biotraitement Basé sur les Données
Les résultats de la fermentation dépendent d’un contrôle strict des paramètres critiques, ce qui entraîne une adoption accrue des analyseurs de bioprocédés et des systèmes de surveillance des processus. Les acheteurs privilégient les solutions qui améliorent la visibilité sur les moteurs de performance tels que le pH, l’oxygène dissous, les métabolites et les indicateurs de productivité. Une surveillance améliorée réduit la variabilité et soutient un dépannage plus rapide, ce qui peut améliorer la probabilité de succès des lots. La préparation à l’intégration avec les systèmes numériques de qualité et de fabrication renforce encore l’achat de piles de surveillance compatibles.
Contraintes de Débit en Aval et Complexité de Purification
Les étapes en aval définissent souvent le débit global et la qualité du produit, surtout lorsque les profils d’impuretés et les exigences de purification deviennent plus exigeants. Les investissements augmentent dans les systèmes de filtration, de séparation et de chromatographie capables de fournir des performances répétables sous pression de l’échelle et du temps. Les installations priorisent également les flux de travail de purification validés pour répondre à des spécifications de qualité strictes et à des attentes de cohérence. Les dépenses récurrentes en consommables et accessoires soutiennent un revenu stable même lorsque les cycles d’investissement fluctuent.
- Par exemple, Sartorius a rapporté que sa plateforme Sartobind Rapid A atteignait une capacité de liaison dynamique d’environ 40 g/L, maintenait des rendements de 98,0% à 99,4% sur des tailles de dispositifs de 1,2 mL, 10 mL et 70 mL, et supportait des temps de cycle moyens de 10 à 11 minutes, soulignant comment les nouvelles technologies de capture visent à la fois la rapidité et la cohérence dans la purification à haut débit.
Standardisation et Transfert Technologique à Travers des Réseaux Multi-Sites
Les grandes organisations biopharmaceutiques harmonisent de plus en plus les plateformes de processus entre les sites pour simplifier le transfert technologique et raccourcir les délais de préparation à la fabrication. La standardisation réduit le fardeau de la formation, améliore la comparabilité des résultats et soutient la planification de la capacité évolutive. Les approches de plateforme simplifient également les pratiques de validation et de documentation à travers les réseaux. Cette tendance soutient les achats consolidés et les relations à long terme avec les fournisseurs axées sur la fiabilité, la couverture de service et le support de qualification.
Défis du Marché de la Fermentation Biopharmaceutique
Les programmes de fermentation biopharmaceutique font face à des risques opérationnels liés à la contamination, à l’échec de lots et à la variabilité lorsque les processus se déplacent à travers les échelles ou les sites. Maintenir la cohérence nécessite de solides contrôles environnementaux, des stratégies de nettoyage validées et un contrôle de processus discipliné, ce qui peut augmenter le coût et la complexité. Les attentes en matière de qualification et les exigences de documentation peuvent allonger les délais d’approvisionnement et de déploiement, en particulier pour les environnements de production réglementés. La continuité de l’approvisionnement en consommables critiques peut également créer des goulets d’étranglement lorsque les installations fonctionnent à haute utilisation ou opèrent des plannings multi-produits.
- Par exemple, Thermo Fisher Scientific déclare que sa plateforme de bioréacteur à usage unique DynaDrive couvre des systèmes de 50 L, 500 L, 3 000 L et 5 000 L, avec des rapports de réduction de 10:1 à 50 L, 20:1 à 500 L, 12,5:1 à 3 000 L, et 20:1 à 5 000 L, et que la plateforme est optimisée pour les processus de culture cellulaire au-dessus de 100 millions de cellules/mL, illustrant comment les fournisseurs conçoivent la cohérence d’échelle et la réduction des risques de contamination dans le matériel de bioprocédés commerciaux.
Les contraintes de main-d’œuvre et d’exécution peuvent ralentir l’adoption de la surveillance avancée et des flux de travail intégrés, surtout lorsque les équipes doivent équilibrer les processus hérités avec les priorités de modernisation. La montée en échelle et le transfert technologique révèlent souvent des lacunes dans la comparabilité, nécessitant un temps de développement supplémentaire pour stabiliser les performances. La planification de la capacité en aval est particulièrement sensible, car les contraintes de purification peuvent retarder le débit de bout en bout même lorsque les performances en amont s’améliorent. De plus, l’intégration de nouveaux systèmes dans l’infrastructure de qualité et de fabrication peut nécessiter un contrôle des changements et une planification de validation minutieux.
Tendances et Opportunités du Marché
Les approches de biotraitement à usage unique et modulaire continuent de se développer là où des changements rapides et une réduction du risque de contamination croisée sont des priorités stratégiques. Cela soutient les opportunités à travers les écosystèmes intégrés de matériel, de gestion des fluides et de consommables qui simplifient l’exécution des campagnes. L’achat de plateformes standardisées crée également de la place pour les fournisseurs capables de fournir un soutien de bout en bout, y compris l’assistance au développement de méthodes et la documentation de validation. À mesure que de plus en plus d’installations visent la rapidité d’accès à la clinique et la flexibilité, la demande augmente pour des solutions qui raccourcissent les délais de déploiement et réduisent la charge opérationnelle.
- Par exemple, Cytiva déclare que sa plateforme à usage unique FlexFactory peut être entièrement qualifiée et prête à fonctionner 6 à 9 mois après la conception conceptuelle, ou 9 à 12 mois sur l’ensemble du calendrier du projet, peut prendre en charge jusqu’à 4 x 2000 L bioréacteurs sur un seul train de traitement en aval, et dispose de près de 200 lignes de traitement opérationnelles installées dans le monde.
L’intensification des processus et l’amélioration de la productivité restent des opportunités clés, surtout là où les fabricants visent à augmenter la production sans expansion proportionnelle de l’empreinte. L’adoption d’analyses et de contrôles plus robustes permet un contrôle plus strict, un dépannage plus rapide et une meilleure répétabilité entre les lots. Les innovations en aval qui s’attaquent aux goulots d’étranglement de la purification peuvent libérer une valeur significative en améliorant le temps de cycle de bout en bout. Les modèles axés sur les services qui accélèrent le transfert de technologie et le soutien à la montée en échelle élargissent également les opportunités avec des organisations équilibrant la capacité interne et les partenariats externes.
Perspectives Régionales
Amérique du Nord
L’Amérique du Nord représentait 43,6 % de part en 2025, soutenue par une forte concentration d’innovateurs biopharmaceutiques, une capacité de fabrication à grande échelle et des écosystèmes établis pour le développement et la validation des processus. La demande est renforcée par l’activité continue de montée en échelle des produits biologiques et les programmes d’amélioration continue qui soutiennent les dépenses récurrentes en équipements et consommables. Les acheteurs de cette région mettent souvent l’accent sur la préparation à la qualification, la couverture des services et la compatibilité d’intégration avec les systèmes de qualité et de fabrication.
Europe
L’Europe détenait 27,4 % de part en 2025, reflétant une forte capacité de production de produits biologiques et un écosystème de fournisseurs mature dans les principaux pôles pharmaceutiques. La demande régionale bénéficie de l’innovation des processus, des pratiques opérationnelles réglementaires établies et des investissements soutenus dans la modernisation de la production. Les réseaux de fabrication multi-sites et les initiatives de standardisation soutiennent également l’approvisionnement basé sur des plateformes et l’utilisation récurrente de consommables en aval.
Asie-Pacifique
L’Asie-Pacifique représentait 17,8 % de part en 2025, stimulée par l’expansion de la capacité de fabrication de produits biologiques, les programmes de localisation et l’augmentation de la production des écosystèmes régionaux biopharmaceutiques et de fabrication sous contrat. Les investissements privilégient souvent des plateformes évolutives capables de soutenir un transfert de technologie rapide et des performances cohérentes sous une utilisation croissante. La dynamique de croissance est renforcée par les efforts visant à construire des chaînes d’approvisionnement résilientes et à renforcer l’autosuffisance manufacturière régionale.
Amérique Latine
L’Amérique latine représentait une part de 6,9% en 2025, soutenue par une croissance sélective dans la fabrication pharmaceutique localisée et le développement progressif des capacités en biotechnologie. La demande est généralement concentrée dans les marchés prioritaires où les besoins du système de santé et les stratégies de production locale encouragent l’investissement. Les acheteurs se concentrent souvent sur des solutions rentables avec un support de service fiable et des performances validées pour les flux de travail principaux.
Moyen-Orient & Afrique
Le Moyen-Orient & Afrique détenait une part de 4,3% en 2025, reflétant une base installée plus petite de centres de fermentation de biotechnologie à grande échelle mais un intérêt croissant pour la localisation et les initiatives de fabrication de soins de santé. La demande est souvent axée sur des projets, liée à des programmes stratégiques et à des ajouts de capacité ciblés. Les priorités d’approvisionnement incluent généralement la fiabilité, le support de formation et des solutions qui simplifient la qualification et l’exécution opérationnelle.
Paysage concurrentiel
La concurrence est façonnée par l’étendue des portefeuilles en amont et en aval, la profondeur du support d’application, l’empreinte de service mondiale et la capacité à répondre aux attentes de qualification et de validation dans les environnements de fabrication réglementés. Les fournisseurs se différencient par des écosystèmes intégrés qui relient les équipements de fermentation, le suivi des processus et les flux de travail de purification en aval, ainsi qu’une disponibilité solide des services de cycle de vie et des consommables. Les clients évaluent également la performance des fournisseurs en matière de support de transfert technologique, de délais de livraison et de qualité de la documentation qui réduit les frictions de déploiement. Le positionnement stratégique favorise de plus en plus les fournisseurs capables de soutenir des flux de travail de bout en bout sur plusieurs sites et modalités.
Thermo Fisher Scientific Inc. est positionnée pour concurrencer grâce à une large boîte à outils bioprocédés qui soutient les clients dans leurs besoins de développement, de montée en échelle et de fabrication commerciale. Son approche met l’accent sur l’intégration à travers les équipements, les consommables de flux de travail et les services qui réduisent la complexité opérationnelle pour les programmes de fabrication axés sur la fermentation. L’échelle et la couverture de service de l’entreprise peuvent soutenir les clients mondiaux cherchant à standardiser à travers des réseaux multi-sites. La profondeur continue de l’écosystème renforce sa capacité à servir à la fois la production à haut débit et les environnements de développement de processus basés sur des plateformes.
Le rapport de recherche et de croissance de l’industrie comprend des analyses détaillées du paysage concurrentiel du marché et des informations sur les principales entreprises, y compris :
Une analyse qualitative et quantitative des entreprises a été réalisée pour aider les clients à comprendre l’environnement commercial plus large ainsi que les forces et faiblesses des principaux acteurs de l’industrie. Les données sont analysées qualitativement pour catégoriser les entreprises comme spécialisées, axées sur une catégorie, axées sur l’industrie et diversifiées ; elles sont analysées quantitativement pour catégoriser les entreprises comme dominantes, leaders, fortes, provisoires et faibles.
Shape Your Report to Specific Countries or Regions & Enjoy 30% Off!
Développements Récents
- En février 2026, Cytiva a élargi son centre de développement et de validation de processus Fast Trak à Bengaluru, en Inde, pour aider les entreprises biopharmaceutiques à raccourcir les délais de développement, réduire les risques de fabrication et augmenter la production avec plus de confiance.
- En avril 2025, Sartorius Stedim Biotech a collaboré avec Tulip pour offrir des solutions numériques pour le biotraitement à usage unique, ciblant les défis opérationnels dans les environnements de fabrication biopharmaceutique.
- En octobre 2025, Merck KGaA a annoncé l’acquisition de la plateforme technologique de chromatographie Protein A de JSR Life Sciences pour renforcer son portefeuille de biotraitement et soutenir une fabrication d’anticorps monoclonaux plus efficace et évolutive.
- En décembre 2024, Eppendorf AG a conclu une collaboration stratégique avec DataHow AG pour intégrer DataHowLab à la plateforme cloud BioNsight d’Eppendorf, améliorant la gestion des données et l’analyse pour le développement de bioprocédés.
Portée du Rapport
| Attribut du Rapport |
Détails |
| Valeur de la taille du marché en 2025 |
25 032,2 millions USD |
| Prévision des revenus en 2032 |
42 155,64 millions USD |
| Taux de croissance (CAGR) |
7,73% (2025–2032) |
| Année de base |
2025 |
| Période de prévision |
2026–2032 |
| Unités quantitatives |
millions USD |
| Segments couverts |
Par Produit/Processus : Produits en amont, Produits en aval; Par Application : Antibiotiques, Protéines Recombinantes, Anticorps Monoclonaux, Probiotiques, Autres; Par Utilisateur Final : Entreprises Biopharmaceutiques, CRO, CDMO, Instituts Académiques & de Recherche |
| Portée régionale |
Amérique du Nord, Europe, Asie-Pacifique, Amérique Latine, Moyen-Orient & Afrique |
| Principales entreprises profilées |
Thermo Fisher Scientific Inc.; Danaher Corporation; Cytiva; Sartorius Stedim Biotech; Merck KGaA; Eppendorf AG; Lonza Group AG; Agilent Technologies; F. Hoffmann-La Roche Ltd.; Becton, Dickinson and Company (BD); GEA Group |
| Nombre de pages |
320 |
Segmentation
Par Produit/Processus
- Produits en amont [Bioréacteurs/Fermenteurs, Analyseurs de Bioprocédés, Systèmes de Surveillance de Processus, Autres Produits en Amont]
- Produits en aval [Systèmes de Filtration et de Séparation, Équipements de Chromatographie, Consommables et Accessoires, Autres Produits de Traitement en Aval]
Par Application
- Antibiotiques
- Protéines Recombinantes
- Anticorps Monoclonaux
- Probiotiques
- Autres
Par Utilisateur Final
- Entreprises biopharmaceutiques
- Organisations de recherche sous contrat (CRO)
- Organisations de développement et de fabrication sous contrat (CDMO)
- Instituts académiques et de recherche
Par région
- Amérique du Nord
- États-Unis
- Canada
- Mexique
- Europe
- Allemagne
- France
- Royaume-Uni
- Italie
- Espagne
- Reste de l’Europe
- Asie-Pacifique
- Chine
- Japon
- Inde
- Corée du Sud
- Asie du Sud-Est
- Reste de l’Asie-Pacifique
- Amérique latine
- Brésil
- Argentine
- Reste de l’Amérique latine
- Moyen-Orient & Afrique
- Pays du CCG
- Afrique du Sud
- Reste du Moyen-Orient et de l’Afrique




