Aperçu du marché :
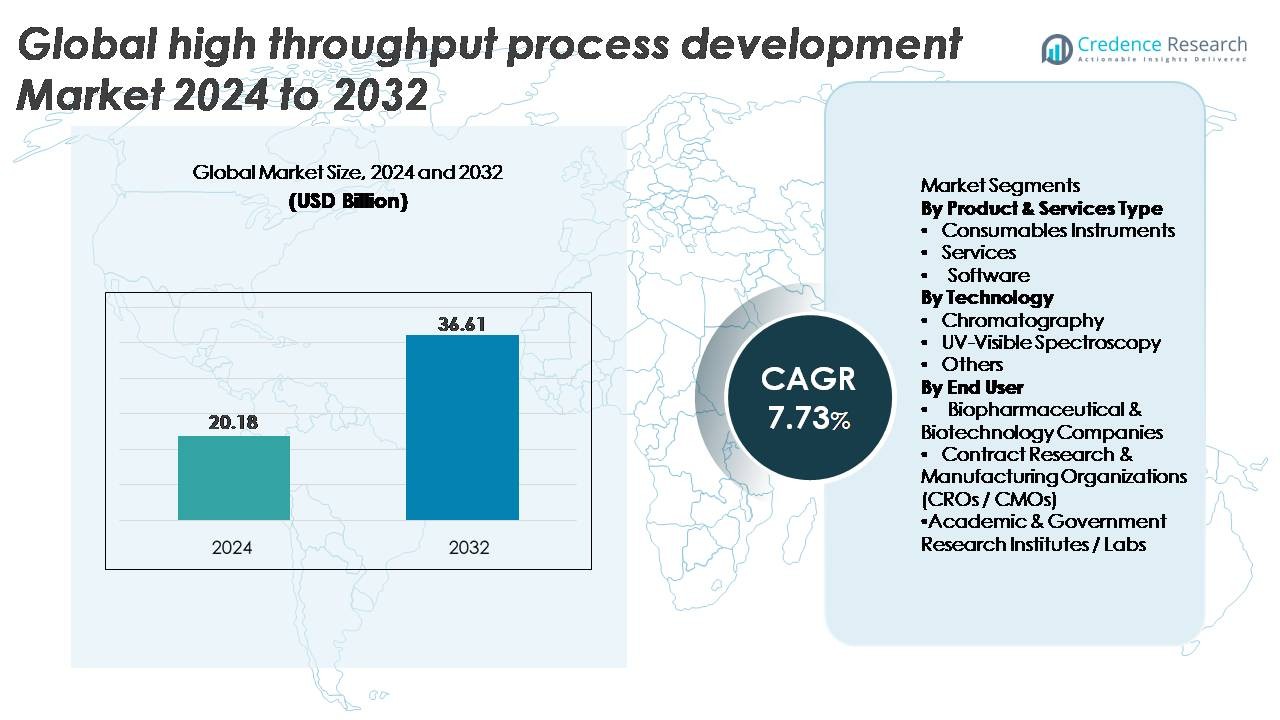
Le marché mondial du développement de processus à haut débit était évalué à 20,18 milliards USD en 2024 et devrait atteindre 36,61 milliards USD d’ici 2032, avec un TCAC de 7,73 % au cours de la période de prévision.
| ATTRIBUT DU RAPPORT |
DÉTAILS |
| Période historique |
2020-2023 |
| Année de base |
2024 |
| Période de prévision |
2025-2032 |
| Taille du marché du développement de processus à haut débit 2024 |
20,18 milliards USD |
| Marché du développement de processus à haut débit, TCAC |
7,73% |
| Taille du marché du développement de processus à haut débit 2032 |
36,61 milliards USD |
Le marché mondial du développement de processus à haut débit est façonné par un groupe solide de leaders technologiques, y compris Sartorius AG, Tecan Trading AG, Thermo Fisher Scientific Inc., Agilent Technologies, Danaher Corporation, Luminex Applikon, Merck KGaA, Eppendorf AG, GE Healthcare, et Bio-Rad Laboratories Inc. Ces entreprises rivalisent grâce à des bioréacteurs multi-parallèles avancés, des systèmes de chromatographie à haut débit, des plateformes de manipulation de liquides automatisées et des logiciels analytiques intégrés qui améliorent la vitesse et la précision de l’optimisation des processus. L’Amérique du Nord domine le marché avec environ 38 % de part, soutenue par une infrastructure de R&D biopharmaceutique mature et une adoption rapide de l’automatisation et du biotraitement numérique. L’Europe suit avec environ 29 %, grâce à un alignement réglementaire solide et des capacités de fabrication de produits biologiques bien établies.
Access crucial information at unmatched prices!
Request your sample report today & start making informed decisions powered by Credence Research Inc.!
Download Sample
Perspectives du marché :
- Le marché mondial du développement de processus à haut débit était évalué à 20,18 milliards USD en 2024 et devrait atteindre 36,61 milliards USD d’ici 2032, avec un TCAC de 7,73 %.
- La croissance du marché est stimulée par l’expansion rapide des pipelines de produits biologiques, la demande croissante pour un dépistage plus rapide des molécules et l’adoption accrue de bioréacteurs multi-parallèles automatisés et de systèmes de chromatographie à haut débit dans la R&D biopharmaceutique.
- Les tendances clés incluent l’intégration de l’analyse prédictive pilotée par l’IA, l’utilisation accrue de plateformes de dépistage microfluidiques et les solutions de biotraitement numérique qui améliorent le débit expérimental, la robustesse des processus et l’intelligence des données.
- La concurrence s’intensifie à mesure que les principaux acteurs innovent dans l’automatisation, les consommables et l’analyse, le segment des consommables détenant la plus grande part en raison de leur utilisation continue dans les flux de travail de dépistage et de purification ; cependant, le coût élevé du capital reste une contrainte pour les laboratoires de biotechnologie émergents.
- Régionalement, l’Amérique du Nord est en tête avec 38 %, suivie de l’Europe à 29 % et de l’Asie-Pacifique à 23 %, reflétant de forts investissements en R&D et l’expansion des écosystèmes de fabrication de produits biologiques.
 Analyse de la segmentation du marché :
Analyse de la segmentation du marché :
Par type de produits & services
Les consommables représentent le segment dominant, détenant la plus grande part de marché en raison de leur utilisation récurrente dans le dépistage rapide, la préparation d’essais et l’optimisation des flux de travail en chromatographie. Les plateformes à haut débit dépendent fortement des microplaques, des résines, des médias de filtration et des réactifs d’essai, rendant les consommables essentiels pour les cycles continus de développement bioprocessus. Leur adoption est en outre stimulée par l’expansion des systèmes de bioréacteurs multi-parallèles et des flux de travail de manipulation de liquides automatisés qui nécessitent des ensembles de consommables standardisés et de haute qualité pour maintenir la cohérence des processus. L’intensité croissante de la R&D biopharmaceutique et la fréquence accrue du dépistage des clones, des milieux et des tampons renforcent la forte demande pour ce segment.
- Par exemple, le système ambr® 250 de Sartorius utilise des consommables de récipients à usage unique avec des volumes de travail de 100 à 250 mL sur jusqu’à 24 bioréacteurs parallèles, tandis que les colonnes HiScreen de Cytiva permettent jusqu’à 4 mL de volume de résine par colonne pour des séries de dépistage rapide de résines, soutenant des études de purification à haut débit.
Par technologie
La chromatographie reste la technologie dominante, capturant la plus grande part de marché en raison de son rôle central dans la purification, le dépistage des résines et l’optimisation des paramètres de séparation lors du développement de bioprocessus. Les systèmes de chromatographie à haut débit permettent de dépister simultanément des centaines de conditions, raccourcissant considérablement les délais de purification. L’adoption augmente à mesure que les fabricants de biomédicaments accélèrent les programmes d’anticorps monoclonaux, de protéines recombinantes et de vecteurs viraux nécessitant des flux de travail de séparation de précision. L’intégration de colonnes miniatures, de plateformes de chromatographie multi-colonnes et d’outils de sélection de résine automatisés favorise davantage la domination de la chromatographie sur la spectroscopie UV-visible et d’autres méthodes analytiques.
- Par exemple, la plateforme ÄKTA avant de Cytiva prend en charge le criblage automatisé de méthodes avec des débits allant jusqu’à 25 mL/min et s’adapte aux formats de colonnes HiTrap et HiScale allant de 1 mL à 160 mL, tandis que les unités OPUS RoboColumn de Repligen fournissent des colonnes miniatures pré-remplies aussi petites que 200 µL, permettant une évaluation rapide de plusieurs chimies de résine en une seule exécution.
Par utilisateur final
Les entreprises biopharmaceutiques et biotechnologiques dominent le segment des utilisateurs finaux, représentant la plus grande part de marché car elles déploient des systèmes à haut débit pour rationaliser le criblage de molécules, la caractérisation des procédés et les activités de mise à l’échelle. La demande est alimentée par l’expansion des pipelines de produits biologiques, y compris les anticorps monoclonaux, les vecteurs de thérapie cellulaire et génique, et les protéines recombinantes qui nécessitent des cycles de développement de procédés rapides et riches en données. Ces entreprises investissent de plus en plus dans des bioréacteurs parallèles automatisés, des systèmes microfluidiques et des analyses prédictives de procédés pour accélérer le temps d’accès à la clinique. Les CRO/CMO et les instituts académiques adoptent également des flux de travail à haut débit, mais leur intensité d’utilisation reste inférieure à celle des environnements de R&D biopharmaceutiques entièrement intégrés.
Principaux moteurs de croissance :
Expansion des pipelines de produits biologiques et demande accrue de criblage de molécules
L’expansion rapide des pipelines de produits biologiques—including les anticorps monoclonaux, les anticorps bispécifiques, les protéines recombinantes et les vecteurs viraux—augmente considérablement la demande pour les plateformes de développement de procédés à haut débit (HTPD). Les entreprises biopharmaceutiques nécessitent un criblage rapide et riche en données des lignées cellulaires, des compositions de milieux, des conditions de tampon et des chimies de résine pour raccourcir les cycles de développement et améliorer la fidélité des procédés en phase précoce. Les technologies à haut débit permettent des expérimentations parallèles, réduisant les délais d’optimisation de mois à semaines. De plus, l’essor de nouvelles modalités telles que les thérapeutiques à base d’ARNm, les constructions d’édition génique et les composants de thérapie cellulaire nécessite une caractérisation complexe des procédés, renforçant encore la demande pour des bioréacteurs multi-parallèles, des systèmes de chromatographie automatisés et des outils d’optimisation microfluidiques. Alors que les attentes réglementaires pour la robustesse des procédés augmentent, les entreprises adoptent le HTPD pour générer des ensembles de données complets qui soutiennent les cadres de qualité par la conception (QbD). Ce moteur reste fondamental alors que les dépenses mondiales en R&D s’intensifient et que les pipelines de développement de produits biologiques se diversifient dans les domaines de l’oncologie, des maladies rares et de l’immunothérapie.
- Par exemple, le système ambr® 15 de Sartorius permet jusqu’à 48 bioréacteurs parallèles fonctionnant à un volume de travail de 10 à 15 mL, tandis que la plateforme Beacon® de Berkeley Lights peut cribler plus de 3 000 cellules uniques simultanément, générant des données fonctionnelles en moins de 24 heures, accélérant considérablement la sélection de clones et le criblage précoce de produits biologiques.
Adoption croissante de l’automatisation, de la robotique et du biotraitement numérique
L’automatisation sert de catalyseur de croissance essentiel alors que les organisations passent de l’expérimentation manuelle à des flux de travail robotisés et améliorés par l’IA. Les manipulateurs de liquides automatisés, les systèmes de microplaques intégrés et les bioréacteurs multi-parallèles réduisent considérablement les erreurs humaines, augmentent le débit et standardisent la conception expérimentale. Les plateformes de biotraitement numérique intègrent désormais des algorithmes d’apprentissage automatique pour l’optimisation des paramètres, la modélisation prédictive et le contrôle adaptatif en temps réel, permettant une convergence plus rapide vers des conditions de processus optimales. Les systèmes de chromatographie automatisés et les stations de préparation d’échantillons robotiques améliorent encore l’efficacité de la purification et la reproductibilité analytique. Ces capacités permettent aux équipes de développement d’évaluer des milliers de conditions dans des délais compressés, soutenant des stratégies de triage rapide des molécules et d’intensification des processus. La prolifération de la gestion des données basée sur le cloud, des cahiers de laboratoire électroniques intégrés et des jumeaux numériques permet la collaboration inter-sites et accélère le transfert de technologie. Collectivement, la synergie entre automatisation et digitalisation stimule l’adoption à grande échelle, en particulier au sein des centres d’innovation biopharmaceutique et des organisations de développement sous contrat.
- Par exemple, la plateforme Microlab STAR de Hamilton offre une haute précision (par exemple, une précision typique de <1,0 % et une précision de <0,8 % CV à 50 µL) et peut traiter jusqu'à des plaques de 384 puits avec son option MultiProbe Head, permettant des applications à haut débit en génomique et en diagnostics cliniques.
Besoins croissants en accélération de l’échelle et en intensification des processus dans la bioproduction
Le mouvement de l’industrie vers une bioproduction intensifiée, continue et flexible crée une forte demande pour des outils HTPD qui soutiennent une montée en échelle rapide et une définition de processus robuste. Alors que les entreprises poursuivent des délais cliniques accélérés et des modèles de production rentables, les systèmes à haut débit fournissent les ensembles de données fondamentaux nécessaires pour passer de l’échelle de laboratoire à l’échelle pilote avec un risque réduit. Les mini-bioréacteurs multi-parallèles permettent une exploration en temps réel des paramètres critiques du processus tels que le pH, l’oxygène dissous, l’agitation et les stratégies d’alimentation en nutriments, garantissant des performances prévisibles à toutes les échelles. De même, les outils de purification à haut débit permettent une sélection rapide des résines, une optimisation des conditions de liaison et un profilage d’élution. Ces capacités sont essentielles pour le biotraitement continu, les opérations basées sur la perfusion et les stratégies intensifiées en aval. Avec la pression croissante pour livrer des processus prêts pour la commercialisation plus tôt dans le développement, le HTPD devient indispensable pour éliminer les goulots d’étranglement, améliorer la cohérence des processus et renforcer les soumissions réglementaires grâce à des ensembles de données riches et statistiquement significatifs.
Principales tendances et opportunités :
Intégration de l’analyse prédictive pilotée par l’IA et de la modélisation avancée des données
L’intelligence artificielle émerge comme une tendance transformatrice, permettant des insights plus profonds dans les ensembles de données à haut débit et accélérant la prise de décision. Les modèles pilotés par l’IA analysent des paramètres multidimensionnels, identifient des interactions non linéaires et prédisent des conditions de processus optimales avec une précision sans précédent. Les algorithmes d’apprentissage automatique peuvent recommander des conceptions expérimentales, signaler des comportements aberrants et simuler des résultats expérimentaux, réduisant ainsi la charge de travail en laboratoire humide. Les jumeaux numériques pour le développement de bioprocédés permettent la simulation de cinétiques de fermentation, de profils chromatographiques et de scénarios d’agrandissement, permettant aux équipes de tester virtuellement les conditions avant d’exécuter des expériences. Cette tendance ouvre des opportunités pour une robustesse accrue des processus, des délais de développement réduits et une documentation QbD renforcée. À mesure que les ensembles de données deviennent plus complexes, en particulier pour les processus de thérapie cellulaire et génique, l’intégration de l’IA devient essentielle pour gérer la variabilité et identifier les moteurs de performance cachés. Les fournisseurs proposant des logiciels avec des analyses intégrées, des modélisations automatisées et des outils de visualisation obtiennent un avantage concurrentiel significatif à mesure que le biotraitement basé sur les données devient la norme de l’industrie.
- Par exemple, le logiciel BioTek Gen5 d’Agilent traite plus de 10 000 points de données par lecture de microplaque et intègre des modules de courbe ajustée par l’IA capables de générer des modèles cinétiques en moins de 30 secondes, tandis que la plateforme d’analyse de données de Sartorius prend en charge la modélisation en temps réel de plus de 200 paramètres de processus simultanément pendant le développement en amont.
Adoption croissante de mini-bioréacteurs multiparallèles et de plateformes de criblage microfluidiques
Les bioréacteurs multiparallèles et les systèmes microfluidiques transforment le développement de processus en phase précoce en permettant de tester simultanément des centaines de conditions avec une consommation minimale de ressources. Ces technologies évolutives offrent un contrôle précis des conditions de culture et permettent une cartographie haute résolution des paramètres critiques. Les plateformes microfluidiques soutiennent des expériences à très petit volume, réduisant l’utilisation de réactifs tout en préservant la pertinence biologique, ce qui les rend idéales pour le criblage de clones, l’optimisation des milieux et les études de production de vecteurs viraux. À mesure que la fabrication se déplace vers des modèles intensifiés et continus, le besoin d’évaluations en amont rapides et rentables augmente fortement. Cette tendance crée des opportunités pour les intégrateurs de systèmes, les fournisseurs de consommables et les éditeurs de logiciels de proposer des solutions qui combinent des tests parallèles avec des analyses en temps réel. Une reproductibilité améliorée, une variabilité réduite et des coûts d’exploitation plus bas positionnent ces plateformes comme des facilitateurs critiques de l’innovation bioprocessus de nouvelle génération.
- Par exemple, le système modulaire ambr® 250 de Sartorius permet jusqu’à 24 bioréacteurs parallèles avec des volumes de travail de 100 à 250 mL, tandis que les plateformes microfluidiques telles que le système Nadia de Dolomite Bio peuvent exécuter jusqu’à 6 000 réactions monocellulaires encapsulées par puce dans une seule expérience, augmentant considérablement le débit et accélérant le criblage des variantes.
Principaux défis :
Exigences élevées en matière d’investissement en capital et complexité d’intégration
Malgré de forts avantages, les systèmes à haut débit nécessitent un investissement initial important dans des instruments automatisés, des équipements analytiques, de la robotique et une infrastructure de gestion des données. Les petites entreprises de biotechnologie, les laboratoires universitaires et les fabricants des marchés émergents ont souvent du mal à justifier les coûts associés aux bioréacteurs multi-parallèles, aux plateformes de chromatographie avancées et aux logiciels pilotés par l’IA. Les défis d’intégration s’intensifient lors de la combinaison d’outils de différents fournisseurs, créant des problèmes d’interopérabilité entre le matériel, les formats de données et les systèmes de contrôle. La mise en œuvre de ces technologies nécessite également une formation spécialisée, des capacités avancées en bioinformatique et une coordination interfonctionnelle entre les équipes de R&D, de développement de processus et de fabrication. À mesure que les organisations biopharmaceutiques étendent les plateformes numériques et automatisées, la gestion du contrôle des changements, de la validation et de la conformité réglementaire ajoute une complexité supplémentaire. Ces obstacles peuvent ralentir l’adoption, en particulier dans les environnements à ressources limitées.
Surcharge de données, complexité des flux de travail et goulots d’étranglement analytiques
Les plateformes à haut débit génèrent des ensembles de données massifs, nécessitant des systèmes de gestion de données sophistiqués, une puissance de calcul et des pipelines analytiques avancés. Sans infrastructure appropriée, les organisations font face à des goulots d’étranglement dans le nettoyage, la normalisation, la visualisation et l’interprétation des données. La gestion de ce volume de données peut mettre à rude épreuve les systèmes LIMS, retarder la prise de décision et augmenter le risque d’incohérences analytiques. La complexité des flux de travail augmente à mesure que la densité expérimentale s’accroît, nécessitant une coordination étroite entre les équipes en amont, en aval et analytiques. De plus, la standardisation des protocoles entre les instruments reste un défi, entraînant des variabilités et des difficultés de comparabilité entre les études. Une expertise insuffisante en modélisation statistique et en analyses pilotées par ML complique encore l’adoption. Ces défis soulignent la nécessité de flux de travail harmonisés, d’écosystèmes numériques robustes et de plateformes analytiques intégrées qui simplifient l’interprétation des données et soutiennent un développement de processus efficace et de haute qualité.
Analyse régionale :
Amérique du Nord
L’Amérique du Nord occupe la position dominante sur le marché mondial du développement de processus à haut débit, représentant environ 38 % de la part totale, grâce à de solides pipelines de R&D en biologie et à une adoption extensive de plateformes de biotraitement automatisées et activées par l’IA. Le leadership de la région est renforcé par une infrastructure de bioproduction avancée, des investissements significatifs dans les laboratoires numériques et l’intégration précoce de bioréacteurs multi-parallèles et de systèmes de chromatographie à haut débit. Les grandes entreprises biopharmaceutiques et les CDMO aux États-Unis accélèrent la demande en donnant la priorité au criblage rapide des molécules et à une caractérisation robuste des processus. Des cadres réglementaires favorables et un financement soutenu pour les innovations en biologie renforcent encore l’avantage du marché de la région.
Europe
L’Europe capture environ 29 % du marché mondial, soutenue par une forte présence de fabricants pharmaceutiques, d’instituts de recherche spécialisés et de fournisseurs de technologies de biotraitement établis. La région bénéficie d’investissements significatifs dans le biotraitement continu, la numérisation et le développement intensifié en amont. Des pays comme l’Allemagne, le Royaume-Uni et la Suisse sont à l’avant-garde de l’adoption grâce à des écosystèmes de production de produits biologiques matures et à des programmes d’innovation financés par le gouvernement. Les systèmes à haut débit sont de plus en plus déployés pour améliorer la sélection des clones, l’optimisation de la purification et les études de mise à l’échelle, en particulier dans le développement d’anticorps thérapeutiques et de thérapies cellulaires. L’accent mis par l’Europe sur la conformité réglementaire et les méthodologies de qualité par conception continue d’accélérer l’adoption tant dans l’industrie que dans le milieu universitaire.
Asie-Pacifique
L’Asie-Pacifique émerge comme la région à la croissance la plus rapide, contribuant à environ 23 % de la part de marché mondiale, stimulée par l’expansion des pôles de fabrication de produits biologiques en Chine, en Inde, en Corée du Sud et à Singapour. La croissance rapide des biosimilaires, du développement de vaccins et de la recherche en thérapie cellulaire alimente des investissements significatifs dans le criblage à haut débit, les mini-bioréacteurs et les plateformes de purification automatisées. Les CDMO régionaux adoptent de plus en plus des outils à haut débit pour servir des clients mondiaux nécessitant des délais de développement accélérés. Les initiatives soutenues par le gouvernement en faveur de l’innovation biotechnologique, combinées à l’expansion des capacités nationales de R&D, renforcent la demande dans les universités, les entreprises biopharmaceutiques et les centres technologiques. L’environnement de fabrication compétitif en termes de coûts de l’APAC accélère encore l’adoption à grande échelle des systèmes modernes à haut débit.
Amérique latine
L’Amérique latine détient environ 6 % du marché mondial, avec une adoption progressive stimulée par des investissements croissants dans la fabrication pharmaceutique et des améliorations dans l’infrastructure biotechnologique régionale. Le Brésil, le Mexique et l’Argentine sont à la tête de la demande alors que les instituts de recherche et certaines entreprises biopharmaceutiques intègrent des outils à haut débit pour améliorer l’efficacité du développement en amont et en aval. Bien que l’adoption en soit à un stade précoce par rapport aux marchés matures, l’intérêt pour l’expérimentation automatisée, les systèmes de flux de travail numériques et les technologies analytiques avancées augmente. La participation croissante à la recherche clinique mondiale et l’expansion des partenariats avec des entreprises biopharmaceutiques multinationales devraient soutenir la modernisation continue des capacités de développement des procédés.
Moyen-Orient & Afrique
La région du Moyen-Orient & Afrique (MEA) représente environ 4 % de la part de marché mondiale, avec une adoption principalement motivée par les activités émergentes de bioproduction aux Émirats arabes unis, en Arabie saoudite et en Afrique du Sud. Les investissements dans les parcs des sciences de la vie, les installations de production de vaccins et les centres de recherche en biotechnologie contribuent à des progrès constants. Bien que les systèmes à haut débit restent limités en raison de contraintes budgétaires et de lacunes infrastructurelles, les stratégies de diversification soutenues par le gouvernement augmentent la demande de technologies modernes de développement de bioprocédés. Les collaborations avec des fournisseurs de technologies internationaux et des institutions académiques soutiennent des améliorations progressives dans les capacités d’analyse des procédés, de criblage automatisé et de laboratoire numérique sur les principaux marchés de la MEA.
Segmentation du marché :
Par type de produits & services
- Consommables
- Instruments
- Services
- Logiciels
Par technologie
- Chromatographie
- Spectroscopie UV-Visible
- Autres
Par utilisateur final
- Entreprises biopharmaceutiques et biotechnologiques
- Organisations de recherche et de fabrication sous contrat (CRO / CMO)
- Instituts / laboratoires de recherche académiques et gouvernementaux
Par Géographie
- Amérique du Nord
- États-Unis
- Canada
- Mexique
- Europe
- Allemagne
- France
- Royaume-Uni
- Italie
- Espagne
- Reste de l’Europe
- Asie-Pacifique
- Chine
- Japon
- Inde
- Corée du Sud
- Asie du Sud-Est
- Reste de l’Asie-Pacifique
- Amérique Latine
- Brésil
- Argentine
- Reste de l’Amérique Latine
- Moyen-Orient & Afrique
- Pays du CCG
- Afrique du Sud
- Reste du Moyen-Orient et de l’Afrique
Paysage Concurrentiel :
Le paysage concurrentiel du marché mondial du développement de processus à haut débit se caractérise par une forte participation des leaders de la technologie bioprocess, des spécialistes de l’automatisation et des innovateurs en logiciels axés sur l’accélération des délais de développement des produits biologiques. Les entreprises rivalisent en faisant progresser les plateformes de bioréacteurs multi-parallèles, en intégrant des analyses pilotées par l’IA et en améliorant les systèmes de chromatographie à haut débit et de microfluidique qui soutiennent le criblage rapide et l’optimisation de la purification. Les principaux fournisseurs offrent de plus en plus des solutions de bout en bout combinant instruments, consommables et logiciels de flux de travail numériques pour renforcer la fidélisation des clients et rationaliser le développement des processus. Les collaborations stratégiques entre les entreprises biopharmaceutiques, les CDMO et les fournisseurs de technologies se développent, en particulier dans les domaines impliquant le biotraitement intensifié et continu. Les fusions et acquisitions jouent également un rôle clé, les grands acteurs cherchant à acquérir des innovateurs de niche dans les technologies de microfluidique, de bioréacteurs miniaturisés et de laboratoires autonomes. Les investissements continus dans l’automatisation, l’analyse prédictive et les plateformes de gestion des données basées sur le cloud façonnent un environnement concurrentiel axé sur la livraison d’une plus grande rapidité, évolutivité et reproductibilité pour les pipelines de produits biologiques de nouvelle génération.
Analyse des acteurs clés :
- Sartorius AG
- Tecan Trading AG
- Thermo Fisher Scientific Inc.
- Agilent Technologies
- Danaher Corporation
- Luminex Applikon
- Merck KGaA
- Eppendorf AG
- GE Healthcare
- Bio-Rad Laboratories Inc.
Développements récents :
- En juin 2025, Sartorius AG a lancé la plateforme de cytométrie iQue 5 HTS, améliorant la vitesse et la flexibilité de la cytométrie en flux à haut débit.
- En novembre 2024, Sartorius AG a ouvert un nouveau Centre pour l’Innovation en Bioprocédés à Marlborough (USA) pour soutenir le développement de procédés et la fabrication en suite GMP.
- En janvier 2024, Tecan Trading AG a introduit des outils numériques de productivité de laboratoire au SLAS 2024, y compris “Next-Gen Introspect”, prévu pour une sortie commerciale au T2 2024, visant à améliorer les flux de travail d’expérimentation à haut débit.
Shape Your Report to Specific Countries or Regions & Enjoy 30% Off!
Couverture du rapport :
Le rapport de recherche offre une analyse approfondie basée sur le type de produits et services, la technologie, l’utilisateur final et la géographie. Il détaille les principaux acteurs du marché, fournissant un aperçu de leur entreprise, de leurs offres de produits, de leurs investissements, de leurs sources de revenus et de leurs applications clés. De plus, le rapport inclut des informations sur l’environnement concurrentiel, l’analyse SWOT, les tendances actuelles du marché, ainsi que les principaux moteurs et contraintes. En outre, il discute des divers facteurs qui ont stimulé l’expansion du marché ces dernières années. Le rapport explore également la dynamique du marché, les scénarios réglementaires et les avancées technologiques qui façonnent l’industrie. Il évalue l’impact des facteurs externes et des changements économiques mondiaux sur la croissance du marché. Enfin, il fournit des recommandations stratégiques pour les nouveaux entrants et les entreprises établies afin de naviguer dans les complexités du marché.
Perspectives futures :
- Les plateformes à haut débit deviendront essentielles pour accélérer les cycles de développement des produits biologiques, des biosimilaires et des thérapies avancées.
- Les mini-bioréacteurs multi-parallèles remplaceront de plus en plus les systèmes traditionnels à l’échelle du banc pour le dépistage précoce des procédés.
- Les analyses prédictives pilotées par l’IA automatiseront davantage la sélection des conditions, réduisant la charge expérimentale et améliorant la précision des processus.
- Les technologies microfluidiques se développeront, permettant le dépistage à très faible volume pour les lignées cellulaires, les milieux et l’optimisation des vecteurs.
- Les stratégies de biotraitement continu et intensifié augmenteront la dépendance aux outils de purification à haut débit et de dépistage de résine.
- Les plateformes de données natives du cloud standardiseront la collaboration intersites et renforceront les écosystèmes de biotraitement numérique.
- Les CDMO investiront massivement dans des suites automatisées à haut débit pour soutenir des délais clients plus rapides et une préparation à l’échelle.
- L’intégration entre les outils à haut débit en amont et en aval créera des flux de travail de développement plus unifiés et de bout en bout.
- Les attentes réglementaires pour des soumissions QbD riches en données accéléreront l’adoption d’expérimentations automatisées et à haute résolution.
- Les marchés émergents en Asie-Pacifique stimuleront l’expansion mondiale à mesure que les capacités de bioproduction régionales se modernisent rapidement.

 Analyse de la segmentation du marché :
Analyse de la segmentation du marché :

