Panoramica del Mercato:
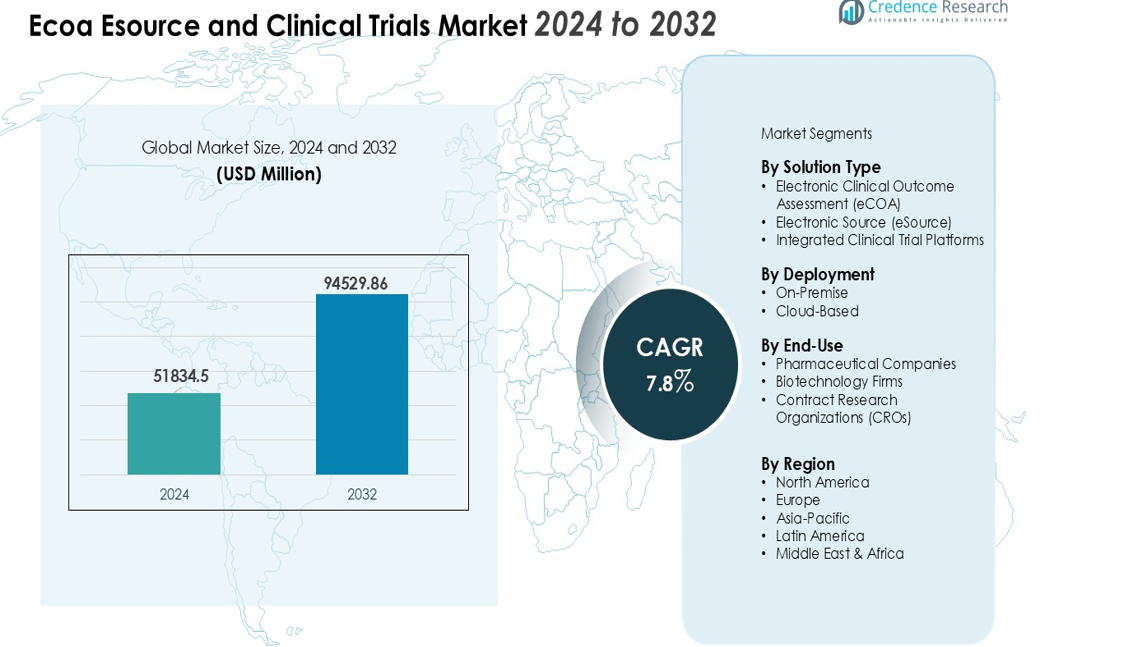
La dimensione del mercato di Ecoa Esource e Clinical Trials è stata valutata a 51834,5 milioni di USD nel 2024 e si prevede che raggiungerà 94529,86 milioni di USD entro il 2032, con un CAGR del 7,8% durante il periodo di previsione (2024-2032).
| ATTRIBUTO DEL RAPPORTO |
DETTAGLI |
| Periodo Storico |
2020-2023 |
| Anno Base |
2024 |
| Periodo di Previsione |
2025-2032 |
| Dimensione del Mercato eCOA, eSource e Clinical Trials 2024 |
51834,5 milioni di USD |
| Mercato eCOA, eSource e Clinical Trials, CAGR |
7,8% |
| Dimensione del Mercato eCOA, eSource e Clinical Trials 2032 |
94529,86 milioni di USD |
I principali driver del mercato includono l’aumento del volume e della complessità degli studi clinici a livello mondiale, che richiedono una raccolta dati elettronica semplificata, un monitoraggio in tempo reale e una gestione sicura dei dati. Il passaggio verso studi clinici decentralizzati e incentrati sul paziente, abilitato dal monitoraggio remoto, dispositivi indossabili, applicazioni di salute mobile e piattaforme elettroniche basate su cloud, ha ulteriormente accelerato l’adozione di soluzioni eCOA e eSource. Inoltre, l’incoraggiamento normativo per le valutazioni elettroniche degli esiti clinici e la crescente necessità di integrità, trasparenza ed efficienza dei dati stanno rafforzando l’espansione del mercato.
A livello regionale, Nord America guida il mercato, supportato da un’infrastruttura avanzata di R&S farmaceutica, adozione precoce della tecnologia e quadri normativi favorevoli. Nel frattempo, Asia-Pacifico sta emergendo come la regione in più rapida crescita grazie all’aumento delle attività di ricerca clinica, all’esternalizzazione degli studi e all’adozione di soluzioni di gestione digitale degli studi, presentando significative opportunità di crescita per il mercato.
Approfondimenti di Mercato:
- Il mercato Ecoa Esource e Clinical Trials è stato valutato a 51.834,5 milioni di USD nel 2024 e si prevede che raggiungerà 94.529,86 milioni di USD entro il 2032, con una crescita a un CAGR del 7,8%.
- L’aumento della complessità e del volume delle sperimentazioni cliniche globali spinge la domanda di soluzioni digitali che consentano la raccolta dati in tempo reale, riducano gli errori e garantiscano la conformità ai protocolli.
- Le sperimentazioni decentralizzate e incentrate sul paziente stanno accelerando l’adozione di soluzioni eCOA ed eSource, supportate da dispositivi indossabili, app di salute mobile e piattaforme di monitoraggio remoto.
- Il supporto normativo per le valutazioni elettroniche degli esiti clinici migliora l’adozione del mercato, consentendo dati di prova accurati, tracciabili e verificabili.
- L’attenzione all’integrità dei dati, alla trasparenza e all’efficienza operativa motiva le aziende farmaceutiche e biotecnologiche ad adottare piattaforme digitali integrate per la gestione delle sperimentazioni.
- Alti costi di implementazione, integrazione complessa con sistemi legacy e requisiti stringenti di privacy dei dati pongono sfide all’adozione diffusa.
- A livello regionale, il Nord America guida con una quota di mercato del 42% grazie a un’infrastruttura avanzata di R&S, l’Europa detiene il 28% supportata dall’armonizzazione normativa e l’Asia-Pacifico rappresenta il 20% e cresce più velocemente grazie all’aumento delle attività di ricerca clinica e all’outsourcing.
Access crucial information at unmatched prices!
Request your sample report today & start making informed decisions powered by Credence Research Inc.!
Download Sample
Fattori di Mercato:
Aumento della Complessità e del Volume delle Sperimentazioni Cliniche che Guidano l’Adozione di Soluzioni Digitali
L’aumento della complessità e del volume delle sperimentazioni cliniche a livello globale ha creato una forte necessità di soluzioni digitali. Gli sponsor richiedono una raccolta dati accurata e in tempo reale per garantire l’efficienza delle sperimentazioni e la sicurezza dei pazienti. Il mercato eCOA, eSource e Clinical Trials beneficia della sua capacità di semplificare la gestione dei dati in più siti. Riduce gli errori nell’inserimento dei dati e accelera l’adesione ai protocolli. Questa efficienza aiuta le organizzazioni a soddisfare i requisiti normativi gestendo studi più grandi e complessi.
- Ad esempio, Medable, un pioniere nelle sperimentazioni cliniche decentralizzate, integra tecnologie di telemedicina, ePRO e monitoraggio remoto, consentendo l’accesso e la collaborazione in tempo reale tra i siti, il che ha aiutato a ridurre le visite ai siti del 30% negli studi recenti.
Passaggio Verso Sperimentazioni Cliniche Decentralizzate e Incentrate sul Paziente che Aumentano la Domanda di Mercato
Le sperimentazioni cliniche si stanno spostando verso modelli decentralizzati, concentrandosi sulla comodità del paziente e sulla partecipazione remota. Consente la raccolta dati da dispositivi indossabili, applicazioni di salute mobile e sistemi di monitoraggio domiciliare. Il mercato eCOA, eSource e Clinical Trials supporta questa trasformazione fornendo accesso sicuro e in tempo reale agli esiti riportati dai pazienti. Le organizzazioni ottengono flessibilità e un migliore coinvolgimento con i partecipanti. Questa tendenza aumenta la domanda di piattaforme digitali per sperimentazioni cliniche capaci di monitoraggio remoto.
- Ad esempio, Science 37, la sua soluzione di reclutamento dei pazienti ha permesso ai clienti di arruolare il 42% di una coorte di prova in otto settimane per uno studio su una malattia rara. L’azienda riporta anche che la sua piattaforma tecnologica accelera l’arruolamento fino a 15 volte più velocemente rispetto ai metodi tradizionali, fornendo il 100% di referenze mediche qualificate.
Incoraggiamento Normativo per le Valutazioni Elettroniche degli Esiti Clinici che Guida l’Implementazione
Le agenzie regolatorie stanno sempre più supportando i metodi elettronici per le valutazioni degli esiti clinici. Migliora l’accuratezza, la tracciabilità e l’auditabilità dei dati di prova. La conformità a queste normative è fondamentale per le approvazioni globali delle prove. Il mercato eCOA, eSource e Clinical Trials fornisce soluzioni elettroniche standardizzate per soddisfare questi requisiti. Le aziende beneficiano di una revisione normativa più rapida e di un rischio ridotto di discrepanze nei dati.
Crescente Attenzione all’Integrità dei Dati, Trasparenza ed Efficienza Operativa
Le aziende farmaceutiche e biotecnologiche danno priorità all’integrità dei dati e all’efficienza operativa nelle sperimentazioni cliniche. Garantisce risultati affidabili e mantiene la credibilità dello sponsor. Il mercato eCOA, eSource e Clinical Trials consente una cattura dati coerente, un’archiviazione sicura e una reportistica semplificata. Le organizzazioni riducono gli errori manuali e risparmiano tempo durante l’analisi. Questa attenzione ai dati di alta qualità e trasparenti continua a guidare l’adozione di soluzioni digitali per la gestione delle prove.
Tendenze di Mercato:
Integrazione di Tecnologie Digitali Avanzate per Migliorare l’Efficienza delle Sperimentazioni Cliniche
Il mercato eCOA, eSource e Clinical Trials mostra una forte tendenza verso l’integrazione di tecnologie digitali avanzate, tra cui il cloud computing, l’intelligenza artificiale e il machine learning. Consente agli sponsor di analizzare grandi volumi di dati clinici in tempo reale e identificare modelli che supportano decisioni più rapide. I dispositivi di monitoraggio remoto dei pazienti e le applicazioni mobili forniscono flussi di dati continui direttamente ai database delle prove. Riduce i ritardi operativi e migliora la conformità ai protocolli in più siti di studio. Le organizzazioni si affidano sempre più a queste tecnologie per migliorare la qualità delle prove e ridurre i costi. Gli strumenti di visualizzazione dei dati e le funzionalità di reportistica automatizzata aiutano le parti interessate a monitorare efficacemente i progressi delle prove.
- Ad esempio, la piattaforma WeTrials consente l’accesso remoto dei pazienti e fornisce risorse educative e orientamento personalizzato per aiutare i partecipanti a trovare e navigare nelle sperimentazioni cliniche, dimostrando uno sforzo per migliorare il coinvolgimento dei pazienti e semplificare le operazioni negli studi multi-sito.
Espansione delle Prove Decentralizzate e Focus su Approcci Centrati sul Paziente
Le sperimentazioni cliniche decentralizzate continuano a guadagnare slancio, enfatizzando la comodità del paziente e la partecipazione remota. Il mercato eCOA, eSource e Clinical Trials supporta queste prove fornendo soluzioni sicure di cattura e gestione elettronica dei dati. Consente l’input diretto del paziente tramite dispositivi mobili, sensori indossabili e monitoraggio domiciliare, garantendo l’accesso in tempo reale per i ricercatori. Questo approccio migliora il coinvolgimento e la ritenzione dei pazienti mantenendo l’integrità dei dati. Gli sponsor adottano piattaforme che consentono l’integrazione di più fonti di dati per una visione olistica dei risultati delle prove. Le piattaforme di prove digitali facilitano un reclutamento più rapido e ampliano l’accesso a popolazioni di pazienti diversificate. La tendenza del mercato riflette un movimento sostenuto verso strategie di ricerca clinica più flessibili, guidate dalla tecnologia e centrate sul paziente.
- Ad esempio, Science 37 costruisce reti globali di trial decentralizzati che facilitano il reclutamento diversificato dei pazienti, portando a un accesso più ampio e a una maggiore robustezza dei risultati.
Analisi delle Sfide del Mercato:
Alti Costi di Implementazione e Integrazione Complessa Ostacolano l’Adozione
Il mercato eCOA, eSource e dei Trial Clinici affronta sfide dovute agli alti costi di implementazione e alla complessità di integrare soluzioni digitali nei flussi di lavoro clinici esistenti. Richiede un investimento significativo in infrastrutture tecnologiche, formazione del personale e manutenzione continua. Le organizzazioni più piccole spesso trovano l’adozione finanziariamente onerosa. La migrazione dei dati dai sistemi legacy può ritardare la distribuzione e interrompere i trial in corso. Problemi di compatibilità con diversi sistemi elettronici possono influenzare il flusso di dati senza interruzioni. Queste barriere rallentano l’adozione diffusa nonostante i benefici di una maggiore efficienza e precisione dei dati.
Preoccupazioni per la Privacy dei Dati, la Conformità Normativa e la Sicurezza Limitano la Crescita
La privacy dei dati e la conformità normativa rimangono sfide critiche per il mercato eCOA, eSource e dei Trial Clinici. Deve aderire a standard rigorosi per la riservatezza dei pazienti, la protezione dei dati e il trasferimento di informazioni transfrontaliere. Qualsiasi violazione della sicurezza può minare la fiducia e portare a sanzioni normative. Le variazioni nelle normative tra le regioni complicano la gestione dei trial per studi multinazionali. Le organizzazioni devono investire in misure di cybersecurity robuste e protocolli di conformità. Gestire grandi volumi di dati clinici sensibili mantenendo accuratezza e accessibilità aggiunge complessità operativa. Queste sfide limitano la crescita del mercato e richiedono una pianificazione strategica per un’implementazione sicura e conforme.
Opportunità di Mercato:
Espansione dei Trial Clinici Decentralizzati e Remoti Creando Potenziale di Crescita
Il mercato eCOA, eSource e dei Trial Clinici presenta significative opportunità attraverso l’espansione dei trial clinici decentralizzati e remoti. Consente agli sponsor di raggiungere popolazioni di pazienti più ampie e ridurre le barriere geografiche nel reclutamento dei trial. Le piattaforme digitali supportano la cattura dei dati in tempo reale da dispositivi indossabili, app mobili e sistemi di monitoraggio domestico. Le organizzazioni possono migliorare il coinvolgimento e la ritenzione dei pazienti mantenendo dati di alta qualità. L’integrazione di più fonti di dati consente un’analisi completa dei risultati dei trial. La crescente domanda di design di trial flessibili e incentrati sul paziente offre un potenziale di mercato sostenuto.
Adozione di Analisi Avanzate e Intelligenza Artificiale Migliorando le Prospettive di Mercato
L’adozione crescente di analisi avanzate, intelligenza artificiale e apprendimento automatico offre ulteriori opportunità per il mercato eCOA, eSource e dei Trial Clinici. Consente l’elaborazione efficiente di grandi volumi di dati clinici e l’identificazione di intuizioni predittive. Gli sponsor possono ottimizzare il design dei trial, monitorare la sicurezza dei pazienti e accelerare il processo decisionale. L’automazione della reportistica e della gestione del rischio migliora l’efficienza operativa. Il crescente interesse per le evidenze del mondo reale e i biomarcatori digitali supporta un’ulteriore integrazione tecnologica. Questi avanzamenti posizionano il mercato per una crescita continua e innovazione nella ricerca clinica.
Analisi della Segmentazione del Mercato:
Per Tipo di Soluzione
Il mercato degli eCOA, eSource e delle sperimentazioni cliniche è segmentato per tipo di soluzione in valutazione elettronica degli esiti clinici (eCOA), fonte elettronica (eSource) e piattaforme integrate per sperimentazioni cliniche. Consente alle organizzazioni di selezionare soluzioni in base alla complessità della sperimentazione e ai requisiti dei dati. Le soluzioni eCOA dominano l’adozione grazie alla loro capacità di catturare efficacemente gli esiti riportati dai pazienti e mantenere l’integrità dei dati. Le piattaforme eSource supportano la cattura diretta dei dati dai record medici elettronici, riducendo gli errori manuali e accelerando i tempi delle sperimentazioni. Le piattaforme integrate forniscono una gestione completa delle sperimentazioni, combinando raccolta dati, monitoraggio e reportistica in un sistema unificato. Queste soluzioni migliorano l’efficienza operativa e la qualità complessiva delle sperimentazioni.
- Ad esempio, la piattaforma digitale ICON integra moduli di eConsent, eCOA, eSource e televisita per facilitare le sperimentazioni cliniche decentralizzate, risultando in un miglioramento del 20% nell’engagement dei pazienti e una riduzione del 15% delle complessità operative delle sperimentazioni.
Per modalità di distribuzione
La distribuzione nel mercato degli eCOA, eSource e delle sperimentazioni cliniche include soluzioni on-premise e basate su cloud. Offre flessibilità per soddisfare le specifiche esigenze infrastrutturali e di sicurezza delle diverse organizzazioni. La distribuzione basata su cloud guida il mercato grazie alla sua scalabilità, accessibilità remota e ridotti costi di gestione IT. La distribuzione on-premise rimane rilevante per le organizzazioni che richiedono un controllo completo sull’archiviazione dei dati e sui sistemi interni. Entrambi i tipi di distribuzione consentono l’accesso in tempo reale ai dati e supportano modelli di sperimentazione decentralizzati. L’adozione dipende dalla dimensione della sperimentazione, dalla sensibilità dei dati e dalle capacità IT dell’organizzazione.
- Ad esempio, la piattaforma eCOA di Castor raggiunge il 90% del completamento dei test di accettazione degli utenti entro 4 settimane, mantenendo una robusta validazione in un ambiente moderno e nativo del cloud.
Per utilizzo finale
I segmenti di utilizzo finale includono aziende farmaceutiche, aziende biotecnologiche e organizzazioni di ricerca a contratto (CRO). Aiuta i promotori a gestire sperimentazioni complesse, garantire la conformità normativa e accelerare lo sviluppo dei farmaci. Le aziende farmaceutiche detengono la quota maggiore grazie agli elevati investimenti in R&S e alla necessità di soluzioni digitali efficienti. I CRO adottano sempre più queste piattaforme per fornire servizi scalabili a più promotori. Le aziende biotecnologiche sfruttano le soluzioni eCOA e eSource per migliorare le sperimentazioni centrate sul paziente e migliorare l’accuratezza dei dati. La crescita del mercato è in linea con l’espansione delle attività di ricerca clinica tra questi utenti finali.
Segmentazioni:
Per tipo di soluzione
- Valutazione Elettronica degli Esiti Clinici (eCOA)
- Fonte Elettronica (eSource)
- Piattaforme Integrate per Sperimentazioni Cliniche
Per distribuzione
- On-Premise
- Basato su Cloud
Per utilizzo finale
- Aziende Farmaceutiche
- Aziende Biotecnologiche
- Organizzazioni di Ricerca a Contratto (CRO)
Regione
- Nord America
- Stati Uniti
- Canada
- Messico
- Europa
- Germania
- Francia
- Regno Unito
- Italia
- Spagna
- Resto d’Europa
- Asia Pacifico
- Cina
- Giappone
- India
- Corea del Sud
- Sud-est asiatico
- Resto dell’Asia Pacifico
- America Latina
- Brasile
- Argentina
- Resto dell’America Latina
- Medio Oriente & Africa
- Paesi del GCC
- Sud Africa
- Resto del Medio Oriente e Africa
Analisi Regionale:
Nord America Leader nell’Adozione Grazie a un’Infrastruttura Farmaceutica Avanzata
Il Nord America rappresenta il 42% del mercato globale di eCOA, eSource e Clinical Trials, riflettendo la sua leadership nella ricerca clinica e nelle tecnologie di prova digitali. La regione mantiene una forte presenza di importanti aziende farmaceutiche e fornitori di tecnologia. Beneficia di un’infrastruttura di ricerca ben consolidata e di quadri normativi che incoraggiano le valutazioni elettroniche degli esiti clinici. Consente una cattura, archiviazione e segnalazione efficienti dei dati in più siti di prova. L’alto investimento nella ricerca clinica e l’adozione precoce di piattaforme di prova innovative rafforzano la sua posizione di mercato. Gli sponsor si affidano a queste soluzioni per garantire la conformità, migliorare il coinvolgimento dei pazienti e aumentare l’efficienza operativa.
Europa Guida la Crescita Attraverso il Supporto Normativo e l’Integrazione Tecnologica
L’Europa detiene il 28% del mercato globale di eCOA, eSource e Clinical Trials, supportata da standard normativi armonizzati e crescente adozione di soluzioni cliniche digitali. La regione facilita la collaborazione transfrontaliera per studi multinazionali e promuove piattaforme elettroniche standardizzate. Permette agli sponsor di integrare il monitoraggio remoto dei pazienti, la segnalazione in tempo reale e la gestione centralizzata dei dati. Gli investimenti in prove centrate sul paziente e decentralizzate migliorano ulteriormente l’efficienza operativa. Rafforza la qualità delle prove, accelera i tempi di studio e supporta diverse aree terapeutiche in tutto il continente.
Asia-Pacifico in Emergenza come la Regione a Crescita Più Rapida con Ricerca Clinica in Espansione
L’Asia-Pacifico rappresenta il 20% del mercato globale di eCOA, eSource e Clinical Trials e mostra il più alto tasso di crescita tra tutte le regioni. La rapida espansione della ricerca clinica, l’esternalizzazione delle prove e l’aumento della produzione farmaceutica guidano l’adozione. Fornisce accesso a popolazioni di pazienti ampie e diversificate, consentendo un’esecuzione delle prove conveniente. Le piattaforme digitali supportano la raccolta dati in tempo reale, il monitoraggio remoto e la segnalazione semplificata. Le iniziative governative che promuovono l’adozione della tecnologia e la sicurezza dei dati rafforzano lo sviluppo del mercato. La regione offre sostanziali opportunità per la crescita a lungo termine e l’innovazione nelle prove cliniche.
Shape Your Report to Specific Countries or Regions & Enjoy 30% Off!
Analisi dei Principali Attori:
- Medidata Solutions, Inc.
- Oracle Corporation
- Veeva Systems Inc.
- Parexel International Corporation
- CRF Health (ora parte di Medidata)
- BioClinica, Inc.
- ERT (eResearchTechnology)
- ICON plc
- IQVIA Holdings, Inc.
- Signant Health
- YPrime, LLC
- ClinOne
Analisi Competitiva:
Il mercato di eCOA, eSource e Clinical Trials è altamente competitivo, guidato dalla presenza di fornitori tecnologici affermati e organizzazioni di ricerca a contratto che offrono soluzioni digitali avanzate. I principali attori si concentrano sull’innovazione dei prodotti, partnership strategiche e espansione geografica per rafforzare le posizioni di mercato. Si enfatizza l’integrazione di piattaforme basate su cloud, analisi guidate dall’IA e strumenti centrati sul paziente per differenziare le offerte. Le aziende investono in soluzioni scalabili che supportano studi decentralizzati, cattura dati in tempo reale e conformità normativa. Le strategie competitive includono acquisizioni, collaborazioni con sponsor farmaceutici e miglioramento dei portafogli di servizi per fornire una gestione completa degli studi. I leader di mercato danno priorità al supporto e alla formazione dei clienti per garantire un’adozione senza problemi delle loro piattaforme. Le aziende più piccole sfruttano soluzioni di nicchia o servizi specializzati per catturare segmenti di mercato mirati. Complessivamente, la competizione incoraggia l’innovazione continua, l’efficienza operativa migliorata e la qualità degli studi potenziata in tutto il mercato globale.
Sviluppi Recenti:
- In ottobre 2025, Medidata Solutions, Inc. ha ampliato la sua partnership con Sanofi per approfondire la collaborazione nello sviluppo clinico abilitato dall’IA.
- In marzo 2025, ICON plc ha formato una partnership con Mural Health Technologies, Inc. per migliorare l’esperienza dei partecipanti e dei siti di studi clinici, utilizzando la piattaforma di Mural Link per pagamenti, coordinamento dei viaggi e comunicazione, facilitando la gestione degli studi centrati sul paziente e riducendo le barriere alla partecipazione.
Copertura del Rapporto:
Il rapporto di ricerca offre un’analisi approfondita basata su Tipo di Soluzione, Implementazione, Uso Finale e Regione. Dettaglia i principali attori del mercato, fornendo una panoramica delle loro attività, offerte di prodotti, investimenti, flussi di entrate e applicazioni chiave. Inoltre, il rapporto include approfondimenti sull’ambiente competitivo, analisi SWOT, tendenze di mercato attuali, nonché i principali fattori trainanti e vincoli. Inoltre, discute vari fattori che hanno guidato l’espansione del mercato negli ultimi anni. Il rapporto esplora anche le dinamiche di mercato, gli scenari normativi e i progressi tecnologici che stanno plasmando l’industria. Valuta l’impatto dei fattori esterni e dei cambiamenti economici in ITALIA sulla crescita del mercato. Infine, fornisce raccomandazioni strategiche per i nuovi entranti e le aziende affermate per navigare nelle complessità del mercato.
Prospettive Future:
- L’adozione crescente di trial clinici decentralizzati e incentrati sul paziente espanderà la crescita del mercato.
- L’integrazione dell’intelligenza artificiale e delle analisi avanzate migliorerà il processo decisionale basato sui dati.
- Le piattaforme basate su cloud domineranno l’implementazione grazie alla scalabilità, flessibilità e accesso remoto.
- L’espansione nei mercati emergenti, specialmente nell’area Asia-Pacifico, creerà nuove opportunità di crescita.
- Il supporto normativo per le valutazioni elettroniche degli esiti clinici accelererà l’adozione di soluzioni digitali.
- Un maggiore focus sul monitoraggio in tempo reale e sull’integrità dei dati guiderà gli investimenti in soluzioni eCOA ed eSource.
- La collaborazione tra fornitori di tecnologia e aziende farmaceutiche migliorerà l’efficienza dei trial.
- La crescente domanda di dispositivi indossabili e applicazioni di salute mobile rafforzerà le capacità dei trial digitali.
- Lo sviluppo di piattaforme integrate che offrono una gestione completa dei trial guadagnerà terreno.
- L’innovazione continua in strumenti di automazione, reporting e conformità sosterrà l’espansione a lungo termine del mercato.




