体液采集与诊断市场概况:
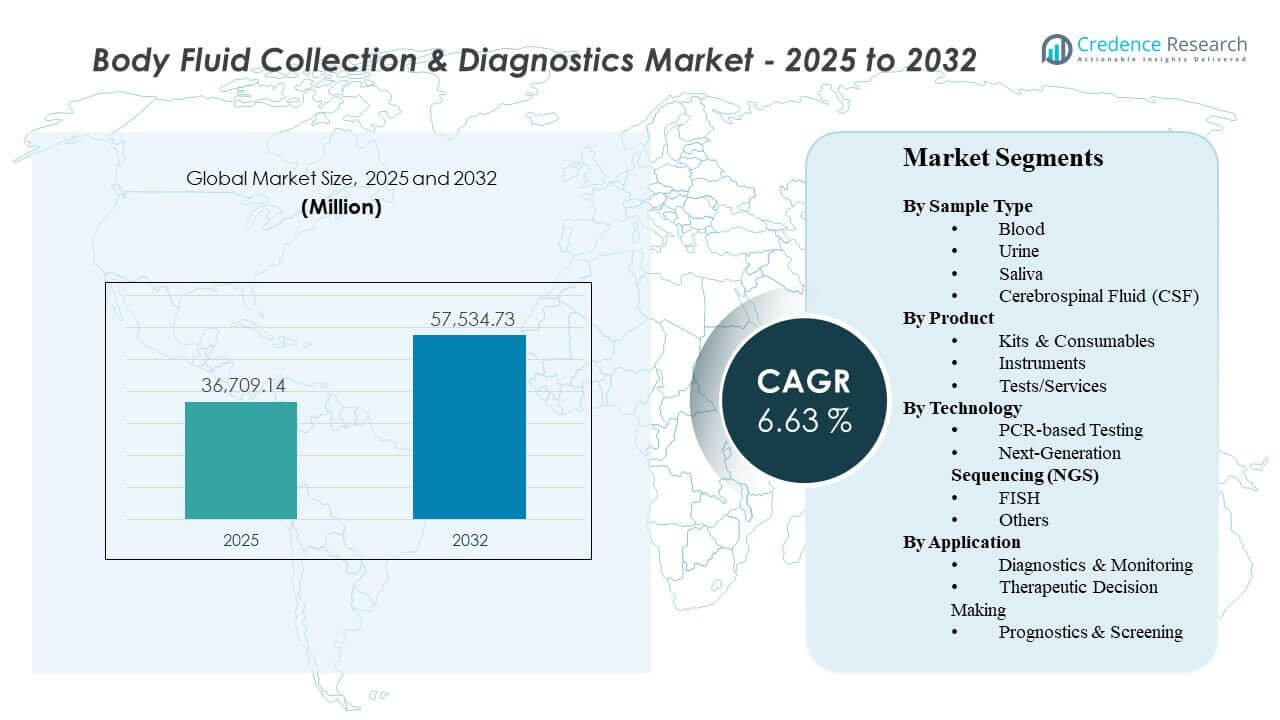
全球体液采集与诊断市场规模在2025年估计为367.0914亿美元,预计到2032年将达到575.3473亿美元,从2025年到2032年的复合年增长率为6.63%。需求因传染病、肿瘤学和慢性病监测的诊断测试量增加而得到加强,其中重复测试和更快的周转要求增加了标准化采集和测试工作流程的使用。北美和欧洲通过成熟的实验室网络和以报销为驱动的采用继续支撑收入,而亚太地区通过扩大访问、容量建设和更广泛的分子测试渗透贡献了增量增长。
| 报告属性 |
详细信息 |
| 历史时期 |
2020-2024 |
| 基准年 |
2025 |
| 预测期 |
2026-2032 |
| 2025年体液采集与诊断市场规模 |
367.0914亿美元 |
| 体液采集与诊断市场,复合年增长率 |
6.63% |
| 2032年体液采集与诊断市场规模 |
575.3473亿美元 |
主要市场趋势与见解
- 血液在样本类型使用中占据74.9%的份额(基准年参考),反映了主导的常规测试和监测路径。
- 试剂盒和耗材占66.8%的份额(基准年参考),得益于实验室间的重复采购和标准化工作流程。
- PCR检测占56.6%的份额(基准年参考),因其速度、可扩展性和针对性检测的广泛临床适配性而得以维持。
- 诊断与监测贡献了42.3%的份额(基准年参考),因为持续的患者管理增加了重复测试的频率。
- 亚太地区在参考的前景跟踪中与最快的区域扩张相关,得益于加速的诊断能力建设、更广泛的测试访问和先进分子工作流程的采用增加。
细分市场分析
体液采集与诊断市场需求集中在高通量工作流程中,样本采集、准备和测试必须在临床环境中保持可靠、快速和标准化。血液主导的测试继续占据主导地位,因为常规筛查、慢性病监测和与分子检测的广泛兼容性使得测试量结构性地高。提供者对可预测周转和较少的预分析错误的偏好支持了标准化耗材和验证协议的广泛使用。
技术采用仍然以PCR为基础,以满足传染病和特定肿瘤检测的需求,得益于成熟的仪器设备、明确的操作程序以及在常规实验室环境中的一致性能。同时,测序方法在需要全面分析和生物标志物深度的领域扩展,特别是在肿瘤学和复杂疾病特征化中。应用组合日益反映出向持续监测和与治疗相关决策的转变,其中检测频率和临床效用与护理路径紧密相连。
样本类型见解
在2024年,血液占据了74.9%的最大份额。血液采样领先,因为血液支持多种疾病领域的常规诊断,并被整合到标准化的采集和实验室处理路径中。与分子检测和生物标志物工作流程的广泛兼容性提高了在急性和慢性环境中的临床效用。高频次的监测和随访测试维持了检测量,强化了血液作为大多数实验室菜单中主要样本类型的地位。
产品见解
在2024年,试剂盒和耗材占据了66.8%的最大份额。试剂盒和耗材领先,因为经常性的采购与实验室和医院中的高检测吞吐量和常规补充周期相一致。预验证的试剂盒标准化了工作流程,减少了操作人员之间的变异性,提高了操作效率。供应链整合和优先供应商合同进一步支持了大型实验室网络中耗材量的集中。
技术见解
在2024年,基于PCR的测试占据了56.6%的最大份额。PCR的采用率最高,因为PCR提供快速周转、可扩展的吞吐量,并且非常适合目标检测要求。成熟的安装基础和训练有素的人员减少了去中心化和中心化实验室中PCR部署的操作摩擦。对可靠的常规分子检测的持续需求维持了PCR作为许多诊断工作流程中的主要模式。
应用见解
在2024年,诊断和监测占据了42.3%的最大份额。诊断和监测领先,因为重复测试嵌入在慢性疾病管理、治疗反应跟踪和随访协议中。临床路径偏好标准化的测试间隔,支持对采集和诊断服务的一致需求。扩展的生物标志物监测和纵向患者管理进一步强化了这一应用领域。
体液采集与诊断市场驱动因素
传染病和慢性病常规检测量的扩大
体液采集与诊断市场的增长得益于对需要反复监测的传染病和慢性病的诊断利用率增加。常规检测需求增加了对标准化采集流程的需求,以减少分析前的变异性。医院和实验室优先考虑可靠性和吞吐量,以管理日益增长的样本负荷。更高的检测频率增强了对消耗品和常规分子流程的持续需求。这也促使供应商简化采血、运输和样本处理步骤,以避免在高峰期出现瓶颈。
- 例如,罗氏报告称其 cobas 6800/8800 系统可在约 3 小时内生成多达 96 个结果,cobas 6800 每 24 小时的总吞吐量为 1,440 个结果,cobas 8800 每 24 小时的总吞吐量为 4,128 个结果,展示了常规高容量检测如何依赖于标准化和可扩展的工作流程。
分子诊断在临床工作流程中的广泛采用
临床路径越来越多地采用分子方法,以实现更快的检测、提高灵敏度和针对性分析,支持对采集和诊断解决方案的持续需求。由于速度和可扩展性,PCR 继续成为许多常规分子工作流程的核心。扩展的分子检测增加了对经过验证的样本准备和标准化试剂盒工作流程的要求。向分子采纳的转变加强了对仪器、试剂和工作流程优化的投资。随着检测范围超出参考实验室,易用性和与 LIS/LIMS 系统的互操作性成为更强的采购标准。
- 例如,Cepheid 表示其 GeneXpert 平台支持超过 20 项 FDA 批准或授权的测试,大多数 PCR 结果在不到 1 小时内交付,并且提供从 2 到 80 个模块的配置,具有 LIS 和 EMR 接口功能,突显了为什么分散的分子采纳倾向于可扩展和互操作的系统。
生物标志物引导的决策和监测的增长
治疗决策和监测路径越来越依赖于需要可靠样本采集和经过验证的诊断的生物标志物。肿瘤学和其他复杂病症推动了更高级检测方法的使用,在这些方法中,详细分析的临床价值更高。生物标志物的使用支持患者旅程中的重复检测周期,增加了整体检测量。这种动态有利于消耗品驱动的工作流程和基于服务的诊断产品。它还增加了对更高质量样本完整性控制的需求,以确保纵向结果的可比性。
实验室容量扩建和工作流程标准化举措
医疗系统扩展实验室容量并标准化操作程序,以减少周转时间并提高各站点的一致性。整合的实验室网络采用统一的试剂盒和协议来管理质量和采购效率。标准化减少了操作摩擦,支持可重复的性能,并改善了规模经济。这些变化加强了对采集设备、消耗品、仪器和检测服务的集成工作流程的需求。同时,自动化和集中采购有助于降低单位成本,同时提高多站点实验室网络的一致性。
体液采集与诊断市场挑战
体液采集与诊断市场的参与者面临着不同地区和应用中的报销覆盖和测试指南的差异,这可能会减缓新检测和先进模式的采用。在成熟市场中的价格压力增加了对效率、差异化和基于价值的证据的需求,以支持持续使用。操作限制,如劳动力短缺和培训需求,可能会限制某些环境中分子工作流程扩展的速度。
在前分析步骤中,质量和一致性风险仍然很大,样本处理、运输和加工的差异性可能会影响结果和重测率。关键试剂和消耗品的供应链中断可能会导致工作流程不稳定和库存限制。仪器、实验室信息系统和报告管道之间的数据集成挑战可能会减缓完整工作流程的现代化,特别是在分散的供应商环境中。
- 例如,BD表示其Vacutainer Barricor血浆采集管在4,000 RCF下离心3分钟是最佳的,而最低要求为1,800 RCF离心10分钟;而Sysmex报告称其Caresphere XQC从全球约13,000台分析仪接收IQC数据,并支持多达1,500台分析仪的同行组,结果可在几分钟内获得,说明供应商如何利用可测量的工作流程和连接性提升来解决一致性和集成差距。
体液采集与诊断市场趋势与机遇
体液采集与诊断市场趋势包括更广泛地采用高灵敏度方法进行目标检测和定量,同时逐步扩大在临床需求最强的地方进行全面分析的方法。随着成本下降和支持临床效用的证据增加,测序相关的工作流程正在扩展,特别是在肿瘤学和复杂疾病特征化中。提供者越来越优先考虑标准化工作流程,以减少变异性并改善周转时间,支持基于试剂盒的采用和集成的样本到结果路径。
在发展中的卫生系统中扩大测试访问以及向慢性和高风险患者群体的纵向监测转变中出现了机遇。生物标志物驱动的护理增长支持对与治疗选择和反应评估相关的常规和高级诊断的需求。将样本采集、准备和分析整合到统一工作流程中的合作伙伴关系可以通过降低操作复杂性和提高可靠性来改善采用。
- 例如,Natera报告称其Signatera结直肠癌项目在超过2,240名患者中生成了数据,显示Signatera阳性患者的复发风险高出35倍,并在复发前6个月检测到复发,而公司还表示,MRD检测和肿瘤基因组分析可以从单个样本中进行,以简化纵向监测工作流程。
区域见解
北美
北美体液采集与诊断市场收入预计在2025年占43.90%的份额,这得益于成熟的实验室网络、广泛的报销覆盖以及高诊断利用率。需求由大型供应商和实验室组织的既定分子检测能力和采购规模所支撑。检测菜单的持续创新和工作流程自动化支持医院和参考实验室的持续采用。
欧洲
欧洲预计在2025年占25.40%的份额,反映了广泛的诊断服务可及性和临床实验室的既定质量标准。采用仍然受到结构化筛查和监测路径的支持,同时主要市场的分子和精准诊断稳步现代化。采购框架和卫生系统成本控制增加了对标准化工作流程和可证明临床效用的重视。
亚太地区
亚太地区预计在2025年占23.10%的份额,这得益于诊断服务的扩展可及性、能力建设以及分子检测渗透率的提高。增长受到医疗投资增加、公共卫生倡议以及大型人口中心先进诊断更广泛可用性的支持。该地区的轨迹与基础设施和检测量扩展的成熟市场相比更快。
拉丁美洲
拉丁美洲预计在2025年占4.80%的份额,需求由实验室可及性的改善、诊断能力的逐步现代化以及主要城市医疗中心的检测需求增加所驱动。增长依赖于采购能力的扩展、供应链的加强以及标准化工作流程的更广泛采用。公共私营合作和参考实验室的扩展可以进一步增加检测的可用性。
中东和非洲
中东和非洲预计在2025年占2.80%的份额,反映了各国诊断基础设施成熟度的差异。需求增长受到医院网络投资、国家实验室升级和常规诊断可及性扩展的支持。采用率受到采购限制、劳动力能力以及实验室现代化进程的影响。
竞争格局
体液采集与诊断市场竞争由涵盖采集设备、样本准备、检测开发、仪器和数据集成的端到端工作流程覆盖所塑造。公司通过测试菜单的广度、工作流程标准化、自动化支持以及安装基础扩展策略来降低实验室的操作复杂性进行差异化。制造和分销的规模优势加强了对经常性消耗品需求的定位,而合作伙伴关系和平台生态系统有助于加强客户保留。
赛默飞世尔科技公司专注于广泛的产品组合,涵盖支持高通量实验室需求的仪器、试剂和分子诊断工作流程。赛默飞世尔科技公司强调标准化试剂盒和可扩展平台,帮助实验室在不同地点和操作人员之间保持一致的性能。赛默飞世尔科技公司继续加强工作流程整合,以提高常规和分子检测需求的周转时间和操作可靠性。
行业研究和增长报告包括市场竞争格局的详细分析以及关于主要公司的信息,包括:
对公司的定性和定量分析已进行,以帮助客户了解更广泛的商业环境以及主要行业参与者的优势和劣势。数据通过定性分析对公司进行分类为纯粹型、类别专注型、行业专注型和多元化;通过定量分析对公司进行分类为主导型、领先型、强势型、暂定型和弱势型。
Shape Your Report to Specific Countries or Regions & Enjoy 30% Off!
最新进展
- 2025年11月,F. Hoffmann-La Roche Ltd. 扩大了与Freenome的合作,在国际市场上商业化Freenome的血液癌症筛查技术,同时加深了围绕cfDNA检测和Roche的SBX测序平台的研发工作。
- 2025年7月,Thermo Fisher Scientific Inc. 在ADLM 2025上推出了LabLink360和Thermo Scientific MAS Max质量控制,旨在提高临床和诊断实验室的质量保证和工作流程效率。
- 2025年6月,Illumina, Inc. 宣布达成最终协议,以3.5亿美元现金加潜在里程碑收购SomaLogic及相关资产,称该交易将加强其在生物标志物发现和疾病概况分析方面的蛋白质组学和多组学战略。
- 2025年1月,Bio-Rad Laboratories, Inc. 参与了Geneoscopy的1.05亿美元C轮融资,公司表示Geneoscopy的ColoSense结直肠癌筛查测试设计用于与Bio-Rad的QXDx ddPCR平台配合使用,这是一个值得关注的诊断相关合作和商业化更新。
报告范围
| 报告属性 |
详细信息 |
| 2025年市场规模价值 |
367.0914亿美元 |
| 2032年收入预测 |
575.3473亿美元 |
| 增长率(CAGR) |
6.63%(2025–2032) |
| 基准年 |
2025 |
| 预测期 |
2026-2032 |
| 定量单位 |
亿美元 |
| 涵盖的细分市场 |
样本类型;产品;技术;应用 |
| 区域范围 |
北美、欧洲、亚太、拉丁美洲、中东和非洲 |
| 主要公司概况 |
Thermo Fisher Scientific Inc.; Bio-Rad Laboratories, Inc.; Illumina, Inc.; F. Hoffmann-La Roche Ltd.; QIAGEN N.V.; Becton, Dickinson and Company; Guardant Health, Inc.; Johnson & Johnson |
| 页数 |
335 |
细分
样本类型
产品
技术
- 基于PCR的检测
- 下一代测序(NGS)
- 荧光原位杂交(FISH)
- 其他
应用
地区




