Visión General del Mercado de Productos Medicinales de Terapias Avanzadas (ATMP) CDMO:
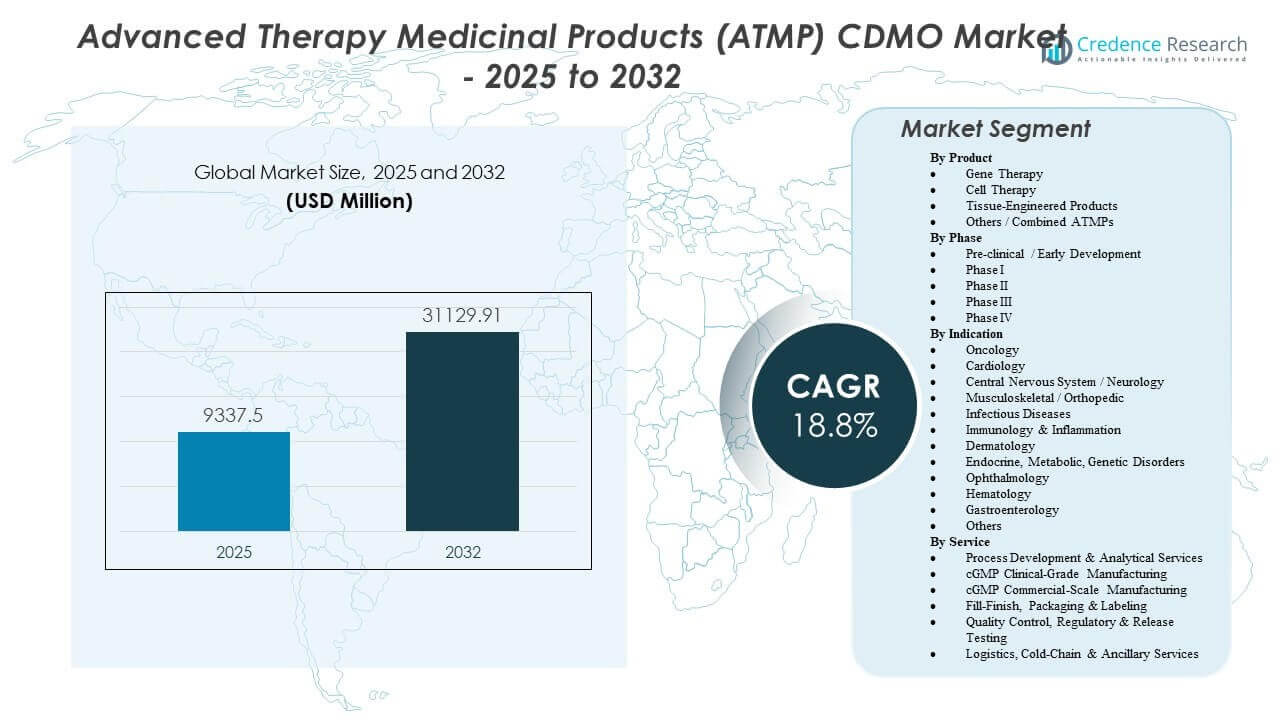
Se proyecta que el mercado de Productos Medicinales de Terapias Avanzadas (ATMP) CDMO crecerá de USD 9,337.5 millones en 2025 a un estimado de USD 31,129.91 millones para 2032, con una tasa de crecimiento anual compuesta (CAGR) del 18.8% de 2025 a 2032.
| ATRIBUTO DEL INFORME |
DETALLES |
| Período Histórico |
2020-2024 |
| Año Base |
2025 |
| Período de Pronóstico |
2026-2032 |
| Tamaño del Mercado de Productos Medicinales de Terapias Avanzadas (ATMP) CDMO 2025 |
USD 9,337.5 millones |
| Mercado de Productos Medicinales de Terapias Avanzadas (ATMP) CDMO, CAGR |
18.8% |
| Tamaño del Mercado de Productos Medicinales de Terapias Avanzadas (ATMP) CDMO 2032 |
USD 31,129.91 millones |
Perspectivas del Mercado de Productos Medicinales de Terapias Avanzadas (ATMP) CDMO:
- Fuertes líneas clínicas y la creciente comercialización de ATMPs impulsan la demanda de vectores virales, producción escalable de terapias celulares y servicios GMP especializados entre desarrolladores globales.
- Las altas necesidades de capital, la limitada experiencia interna y los complejos requisitos regulatorios siguen siendo restricciones clave que empujan a los patrocinadores hacia la subcontratación, pero crean desafíos operativos para las empresas más pequeñas.
- América del Norte lidera el mercado debido a un ecosistema biotecnológico maduro y capacidades avanzadas de fabricación, mientras que Europa sigue con fuertes marcos regulatorios y centros de vectores establecidos.
- Asia Pacífico emerge como la región de más rápido crecimiento, respaldada por la expansión de la infraestructura GMP, inversiones estratégicas y la creciente participación de jugadores biotecnológicos regionales en el desarrollo de ATMP.
Impulsores del Mercado de Productos Medicinales de Terapias Avanzadas (ATMP) CDMO
Rápida Expansión de Programas Clínicos de Terapia Celular y Génica en Áreas Terapéuticas Principales
Las líneas de terapia celular y génica continúan expandiéndose en oncología y enfermedades raras. Los patrocinadores avanzan más candidatos a ensayos de Fase II y Fase III. Este cambio aumenta la demanda de capacidad de fabricación de grado clínico y comercial. El mercado de Productos Medicinales de Terapias Avanzadas (ATMP) CDMO gana impulso a partir de esta profundidad de línea. Los desarrolladores requieren plataformas escalables de vectores virales y procesamiento celular. La preparación comercial exige sistemas de producción validados y reproducibles. Los contratos a largo plazo aseguran la continuidad del suministro para terapias aprobadas. Un fuerte apoyo de los inversores impulsa aún más la actividad de subcontratación.
- Por ejemplo, Novartis informó que más de 6,000 pacientes en todo el mundo fueron tratados con su terapia CAR-T Kymriah®, reflejando la creciente demanda clínica y comercial.
Access crucial information at unmatched prices!
Request your sample report today & start making informed decisions powered by Credence Research Inc.!
Download Sample
Capacidades Limitadas de Fabricación Interna Entre Empresas Biotecnológicas Emergentes
Muchas pequeñas y medianas empresas biotecnológicas carecen de infraestructura GMP. Las instalaciones de fabricación internas requieren un alto capital inicial y experiencia regulatoria. Los patrocinadores prefieren CDMOs con experiencia para gestionar flujos de trabajo de producción complejos. La subcontratación reduce el riesgo operativo y acelera los plazos de desarrollo. Los socios especializados proporcionan ingeniería de vectores y soporte analítico. La capacidad flexible permite a los clientes adaptarse a los resultados de los ensayos. Las asociaciones estratégicas mejoran la eficiencia en todas las etapas de desarrollo. Las estrategias ligeras en activos fortalecen la disciplina financiera.
Requisitos Regulatorios Complejos Y Estándares De Calidad Estrictos
Los productos ATMP enfrentan una estricta supervisión regulatoria en los principales mercados. La documentación exige validación detallada y datos de calidad. Los CDMOs ofrecen conocimiento regulatorio y preparación para inspecciones. Los patrocinadores confían en sistemas de calidad establecidos para reducir el riesgo de aprobación. Los procedimientos estandarizados apoyan un rendimiento consistente del producto. La experiencia en cumplimiento mejora la credibilidad con las autoridades. La mitigación de riesgos se convierte en central en las fases clínicas avanzadas. Los sólidos marcos de calidad impulsan la preferencia por la subcontratación.
Creciente Comercialización De Terapias Avanzadas Aprobadas
Las terapias génicas y celulares aprobadas se trasladan a programas de acceso más amplio para pacientes. El suministro comercial requiere una capacidad de producción estable y de alto volumen. Los CDMOs invierten en suites GMP ampliadas para satisfacer esta necesidad. Los patrocinadores priorizan socios de fabricación confiables. La transferencia de tecnología de la escala clínica a la comercial requiere experiencia. La gestión del ciclo de vida apoya una presencia sostenida en el mercado. Los compromisos post-aprobación aumentan la complejidad operativa. El crecimiento comercial sostiene la demanda a largo plazo de CDMOs.
- Por ejemplo, Catalent Cell & Gene Therapy escaló la fabricación de AAV para Zolgensma en su instalación de Harmans, Maryland, un sitio de 200,000 pies cuadrados equipado con 18 suites cGMP que apoyan los programas globales de terapia génica de Novartis.
Tendencias Del Mercado De CDMO De Productos Medicinales De Terapia Avanzada (ATMP)
Cambio Hacia Ofertas De Servicios Integrados De Extremo A Extremo
Los clientes buscan socios únicos que gestionen el desarrollo hasta la comercialización. Los CDMOs amplían sus carteras para incluir análisis, llenado-acabado y logística. Los modelos integrados mejoran la coordinación en las etapas del proyecto. Los patrocinadores reducen la fragmentación de proveedores y la carga de supervisión. Los servicios integrales fortalecen la retención de clientes. La integración vertical mejora la diferenciación competitiva. Las alianzas estratégicas a largo plazo reemplazan los contratos a corto plazo. Los modelos de servicio consolidados mejoran la eficiencia operativa.
Adopción De Automatización Y Plataformas De Fabricación Cerradas
La automatización mejora la precisión en la expansión celular y la producción de vectores. Los sistemas cerrados reducen el riesgo de contaminación y la variabilidad manual. La robótica mejora la reproducibilidad en lotes específicos de pacientes. Los controles digitales fortalecen la supervisión del proceso. La automatización reduce la dependencia de la intervención manual. Los sistemas estandarizados apoyan la producción alogénica escalable. Las actualizaciones tecnológicas impulsan una mayor utilización de las instalaciones. La eficiencia operativa mejora a través de herramientas de fabricación inteligente.
Diversificación Geográfica De La Huella De Fabricación
Las CDMOs se expanden en Asia Pacífico y en centros biotecnológicos emergentes. Las instalaciones regionales reducen el riesgo logístico y el tiempo de entrega. Los gobiernos apoyan la inversión en biotecnología a través de incentivos. La capacidad local fortalece la resiliencia de la cadena de suministro. Los patrocinadores buscan redes de producción diversificadas. Las asociaciones transfronterizas aceleran la entrada al mercado. La experiencia regional mejora la alineación regulatoria. La distribución geográfica mejora la competitividad global.
- Por ejemplo, FUJIFILM Diosynth Biotechnologies expandió sus capacidades globales al adquirir la instalación de biológicos a gran escala en Hillerød, Dinamarca, que incluye seis biorreactores de acero inoxidable de 15,000 litros y apoya la fabricación comercial de biológicos para clientes globales.
Inversión en Plataformas de Vectores y Células de Próxima Generación
La innovación en sistemas AAV y lentivirales aumenta la eficiencia. Las plataformas de producción de alto rendimiento mejoran la escalabilidad. Las terapias celulares alogénicas ganan atención para un uso más amplio. Los análisis avanzados mejoran la optimización de procesos. Los sistemas de biorreactores novedosos mejoran la consistencia del rendimiento. Las tecnologías de plataforma acortan los plazos de desarrollo. La mejora continua impulsa la diferenciación del servicio. El enfoque en la innovación asegura el potencial de crecimiento a largo plazo.
- Por ejemplo, AGC Biologics introdujo sus plataformas BravoAAV™ y ProntoLVV™, utilizando bioprocesos de suspensión escalables de hasta 2,000 L para AAV y 1,000 L para LVV para aumentar la eficiencia de producción de vectores. Estos sistemas plantillas reducen los plazos de preparación GMP a unos nueve meses, apoyando el avance más rápido de los programas de terapia génica.
Análisis de Desafíos del Mercado de Productos Medicinales de Terapias Avanzadas (ATMP) CDMO
Restricciones de Capacidad y Cuellos de Botella en la Producción de Vectores Virales
El suministro de vectores virales sigue siendo limitado en varias regiones. Los tiempos de entrega para plásmidos y materias primas extienden los plazos de los proyectos. La expansión de instalaciones requiere inspecciones regulatorias y validación. El mercado de Productos Medicinales de Terapias Avanzadas (ATMP) CDMO enfrenta presión para satisfacer la demanda urgente. La logística de cadena de frío añade complejidad a la distribución global. La escasez de mano de obra especializada ralentiza los planes de expansión. Los estándares de cumplimiento de calidad siguen siendo estrictos y requieren muchos recursos. Los patrocinadores esperan una rápida respuesta y un rendimiento constante. Equilibrar la demanda y la oferta sigue siendo un desafío clave.
Variabilidad Regulatoria y Altas Estructuras de Costos en los Mercados Globales
Las vías regulatorias difieren en las principales regiones. Los estándares de documentación exigen datos de validación extensivos. Las auditorías de cumplimiento requieren equipos de calidad dedicados. Los altos costos operativos impactan las estrategias de precios. Los desarrolladores más pequeños enfrentan presión de financiamiento durante los retrasos clínicos. La volatilidad de la moneda afecta los contratos transfronterizos. Los riesgos de propiedad intelectual complican las asociaciones. Las negociaciones de contratos implican términos detallados de reparto de riesgos. Estos factores aumentan la presión operativa sobre las CDMOs.
Oportunidades del Mercado de Productos Medicinales de Terapias Avanzadas (ATMP) CDMO
Expansión en Centros Biotecnológicos Emergentes y Plataformas de Manufactura Regionales
Los clústeres biotecnológicos emergentes invierten en infraestructura avanzada de biológicos. Los gobiernos ofrecen incentivos para atraer instalaciones de ATMP. El mercado de CDMO de Productos Medicinales de Terapia Avanzada (ATMP) puede expandirse a través de asociaciones regionales. La producción local reduce el riesgo y costo logístico. Los sitios GMP regionales apoyan un acceso más rápido para los pacientes. Las empresas conjuntas crean modelos de inversión compartida. Los programas de transferencia de tecnología fortalecen la experiencia local. La entrada temprana en nuevos mercados asegura contratos a largo plazo. La diversificación geográfica mejora la resiliencia.
Crecimiento De Plataformas Alogénicas Y Tecnologías De Vectores De Próxima Generación
Las terapias alogénicas buscan una producción escalable y disponible. Las líneas celulares estandarizadas simplifican los flujos de trabajo de fabricación. Las nuevas plataformas de vectores mejoran la eficiencia de transducción. Los sistemas de suspensión de alta capacidad aumentan la producción. Las analíticas avanzadas acortan los tiempos de liberación. Las tendencias de medicina personalizada apoyan la producción de terapias de nicho. Los gemelos digitales mejoran la optimización de procesos. Las inversiones estratégicas en innovación crean diferenciación. Estos desarrollos abren nuevas vías de ingresos para los CDMOs.
Análisis De Segmentación Del Mercado De CDMO De Productos Medicinales De Terapia Avanzada (ATMP):
Por Producto
El panorama de productos abarca terapia génica, terapia celular, productos de ingeniería tisular y ATMP combinados. En el mercado de CDMO de Productos Medicinales de Terapia Avanzada (ATMP), la terapia génica tiene una fuerte demanda debido a las plataformas basadas en vectores virales como AAV y sistemas lentivirales. Estos vectores apoyan las líneas de investigación de enfermedades raras y oncología. La terapia celular incluye formatos CAR-T, de células madre y no madre en modelos autólogos y alogénicos. Las terapias autólogas requieren fabricación específica para el paciente, mientras que las plataformas alogénicas buscan la escala. Los productos de ingeniería tisular dependen de andamios y matrices para la reparación estructural. Las terapias híbridas gen-celulares y los andamios biodegradables amplían las opciones de tratamiento complejo.
- Por ejemplo, WuXi Advanced Therapies lanzó la tecnología OXGENE TESSA™ para la fabricación de AAV, que elimina la necesidad de transfección de plásmidos y ha demostrado un aumento de 10 veces en el rendimiento de AAV en comparación con los métodos tradicionales de triple transfección.
Por Fase
Las fases de desarrollo van desde preclínica y desarrollo temprano hasta la Fase I a la Fase IV. Los programas en etapas tempranas se centran en el diseño de procesos y la validación de seguridad. Las fases I y II enfatizan la optimización de dosis y la producción controlada por lotes. La fase III requiere volúmenes mayores y sistemas GMP validados. La fase IV apoya el suministro post-aprobación y la gestión del ciclo de vida. Los patrocinadores aumentan la subcontratación en fases posteriores para asegurar la preparación comercial. La mitigación de riesgos y el cumplimiento regulatorio se vuelven críticos en etapas avanzadas. Los CDMOs alinean la capacidad con la progresión clínica.
Por Indicación
La oncología lidera debido a la alta adopción de terapias CAR-T y modificadas genéticamente. La cardiología y la neurología se expanden a través de programas regenerativos y basados en genes. Los segmentos musculoesqueléticos y ortopédicos utilizan andamios de ingeniería tisular para la reparación. Las enfermedades infecciosas y la inmunología aprovechan la edición genética y la modulación inmune. La dermatología y la oftalmología apoyan modelos de entrega génica localizada. Los trastornos endocrinos y genéticos dependen de la corrección génica duradera. La hematología sigue siendo central para la demanda de vectores virales y células madre. La gastroenterología y otras indicaciones crean necesidades de fabricación de nicho.
Por Servicio
Las ofertas de servicios abarcan desde el desarrollo de procesos hasta el soporte logístico. Los servicios de desarrollo de procesos y analíticos construyen flujos de trabajo escalables y conformes. La fabricación de grado clínico cGMP apoya ensayos en etapas tempranas y medias. La producción a escala comercial requiere instalaciones validadas y sistemas de suministro robustos. El llenado, acabado, empaquetado y etiquetado aseguran la integridad del producto. El control de calidad y las pruebas regulatorias mantienen los estándares de cumplimiento. La logística de cadena de frío gestiona materiales sensibles a la temperatura. Los modelos de servicio integrados mejoran la eficiencia a lo largo de los ciclos de desarrollo.
- Por ejemplo, los servicios Patheon de Thermo Fisher Scientific introdujeron el programa Quick to Care™, integrando la fabricación de sustancias y productos farmacéuticos con el empaquetado clínico para agilizar los flujos de trabajo de desarrollo temprano. La plataforma permite a las empresas biotecnológicas emergentes acelerar la preparación para el suministro clínico consolidando pasos que tradicionalmente requieren múltiples socios de servicio.
Segmentación:
Por Producto
- Terapia Génica
- Basada en Vectores Virales
- Terapia Celular
- CAR-T
- Células Madre
- No Células Madre
- Autóloga
- Alogénica
- Productos de Ingeniería de Tejidos
- Otros / ATMPs Combinados
- Gen-Célula Híbrido
- Andamios Biodegradables
Por Fase
- Pre-clínica / Desarrollo Temprano
- Fase I
- Fase II
- Fase III
- Fase IV
Por Indicación
- Oncología
- Cardiología
- Sistema Nervioso Central / Neurología
- Musculoesquelético / Ortopédico
- Enfermedades Infecciosas
- Inmunología & Inflamación
- Dermatología
- Trastornos Endocrinos, Metabólicos, Genéticos
- Oftalmología
- Hematología
- Gastroenterología
- Otros
Por Servicio
- Desarrollo de Procesos & Servicios Analíticos
- Fabricación de Grado Clínico cGMP
- Fabricación a Escala Comercial cGMP
- Llenado, Acabado, Empaquetado & Etiquetado
- Control de Calidad, Pruebas Regulatorias & de Liberación
- Logística, Cadena de Frío & Servicios Auxiliares
Por Región
- Norteamérica
- Europa
- Alemania
- Francia
- Reino Unido
- Italia
- España
- Resto de Europa
- Asia Pacífico
- China
- Japón
- India
- Corea del Sur
- Sudeste Asiático
- Resto de Asia Pacífico
- América Latina
- Brasil
- Argentina
- Resto de América Latina
- Oriente Medio y África
- Países del CCG
- Sudáfrica
- Resto de Oriente Medio y África
Análisis Regional:
Norteamérica posee la mayor participación del mercado de Productos Medicinales de Terapia Avanzada (ATMP) CDMO, representando casi el 45% de los ingresos globales. Un fuerte financiamiento biotecnológico y una alta concentración de desarrolladores de terapia génica y celular respaldan este dominio. Estados Unidos lidera el crecimiento regional con infraestructura GMP avanzada y vías regulatorias claras. Canadá apoya la expansión a través de subvenciones de investigación y colaboraciones académicas. Europa captura alrededor del 30% del mercado, impulsada por Alemania, el Reino Unido y Francia. Sólidos marcos de la EMA y programas de investigación transfronterizos fortalecen la capacidad regional. La región se beneficia de centros establecidos de vectores virales y procesamiento celular.
Asia Pacífico representa cerca del 20% de la participación global y registra la tasa de expansión más rápida. China y Japón invierten fuertemente en la producción de terapia génica y la innovación biotecnológica doméstica. Corea del Sur e India expanden la capacidad GMP a través de asociaciones públicas y privadas. Los incentivos gubernamentales fomentan la transferencia de tecnología y el desarrollo de instalaciones. Los menores costos operativos atraen contratos internacionales de subcontratación. La disponibilidad de mano de obra calificada mejora el rendimiento técnico. Los actores regionales buscan alianzas estratégicas con empresas biotecnológicas occidentales.
América Latina y Oriente Medio y África representan colectivamente casi el 5% del mercado. Brasil y México lideran la actividad en América Latina a través de iniciativas de investigación clínica. Los países del CCG invierten en infraestructura sanitaria avanzada y parques biotecnológicos. Sudáfrica apoya redes regionales de ensayos clínicos. La penetración del mercado sigue siendo limitada debido a brechas regulatorias y restricciones de financiamiento. Las asociaciones locales ayudan a las CDMO globales a ingresar a mercados emergentes. Las reformas políticas graduales apuntan a atraer inversión extranjera.
Shape Your Report to Specific Countries or Regions & Enjoy 30% Off!
Análisis de Jugadores Clave:
- Lonza Group
- Catalent Inc.
- Thermo Fisher Scientific (Patheon)
- AGC Biologics
- FUJIFILM Diosynth Biotechnologies
- Charles River Laboratories
- Oxford Biomedica PLC
- WuXi Advanced Therapies
- Minaris Regenerative Medicine
- Aldevron
- Samsung Biologics
- Rentschler Biopharma SE
- CELONIC Group
- Eurofins Scientific SE
- RoslinCT
- Andelyn Biosciences
- BlueReg
- CGT Catapult
- Curia Global Inc.
- Bio Elpida by Polyplus
Análisis Competitivo:
El mercado de Productos Medicinales de Terapia Avanzada (ATMP) CDMO presenta una combinación de fabricantes biotecnológicos especializados y CDMOs globales diversificados. Los líderes del sector se centran en la ampliación de vectores virales, la automatización de terapias celulares y modelos de servicio integrados. Las empresas invierten en la expansión de capacidad en América del Norte y Europa para asegurar contratos a largo plazo. Las adquisiciones estratégicas fortalecen la experiencia técnica en plataformas AAV y lentivirales. Las asociaciones con startups biotecnológicas crean acceso temprano a tuberías de alto potencial. Las empresas compiten en historial regulatorio, tiempo de respuesta y cumplimiento de calidad. Las ofertas integradas que abarcan desde el desarrollo de procesos hasta la fabricación comercial proporcionan una ventaja sólida. La competencia de precios sigue siendo secundaria a la capacidad técnica y la fiabilidad. La expansión de capacidad y la diversificación geográfica moldean el posicionamiento competitivo a largo plazo.
Desarrollos Recientes:
- En enero de 2024, Pluri, una empresa biotecnológica con sede en Israel, lanzó PluriCDMO, una nueva división que ofrece servicios de fabricación de terapias celulares como una organización de desarrollo y fabricación por contrato (CDMO), con una instalación GMP de 47,000 pies cuadrados.
- En enero de 2024, Charles River Laboratories International Inc. introdujo su oferta de plásmidos Rep/Cap listos para usar para agilizar los programas de terapia génica basados en virus adenoasociados (AAV).
Cobertura del Informe:
El informe de investigación ofrece un análisis en profundidad basado en Producto, Fase, Indicación, Servicio y Región. Detalla a los principales actores del mercado, proporcionando una visión general de su negocio, ofertas de productos, inversiones, fuentes de ingresos y aplicaciones clave. Además, el informe incluye perspectivas sobre el entorno competitivo, análisis FODA, tendencias actuales del mercado, así como los principales impulsores y restricciones. Asimismo, discute varios factores que han impulsado la expansión del mercado en los últimos años. El informe también explora la dinámica del mercado, los escenarios regulatorios y los avances tecnológicos que están dando forma a la industria. Evalúa el impacto de factores externos y cambios económicos globales en el crecimiento del mercado. Por último, proporciona recomendaciones estratégicas para nuevos entrantes y empresas establecidas para navegar por las complejidades del mercado.
Perspectivas Futuras:
- La demanda de plataformas integradas de desarrollo y fabricación comercial fortalecerá las asociaciones de externalización a largo plazo.
- La expansión de los programas de terapia celular alogénica mejorará la escalabilidad y la estandarización en los sitios de producción.
- La automatización y las tecnologías de sistemas cerrados mejorarán la consistencia de los lotes y reducirán el riesgo operativo.
- La innovación en vectores virales aumentará la eficiencia de transducción y mejorará los rendimientos de fabricación.
- Las alianzas estratégicas entre CDMOs y startups biotecnológicas acelerarán las transiciones de programas en etapas tempranas.
- Los centros de fabricación regionales en Asia Pacífico atraerán contratos de suministro clínico transfronterizos.
- Los análisis avanzados y los sistemas de calidad digital apoyarán el cumplimiento regulatorio y la integridad de los datos.
- La inversión en instalaciones GMP modulares proporcionará capacidad flexible para líneas de productos múltiples.
- El crecimiento en las líneas de enfermedades raras y oncología sostendrá contratos de servicios de alto valor.
- La logística de cadena de frío y las redes de distribución especializadas se expandirán para apoyar la comercialización global.




