Markedsoversigt
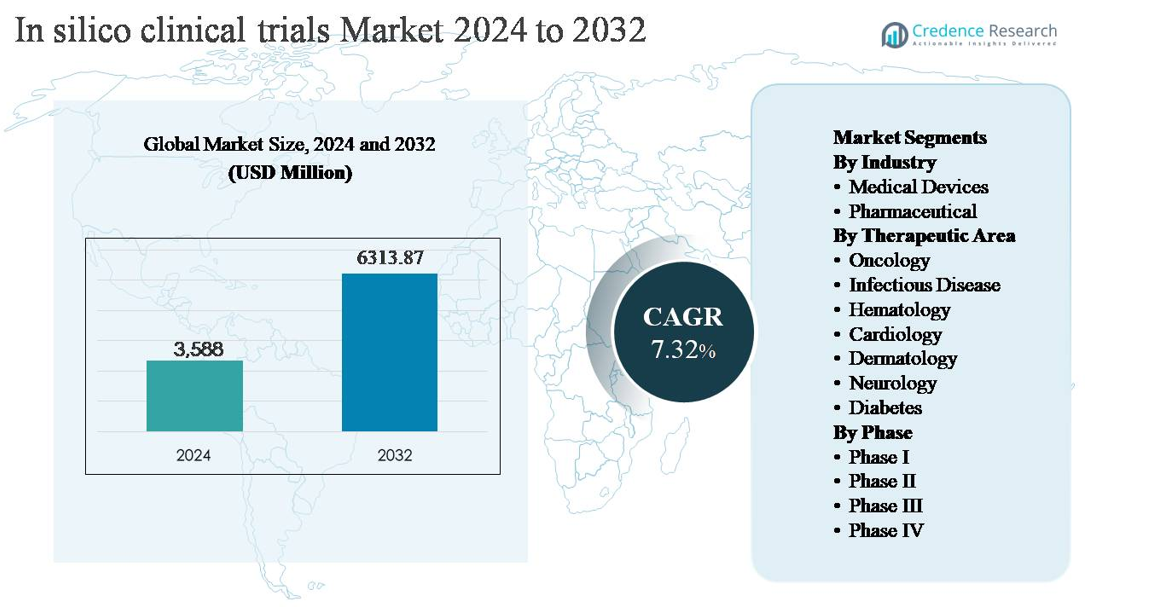
Markedet for in silico kliniske forsøg blev vurderet til USD 3.588 millioner i 2024 og forventes at nå USD 6.313,87 millioner i 2032, med en sammensat årlig vækstrate (CAGR) på 7,32% i prognoseperioden.
| RAPPORT ATTRIBUTE |
DETALJER |
| Historisk periode |
2020-2023 |
| Basisår |
2024 |
| Prognoseperiode |
2025-2032 |
| In Silico Kliniske Forsøg Markedsstørrelse 2024 |
USD 3.588 millioner |
| In Silico Kliniske Forsøg Marked, CAGR |
7,32% |
| In Silico Kliniske Forsøg Markedsstørrelse 2032 |
USD 6.313,87 millioner |
Markedet for in silico kliniske forsøg ledes af en gruppe specialiserede teknologi- og life-science-analysevirksomheder, der leverer avancerede modellerings-, simulerings- og AI-drevne platforme. Nøglespillere som Dassault Systèmes SE, Certara, Inc., Insilico Medicine, Inc., GNS Healthcare Inc., Novadiscovery SAS, InSilicoTrials, Immunetrics Inc., Nuventra Pharma Sciences, Abzena Ltd., og The AnyLogic Company konkurrerer på forudsigelsesnøjagtighed, reguleringsmæssig validering og integration på tværs af lægemiddel- og enhedsudviklingsarbejdsgange. Disse virksomheder støtter farmaceutiske og medicinske enhedssponsorer i at optimere forsøgsdesign, dosisvalg og patientstratificering. Nordamerika forbliver det førende regionale marked, der tegner sig for cirka 38% af den globale markedsandel, drevet af stærk F&U-investering, tidlig teknologiadoption og understøttende reguleringsengagement.
Markedsindsigt
- Markedet for in silico kliniske forsøg blev vurderet til USD 3.588 millioner i 2024 og forventes at nå USD 6.313,87 millioner i 2032, med en CAGR på 7,32% i prognoseperioden.
- Markedsvæksten drives primært af stigende omkostninger og kompleksitet ved konventionelle kliniske forsøg, hvilket får farmaceutiske og medicinske enhedsvirksomheder til at vedtage simuleringsbaserede tilgange for at reducere udviklingstidslinjer, optimere protokoller og forbedre forsøgs succesrater, hvor den farmaceutiske sektor har den dominerende andel på grund af omfattende lægemiddel F&U-aktivitet.
- Vigtige markedstendenser inkluderer stigende integration af AI, maskinlæring og digital tvilling-teknologier, sammen med udvidet brug inden for onkologi og kardiologi, hvor onkologi forbliver den førende terapeutiske område-segment på grund af høje forsøgsfejlrater og efterspørgsel efter personlig behandlingsmodellering.
- Det konkurrenceprægede landskab er præget af specialiserede aktører, der tilbyder avancerede modelleringsplatforme, med konkurrence fokuseret på forudsigelsesnøjagtighed, reguleringsaccept og end-to-end arbejdsgangsintegration gennem strategiske samarbejder med life science-virksomheder.
- Regionalt fører Nordamerika med cirka 38% markedsandel, efterfulgt af Europa med 28% og Asien og Stillehavsområdet med 22%, mens Latinamerika og Mellemøsten & Afrika tilsammen tegner sig for den resterende andel, hvilket afspejler fremvoksende adoption.
Access crucial information at unmatched prices!
Request your sample report today & start making informed decisions powered by Credence Research Inc.!
Download Sample
Markedssegmenteringsanalyse:
Efter Industri:
Det farmaceutiske segment repræsenterer den dominerende andel af markedet for in silico kliniske forsøg og står for størstedelen af den samlede indtægt på grund af dets omfattende anvendelse inden for lægemiddelopdagelse og kliniske udviklingsprocesser. Farmaceutiske virksomheder anvender i stigende grad in silico-modellering til at optimere dosisvalg, forudsige effektivitet og reducere fejl i sene faser af forsøg, især i komplekse biologiske og småmolekylære programmer. Segmentet for medicinsk udstyr, selvom det er mindre, udvider sig støt, da regulerende myndigheder accepterer beregningsmæssige beviser for enhedens sikkerhed og ydeevne. Dominansen af farmaceutiske produkter er drevet af høj FoU-intensitet, stigende forsøgsomkostninger og stærkt pres for at forkorte udviklingstidslinjer.
- For eksempel har Novartis offentligt dokumenteret brugen af QSP-platforme til at simulere lægemiddel-sygdomsinteraktioner på tværs af virtuelle kohorter, der overstiger 10.000 modellerede patienter til immunologi- og onkologiprogrammer, hvilket muliggør evaluering af flere doseringsregimer og tidsplaner før studier på mennesker.
Efter Terapeutisk Område:
Onkologi er det dominerende terapeutiske område på markedet for in silico kliniske forsøg og har den største markedsandel på grund af den høje kompleksitet af kræftbiologi og behovet for personlig behandlingsmodellering. Virtuelle tumorsimuleringer, biomarkørstratificering og responsforudsigelsesværktøjer anvendes bredt til at optimere forsøgsdesign og patientudvælgelse. Infektionssygdomme følger, understøttet af udbrudsmodellering og vaccineudviklingsapplikationer, mens kardiologi og neurologi viser stigende adoption gennem organ-niveau simuleringer. Onkologilederskab er drevet af høje kliniske fejlrater, efterspørgsel efter præcisionsmedicin og betydelige onkologi FoU-udgifter.
- For eksempel har Roche og dets Genentech-division rapporteret brugen af kvantitative systemfarmakologimodeller, der integrerer genomiske og farmakologiske data fra mere end 11.000 tumorprøver afledt fra The Cancer Genome Atlas til at simulere pathway-hæmning og forudsige responsvariabilitet på tværs af virtuelle onkologikohorter.
Efter Fase:
Fase II udgør det dominerende fasesegment på markedet for in silico kliniske forsøg og fanger den højeste markedsandel, da sponsorer i stigende grad stoler på simuleringer for at evaluere effektivitetssignaler og forfine forsøgsendepunkter. In silico-tilgange er særligt værdifulde i Fase II for at reducere antallet af patienter og forbedre go/no-go-beslutninger før dyre sene faseforsøg. Fase I-adoption understøttes af sikkerheds- og dosisfindingsimuleringer, mens Fase III-brug vokser for virtuel kohortesupplementering. Dominansen af Fase II er drevet af dens kritiske rolle i reduktion af frafald og omkostningsoptimering.
Vigtige Vækstdrivere
Stigende Omkostninger og Kompleksitet ved Konventionelle Kliniske Forsøg
Stigende omkostninger, forlængede tidslinjer og høje fejlrater i traditionelle kliniske forsøg er en primær driver, der fremskynder adoptionen af in silico kliniske forsøg. Sene fase kliniske studier kræver store patientkohorter, multisite-koordinering og omfattende reguleringsmæssig overvågning, hvilket betydeligt øger udviklingsudgifterne. In silico-tilgange gør det muligt for sponsorer at simulere patientreaktioner, forfine inklusionskriterier og optimere doseringsstrategier, før fysiske forsøg begynder. Disse kapaciteter hjælper med at reducere unødvendige protokolændringer og mindske byrden ved patientrekruttering. Ved at identificere ineffektive kandidater tidligere kan udviklere omdirigere ressourcer mere effektivt. Det voksende pres på farmaceutiske og medicinske udstyrsfirmaer for at kontrollere FoU-udgifter, samtidig med at innovationsoutput opretholdes, fortsætter med at skubbe in silico-forsøg ind i mainstream udviklingsstrategier.
- For eksempel har AstraZeneca afsløret brugen af modelinformerede lægemiddeludviklingsrammer, der integrerer PBPK og sygdomsprogressionsmodeller til at simulere kliniske resultater på tværs af virtuelle kohorter, der overstiger 5.000 patienter, hvilket muliggør protokolforfining og dosisoptimering inden igangsættelse af fase III-forsøg.
Fremskridt inden for Computational Modeling og Kunstig Intelligens
Hurtige forbedringer inden for computervidenskab, maskinlæring og digitale tvillingeteknologier udvider betydeligt omfanget og pålideligheden af in silico kliniske forsøg. Avancerede algoritmer kan nu integrere genomiske, proteomiske og fysiologiske datasæt for at skabe meget forudsigelige virtuelle patientpopulationer. Disse modeller giver forskere mulighed for at teste flere forsøgs-scenarier samtidigt, hvilket forbedrer nøjagtigheden i resultatforudsigelse. AI-drevne platforme forbedrer også adaptive forsøgsdesign ved kontinuerligt at lære fra indkommende data. Efterhånden som modellernes præcision forbedres, styrkes den regulatoriske tillid til simuleringsbaseret evidens. Konvergensen af højtydende computing og AI muliggør bredere anvendelse af in silico metoder på tværs af terapeutiske områder og forsøgsfaser.
- For eksempel har Siemens Healthineers avanceret digitale tvillingeteknologier gennem sine computermodeller af hjertet, som er bygget ved hjælp af millioner af finite elementer til at simulere hjerte-elektrofysiologi og hæmodynamik under forskellige patologiske tilstande, hvilket understøtter virtuel evaluering af kardiovaskulære terapier og interventioner.
Voksende Regulatorisk Accept og Støttende Rammer
Reguleringsmyndigheder anerkender i stigende grad in silico evidens som en komplementær komponent i klinisk evaluering, hvilket driver markedsvækst. Regulatorisk vejledning opfordrer nu til brugen af computermodellering til enhedsvalidering, dosisoptimering og risikovurdering. In silico forsøg hjælper med at understøtte regulatoriske indsendelser ved at give robuste mekanistiske indsigter og reducere afhængigheden af omfattende menneskelig testning. Dette skift er særligt tydeligt i udviklingen af medicinsk udstyr, hvor virtuel testning kan demonstrere sikkerhed på tværs af flere scenarier. Efterhånden som regulatorer fortsætter med at formalisere standarder for modelvalidering og rapportering, øges industriens tillid til simuleringsdrevet udvikling, hvilket yderligere accelererer adoptionen.
Vigtige Tendenser & Muligheder
Udvidelse af Personlig og Præcisionsmedicin Applikationer
In silico kliniske forsøg er i stigende grad tilpasset væksten af personlig medicin, hvilket skaber betydelige muligheder for markedsudvidelse. Virtuel patientmodellering muliggør stratificering baseret på genetiske, fænotypiske og biomarkørdata, hvilket understøtter mere målrettet terapeutisk udvikling. Denne tilgang giver udviklere mulighed for at simulere behandlingsrespons på tværs af forskellige subpopulationer, hvilket forbedrer forsøgets effektivitet og resultater. Præcisionsmodellering er særligt værdifuld inden for onkologi og sjældne sygdomme, hvor patientheterogenitet begrænser traditionelle forsøgsdesign. Efterhånden som personlige terapier vinder frem, forventes efterspørgslen efter sofistikerede in silico platforme, der er i stand til at forudsige individuelle responser, at stige støt.
- For eksempel har Moderna udnyttet in silico neoantigen udvælgelsesplatforme til sine personlige kræftvaccineprogrammer ved at bruge beregningsmæssige pipelines til at prioritere op til 34 patient-specifikke neoantigen-sekvenser pr. individuel tumorprofil inden klinisk fremstilling.
Integration med virkelige data og digitale sundhedsteknologier
Integrationen af virkelige data fra elektroniske patientjournaler, bærbare enheder og digitale sundhedsplatforme repræsenterer en vigtig vækstmulighed for in silico kliniske forsøg. Kombinationen af simuleringsmodeller med virkelige beviser forbedrer forudsigelsesnøjagtigheden og understøtter post-markedsovervågning og adaptive forsøgsdesigns. Denne trend muliggør kontinuerlig modelraffinering og langsigtet resultatvurdering ud over kontrollerede forsøgsindstillinger. Farmaceutiske sponsorer ser i stigende grad denne integration som en vej til at forbedre regulatoriske indsendelser og livscyklusstyringsstrategier. Den voksende tilgængelighed af strukturerede sundhedsdata forventes at styrke denne mulighed yderligere.
- For eksempel kombinerede Verily’s Project Baseline output fra bærbare sensorer, kliniske målinger og EHR-data fra 10.000 tilmeldte deltagere for at generere dybt fænotypede longitudinelle datasæt, der blev brugt til sygdomsprogressionsmodellering og virtuel kohortegenerering.
Vigtige udfordringer
Modelvalidering, standardisering og begrænsninger i datakvalitet
Sikring af nøjagtighed, reproducerbarhed og klinisk relevans af in silico modeller forbliver en stor udfordring. Variabilitet i datakilder, antagelser og modelleringsteknikker kan føre til inkonsistente resultater på tværs af platforme. Manglen på standardiserede valideringsrammer komplicerer regulatorisk gennemgang og begrænser sammenlignelighed på tværs af studier. Højkvalitets, repræsentative datasæt er essentielle for pålidelige simuleringer, men adgangen til omfattende kliniske og biologiske data er fortsat ujævn. At tackle disse udfordringer kræver samarbejde mellem industri, regulatorer og teknologileverandører for at etablere fælles standarder og bedste praksis.
Begrænset teknisk ekspertise og integrationsbarrierer
Effektiv implementering af in silico kliniske forsøg kræver specialiseret ekspertise inden for beregningsbiologi, datavidenskab og klinisk forskning, som mange organisationer mangler. Integration af simuleringsplatforme i eksisterende F&U-arbejdsgange kan være komplekst og ressourcekrævende. Modstand mod forandring inden for etablerede kliniske udviklingsteams bremser yderligere adoption. Derudover præsenterer det organisatoriske udfordringer at tilpasse tværfaglige interessenter omkring modeldrevet beslutningstagning. At overvinde disse barrierer vil kræve målrettet arbejdsstyrkeudvikling, forbedrede brugervenlige platforme og stærkere tværfunktionelt samarbejde.
Regional analyse
Nordamerika
Nordamerika dominerer markedet for in silico kliniske forsøg og tegner sig for cirka 38% af den globale markedsandel. Regionen drager fordel af avanceret sundhedsinfrastruktur, stærk farmaceutisk F&U-investering og tidlig adoption af beregningsmodellering og AI-drevne forsøgsplatforme. USA fører regional vækst på grund af tilstedeværelsen af store farmaceutiske virksomheder, specialiserede softwareleverandører og akademiske forskningsinstitutioner, der aktivt bruger virtuelle patientsimuleringer. Gunstig regulatorisk vejledning, der understøtter modellering og simulering i lægemiddel- og enhedsudvikling, styrker yderligere adoption. Høje kliniske forsøgsomkostninger og stærk efterspørgsel efter effektivitet fortsætter med at styrke Nordamerikas førerposition.
Europa
Europa har næsten 28% af den globale andel af in silico kliniske forsøg, understøttet af stærk regulatorisk tilpasning, offentlige-private forskningssamarbejder og voksende accept af digitale beviser i klinisk udvikling. Lande som Tyskland, Storbritannien og Frankrig er nøglebidragydere, drevet af robuste biomedicinske forskningsøkosystemer og stigende investeringer i personlig medicin. Europæiske regulatorer støtter i stigende grad modellering og simulering til sikkerhedsvurdering og dosisoptimering, især inden for medicinsk udstyr. Regionens fokus på omkostningsbegrænsning, etisk forsøgsdesign og innovation inden for computervidenskab opretholder en stabil markedsudvidelse.
Asien og Stillehavsområdet
Asien og Stillehavsområdet står for cirka 22% af den globale markedsandel og repræsenterer det hurtigst voksende regionale marked for in silico kliniske forsøg. Hurtig udvidelse af farmaceutisk produktion, stigende klinisk forsøgsaktivitet og stigende investeringer i digital sundhed understøtter adoptionen. Kina, Japan, Sydkorea og Indien er nøglemarkeder, drevet af voksende computerkapaciteter og ekspanderende bioteksektorer. Regeringer i hele regionen fremmer AI og datadrevet sundhedsinnovation, hvilket accelererer brugen af virtuelle forsøgsmetoder. Stigende kliniske forsøgsvolumener og pres for at reducere udviklingstidslinjer fortsætter med at drive stærk regional vækstmomentum.
Latinamerika
Latinamerika repræsenterer omkring 7% af det globale in silico kliniske forsøg marked, med gradvis adoption drevet af ekspanderende klinisk forskningsaktivitet og forbedring af sundhedsinfrastrukturen. Brasilien og Mexico er de primære bidragydere, understøttet af voksende farmaceutisk outsourcing og regional forsøgsdeltagelse. Mens adoptionen forbliver begrænset sammenlignet med udviklede regioner, opmuntrer stigende bevidsthed om omkostningseffektive forsøgsmodeller interessen for in silico tilgange. Regional vækst understøttes af samarbejder med globale sponsorer, der søger optimerede forsøgsdesigns. Fortsatte investeringer i digitale sundhedskapaciteter forventes at styrke markedsindtrængningen over tid.
Mellemøsten & Afrika
Mellemøsten & Afrika regionen har cirka 5% af den globale markedsandel, hvilket afspejler tidlig adoption af in silico kliniske forsøg. Vækst understøttes af moderniseringsinitiativer inden for sundhedsvæsenet, især i Gulf Cooperation Council-landene, der investerer i digital sundhed og avanceret forskningsinfrastruktur. Sydafrika bidrager også gennem ekspanderende kliniske forskningskapaciteter. Begrænset adgang til høj-kvalitets datasæt og teknisk ekspertise begrænser i øjeblikket adoptionen. Dog forventes stigende deltagelse i globale kliniske forsøg og stigende interesse i AI-drevne sundhedsløsninger gradvist at forbedre den regionale markeds tilstedeværelse.
Markedssegmenteringer:
Efter Industri
- Medicinsk Udstyr
- Farmaceutisk
Efter Terapeutisk Område
- Onkologi
- Infektionssygdomme
- Hæmatologi
- Kardiologi
- Dermatologi
- Neurologi
- Diabetes
Efter Fase
- Fase I
- Fase II
- Fase III
- Fase IV
Efter Geografi
- Nordamerika
- Europa
- Tyskland
- Frankrig
- Storbritannien
- Italien
- Spanien
- Resten af Europa
- Asien og Stillehavsområdet
- Kina
- Japan
- Indien
- Sydkorea
- Sydøstasien
- Resten af Asien og Stillehavsområdet
- Latinamerika
- Brasilien
- Argentina
- Resten af Latinamerika
- Mellemøsten & Afrika
- GCC-lande
- Sydafrika
- Resten af Mellemøsten og Afrika
Konkurrencelandskab
Konkurrencelandskabet for markedet for in silico kliniske forsøg er kendetegnet ved en blanding af specialiserede simulationssoftwareleverandører, AI-drevne analysefirmaer og etablerede life science-teknologivirksomheder. Markedsdeltagere konkurrerer på dybden af biologisk modellering, forudsigelsesnøjagtighed og evnen til at integrere multi-omics og virkelige data i virtuelle patientsimulationer. Førende aktører fokuserer på at udvide platformkapaciteter på tværs af flere terapeutiske områder og kliniske faser, samtidig med at de styrker reguleringsmæssigt tilpassede valideringsrammer. Strategiske samarbejder med farmaceutiske virksomheder, medicinsk udstyrsproducenter og akademiske institutioner er almindelige, hvilket muliggør fælles udvikling af sygdomsspecifikke modeller. Leverandører investerer også kraftigt i kunstig intelligens, cloud-baserede arkitekturer og digitale tvillingeteknologier for at forbedre skalerbarhed og brugervenlighed. Konkurrencemæssig differentiering afhænger i stigende grad af modelgennemsigtighed, regulatorisk accept og end-to-end workflow-integration, hvilket positionerer innovation og troværdighed som kritiske succesfaktorer.
Shape Your Report to Specific Countries or Regions & Enjoy 30% Off!
Nøglespilleranalyse
- Dassault Systemes SE
- Insilico Medicine, Inc.
- Certara, Inc.
- GNS Healthcare Inc.
- Novadiscovery SAS
- InSilicoTrials
- The AnyLogic Company
- Immunetrics Inc.
- Abzena Ltd.
- Nuventra Pharma Sciences
Seneste Udviklinger
- I januar 2025 avancerede Insilico Medicine sin AI-aktiverede in silico kliniske forsøgsramme for at støtte fase II-udviklingen af INS018_055, et anti-fibrotisk lille molekyle. Virksomheden anvendte multimodale simulationsmodeller trænet på over 1 milliard biologiske og kemiske datapunkter, der integrerer transkriptomiske signaturer og farmakokinetiske parametre for at forudsige dosisrespons og responderstratificering før patientindskrivning. In silico-arbejdsgangen simulerede behandlingsresultater på tværs af flere tusinde virtuelle patienter, hvilket understøttede protokoloptimering og biomarkør-informeret kohortevalg.
- I oktober 2024 udvidede Dassault Systèmes sin Living Heart Project-simulationsportefølje for at støtte in silico klinisk evidensgenerering for kardiovaskulære lægemidler og enheder. Den opdaterede platform muliggør elektrofysiologiske og hæmodynamiske simulationer ved hjælp af hjertemodeller, der indeholder over 5 millioner endelige elementer, hvilket tillader virtuel evaluering af lægemiddelinduceret arytmirisiko og enhed-væv interaktioner på tværs af patient-specifikke anatomier. Platformen integrerer kliniske billeddata, herunder CT- og MRI-input med rumlige opløsninger under 1 mm, hvilket muliggør realistiske virtuelle kohorter til reguleringsmæssige simulationsstudier.
- I juli 2024 frigav Certara en opgraderet version af sin Simcyp™ fysiologisk baserede farmakokinetiske (PBPK) simulator, der er bredt anvendt til in silico kliniske forsøg og regulatoriske indsendelser. Opdateringen udvidede virtuelle populationsbiblioteker til at inkludere mere end 40 foruddefinerede fysiologiske populationsmodeller, der dækker pædiatriske, geriatriske, nyreinsufficiens og leverinsufficiens scenarier. Hver model inkorporerer over 20 organkompartimenter med alders- og sygdomsspecifikke fysiologiske parametre, hvilket muliggør virtuel vurdering af dosering, lægemiddel-lægemiddel interaktioner og eksponeringsvariabilitet før klinisk udførelse.
Rapportdækning
Forskningsrapporten tilbyder en dybdegående analyse baseret på Industri, Terapeutisk område, Fase og Geografi. Den beskriver førende markedsaktører og giver et overblik over deres forretning, produkttilbud, investeringer, indtægtskilder og nøgleapplikationer. Derudover indeholder rapporten indsigt i det konkurrenceprægede miljø, SWOT-analyse, aktuelle markedstendenser samt de primære drivkræfter og begrænsninger. Desuden diskuterer den forskellige faktorer, der har drevet markedsudvidelse i de seneste år. Rapporten udforsker også markedsdynamik, regulatoriske scenarier og teknologiske fremskridt, der former industrien. Den vurderer virkningen af eksterne faktorer og globale økonomiske ændringer på markedsvækst. Endelig giver den strategiske anbefalinger til nye aktører og etablerede virksomheder for at navigere i markedets kompleksiteter.
Fremtidsperspektiver
- Anvendelsen af in silico kliniske forsøg vil fortsætte med at udvide sig, da sponsorer søger at reducere udviklingstider og forbedre forsøgets effektivitet.
- Computermodellering vil spille en større rolle i tidlig beslutningstagning på tværs af lægemiddel- og medicinsk udstyrsudvikling.
- Kunstig intelligens og maskinlæring vil yderligere forbedre forudsigelsesnøjagtighed og adaptive forsøgsdesignmuligheder.
- Regulatorisk accept af simuleringsbaseret evidens vil styrkes, hvilket understøtter bredere anvendelse i indsendelser og godkendelser.
- Integration med data fra den virkelige verden vil forbedre langtidsforudsigelse af resultater og evaluering efter markedet.
- Initiativer inden for personlig medicin vil drive efterspørgslen efter patient-specifikke og biomarkør-drevne virtuelle forsøg.
- Onkologi og kardiologi vil forblive førende terapeutiske områder for avancerede in silico applikationer.
- Cloud-baserede platforme vil forbedre skalerbarhed og global tilgængelighed af simuleringsværktøjer.
- Samarbejde mellem teknologileverandører, medicinalvirksomheder og regulatorer vil intensiveres.
- Standardisering af modelleringsrammer vil forbedre troværdighed, interoperabilitet og industridækkende anvendelse.




