Aperçu du marché des produits médicinaux de thérapie avancée (ATMP) CDMO :
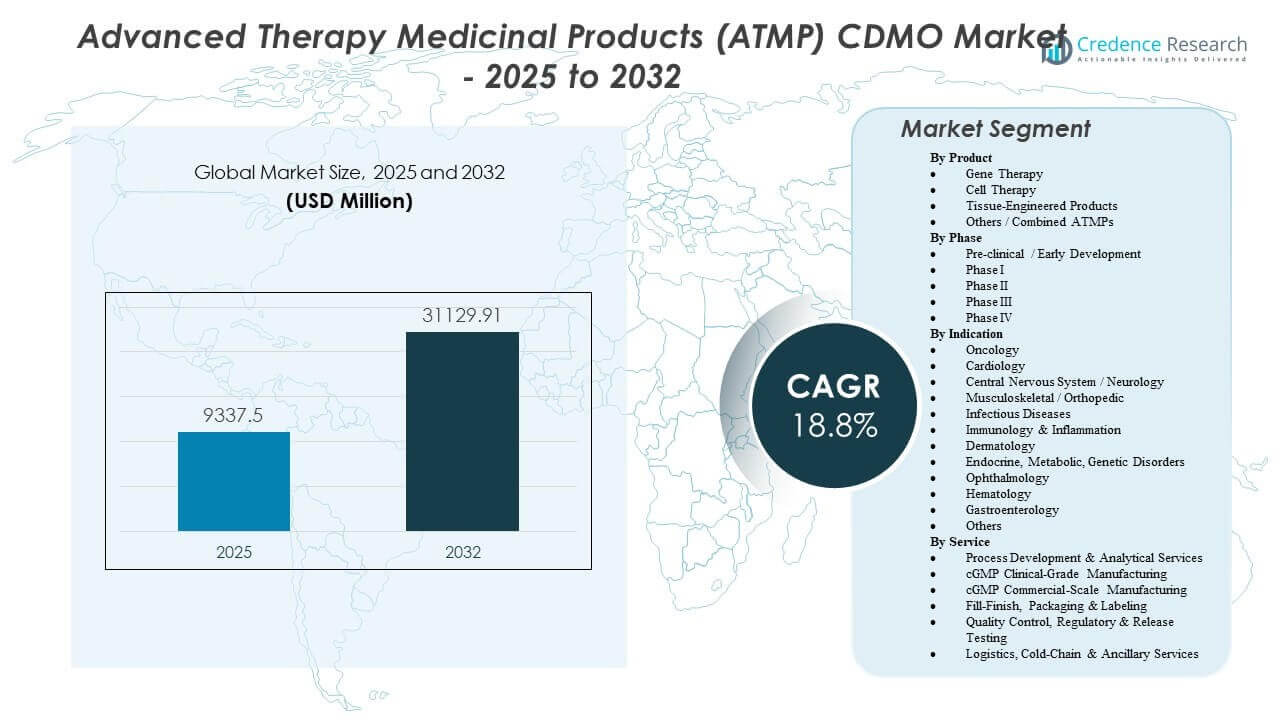
Le marché des produits médicinaux de thérapie avancée (ATMP) CDMO devrait passer de 9 337,5 millions USD en 2025 à environ 31 129,91 millions USD d’ici 2032, avec un taux de croissance annuel composé (TCAC) de 18,8 % de 2025 à 2032.
| ATTRIBUT DU RAPPORT |
DÉTAILS |
| Période Historique |
2020-2024 |
| Année de Base |
2025 |
| Période de Prévision |
2026-2032 |
| Taille du Marché des ATMP CDMO 2025 |
9 337,5 millions USD |
| Marché des ATMP CDMO, TCAC |
18,8% |
| Taille du Marché des ATMP CDMO 2032 |
31 129,91 millions USD |
Informations sur le marché des produits médicinaux de thérapie avancée (ATMP) CDMO :
- Des pipelines cliniques solides et une commercialisation croissante des ATMP stimulent la demande pour des vecteurs viraux, la production de thérapies cellulaires évolutives et des services GMP spécialisés auprès des développeurs mondiaux.
- Les besoins en capitaux élevés, l’expertise interne limitée et les exigences réglementaires complexes restent des contraintes majeures qui poussent les sponsors vers l’externalisation mais créent des défis opérationnels pour les petites entreprises.
- L’Amérique du Nord domine le marché grâce à un écosystème biotechnologique mature et des capacités de fabrication avancées, tandis que l’Europe suit avec des cadres réglementaires solides et des hubs de vecteurs établis.
- L’Asie-Pacifique émerge comme la région à la croissance la plus rapide, soutenue par l’expansion des infrastructures GMP, des investissements stratégiques et l’implication croissante des acteurs biotechnologiques régionaux dans le développement des ATMP.
Moteurs du marché des produits médicinaux de thérapie avancée (ATMP) CDMO
Expansion rapide des programmes cliniques de thérapie cellulaire et génique dans les principales aires thérapeutiques
Les pipelines de thérapie cellulaire et génique continuent de s’étendre dans l’oncologie et les maladies rares. Les sponsors avancent plus de candidats en essais de Phase II et Phase III. Ce changement augmente la demande de capacité de fabrication clinique et commerciale. Le marché des produits médicinaux de thérapie avancée (ATMP) CDMO gagne en dynamisme grâce à cette profondeur de pipeline. Les développeurs nécessitent des plateformes de traitement cellulaire et de vecteurs viraux évolutives. La préparation commerciale exige des systèmes de production validés et reproductibles. Les contrats à long terme garantissent la continuité de l’approvisionnement pour les thérapies approuvées. Un soutien fort des investisseurs alimente davantage l’activité d’externalisation.
- Par exemple, Novartis a rapporté plus de 6 000 patients traités dans le monde avec sa thérapie CAR-T Kymriah®, reflétant la demande clinique et commerciale croissante.
Access crucial information at unmatched prices!
Request your sample report today & start making informed decisions powered by Credence Research Inc.!
Download Sample
Capacités de fabrication interne limitées parmi les entreprises biotechnologiques émergentes
De nombreuses petites et moyennes entreprises de biotechnologie manquent d’infrastructure BPF. Les installations de fabrication internes nécessitent un capital initial élevé et une expertise réglementaire. Les commanditaires préfèrent que des CDMO expérimentés gèrent des flux de production complexes. L’externalisation réduit le risque opérationnel et accélère les délais de développement. Les partenaires spécialisés fournissent un soutien en ingénierie vectorielle et analytique. Une capacité flexible permet aux clients de s’adapter aux résultats des essais. Les partenariats stratégiques améliorent l’efficacité à travers les étapes de développement. Les stratégies légères en actifs renforcent la discipline financière.
Exigences Réglementaires Complexes Et Normes De Qualité Strictes
Les produits ATMP font face à une surveillance réglementaire stricte sur les principaux marchés. La documentation exige une validation détaillée et des données de qualité. Les CDMO offrent des connaissances réglementaires et une préparation aux inspections. Les commanditaires comptent sur des systèmes de qualité établis pour réduire le risque d’approbation. Les procédures standardisées soutiennent une performance produit cohérente. L’expertise en conformité renforce la crédibilité auprès des autorités. L’atténuation des risques devient centrale dans les phases cliniques avancées. Des cadres de qualité solides stimulent la préférence pour l’externalisation.
Commercialisation Croissante Des Thérapies Avancées Approuvées
Les thérapies géniques et cellulaires approuvées passent à des programmes d’accès élargi pour les patients. L’approvisionnement commercial nécessite une capacité de production stable et à grand volume. Les CDMO investissent dans l’expansion des suites BPF pour répondre à ce besoin. Les commanditaires privilégient des partenaires de fabrication fiables. Le transfert technologique de l’échelle clinique à l’échelle commerciale nécessite une expertise. La gestion du cycle de vie soutient une présence durable sur le marché. Les engagements post-approbation augmentent la complexité opérationnelle. La croissance commerciale soutient la demande à long terme pour les CDMO.
- Par exemple, Catalent Cell & Gene Therapy a augmenté la production d’AAV pour Zolgensma dans son installation de Harmans, Maryland, un site de 200 000 pieds carrés équipé de 18 suites cGMP qui soutient les programmes de thérapie génique mondiaux de Novartis.
Tendances Du Marché Des CDMO Pour Les Produits Médicinaux De Thérapie Avancée (ATMP)
Passage Aux Offres De Services Intégrés De Bout En Bout
Les clients recherchent des partenaires uniques qui gèrent le développement jusqu’à la commercialisation. Les CDMO élargissent leurs portefeuilles pour inclure l’analytique, le remplissage-finition et la logistique. Les modèles intégrés améliorent la coordination à travers les étapes du projet. Les commanditaires réduisent la fragmentation des fournisseurs et le fardeau de la supervision. Les services complets renforcent la fidélisation des clients. L’intégration verticale améliore la différenciation concurrentielle. Les alliances stratégiques pluriannuelles remplacent les contrats à court terme. Les modèles de services consolidés améliorent l’efficacité opérationnelle.
Adoption De L’Automatisation Et Des Plates-Formes De Fabrication Fermées
L’automatisation améliore la précision dans l’expansion cellulaire et la production de vecteurs. Les systèmes fermés réduisent le risque de contamination et la variabilité manuelle. La robotique améliore la reproductibilité à travers les lots spécifiques aux patients. Les contrôles numériques renforcent la supervision des processus. L’automatisation réduit la dépendance à l’intervention manuelle. Les systèmes standardisés soutiennent une production allogénique évolutive. Les mises à niveau technologiques augmentent l’utilisation des installations. L’efficacité opérationnelle s’améliore grâce aux outils de fabrication intelligents.
Diversification Géographique De L’Empreinte De Fabrication
Les CDMO s’étendent en Asie-Pacifique et dans les pôles biotechnologiques émergents. Les installations régionales réduisent les risques logistiques et le temps de livraison. Les gouvernements soutiennent l’investissement biotechnologique par le biais d’incitations. La capacité locale renforce la résilience de la chaîne d’approvisionnement. Les sponsors recherchent des réseaux de production diversifiés. Les partenariats transfrontaliers accélèrent l’entrée sur le marché. L’expertise régionale améliore l’alignement réglementaire. La répartition géographique améliore la compétitivité mondiale.
- Par exemple, FUJIFILM Diosynth Biotechnologies a élargi ses capacités mondiales en acquérant l’installation de production de produits biologiques à grande échelle à Hillerød, au Danemark, qui comprend six bioréacteurs en acier inoxydable de 15 000 litres et soutient la fabrication commerciale majeure de produits biologiques pour des clients mondiaux.
Investissement dans les plateformes de vecteurs et de cellules de nouvelle génération
L’innovation dans les systèmes AAV et lentiviraux augmente l’efficacité. Les plateformes de production à haut rendement améliorent l’évolutivité. Les thérapies cellulaires allogéniques attirent l’attention pour un usage plus large. Les analyses avancées améliorent l’optimisation des processus. Les nouveaux systèmes de bioréacteurs améliorent la cohérence des résultats. Les technologies de plateforme raccourcissent les délais de développement. L’amélioration continue stimule la différenciation des services. L’accent mis sur l’innovation garantit un potentiel de croissance à long terme.
- Par exemple, AGC Biologics a introduit ses plateformes BravoAAV™ et ProntoLVV™, utilisant des bioprocédés en suspension évolutifs allant jusqu’à 2 000 L pour l’AAV et 1 000 L pour le LVV afin d’améliorer l’efficacité de la production de vecteurs. Ces systèmes standardisés réduisent les délais de préparation GMP à environ neuf mois, soutenant l’avancement plus rapide des programmes de thérapie génique.
Analyse des défis du marché des produits médicinaux de thérapie avancée (ATMP) CDMO
Contraintes de capacité et goulets d’étranglement de la chaîne d’approvisionnement dans la production de vecteurs viraux
L’approvisionnement en vecteurs viraux reste limité dans plusieurs régions. Les délais pour les plasmides et les matières premières prolongent les délais des projets. L’expansion des installations nécessite des inspections réglementaires et une validation. Le marché des produits médicinaux de thérapie avancée (ATMP) CDMO subit une pression pour répondre à la demande urgente. La logistique de la chaîne du froid ajoute de la complexité à la distribution mondiale. Les pénuries de main-d’œuvre spécialisée ralentissent les plans d’expansion. Les normes de conformité de qualité restent strictes et consomment beaucoup de ressources. Les sponsors s’attendent à un retour rapide et à des résultats constants. L’équilibre entre l’offre et la demande reste un défi clé.
Variabilité réglementaire et structures de coûts élevées sur les marchés mondiaux
Les voies réglementaires diffèrent selon les principales régions. Les normes de documentation exigent des données de validation étendues. Les audits de conformité nécessitent des équipes de qualité dédiées. Les coûts d’exploitation élevés impactent les stratégies de tarification. Les petits développeurs subissent une pression de financement lors des retards cliniques. La volatilité des devises affecte les contrats transfrontaliers. Les risques de propriété intellectuelle compliquent les partenariats. Les négociations de contrats impliquent des termes détaillés de partage des risques. Ces facteurs augmentent la pression opérationnelle sur les CDMO.
Opportunités du marché des produits médicinaux de thérapie avancée (ATMP) CDMO
Expansion dans les pôles biotechnologiques émergents et plateformes de fabrication régionales
Les clusters biotechnologiques émergents investissent dans des infrastructures avancées de produits biologiques. Les gouvernements offrent des incitations pour attirer les installations ATMP. Le marché des CDMO de Produits Médicinaux de Thérapie Avancée (ATMP) peut s’étendre grâce à des partenariats régionaux. La production locale réduit le risque logistique et le coût. Les sites GMP régionaux soutiennent un accès plus rapide aux patients. Les coentreprises créent des modèles d’investissement partagés. Les programmes de transfert de technologie renforcent l’expertise locale. Une entrée précoce sur de nouveaux marchés sécurise des contrats à long terme. La diversification géographique améliore la résilience.
Croissance des plateformes allogéniques et des technologies de vecteurs de nouvelle génération
Les thérapies allogéniques visent une production évolutive prête à l’emploi. Les lignées cellulaires standardisées simplifient les flux de travail de fabrication. Les nouvelles plateformes de vecteurs améliorent l’efficacité de la transduction. Les systèmes de suspension à haute capacité augmentent la production. Les analyses avancées raccourcissent les délais de libération. Les tendances de la médecine personnalisée soutiennent la production de thérapies de niche. Les jumeaux numériques améliorent l’optimisation des processus. Les investissements stratégiques dans l’innovation créent une différenciation. Ces développements ouvrent de nouvelles voies de revenus pour les CDMO.
Analyse de la segmentation du marché des CDMO de Produits Médicinaux de Thérapie Avancée (ATMP) :
Par produit
Le paysage des produits couvre la thérapie génique, la thérapie cellulaire, les produits de génie tissulaire et les ATMP combinés. Sur le marché des CDMO de Produits Médicinaux de Thérapie Avancée (ATMP), la thérapie génique connaît une forte demande grâce aux plateformes basées sur des vecteurs viraux tels que les systèmes AAV et lentiviraux. Ces vecteurs soutiennent les pipelines de maladies rares et d’oncologie. La thérapie cellulaire inclut les formats CAR-T, cellules souches et non cellules souches dans les modèles autologues et allogéniques. Les thérapies autologues nécessitent une fabrication spécifique au patient, tandis que les plateformes allogéniques visent l’échelle. Les produits de génie tissulaire reposent sur des échafaudages et des matrices pour la réparation structurelle. Les thérapies hybrides gène-cellule et les échafaudages biodégradables élargissent les options de traitement complexes.
- Par exemple, WuXi Advanced Therapies a lancé la technologie OXGENE TESSA™ pour la fabrication d’AAV, qui élimine le besoin de transfection plasmidique et a démontré une augmentation de rendement en AAV de 10 fois par rapport aux méthodes traditionnelles de triple transfection.
Par phase
Les phases de développement vont du préclinique et du développement précoce à la Phase I jusqu’à la Phase IV. Les programmes en début de phase se concentrent sur la conception des processus et la validation de la sécurité. Les phases I et II mettent l’accent sur l’optimisation des doses et la production par lots contrôlée. La Phase III nécessite des volumes plus importants et des systèmes GMP validés. La Phase IV soutient l’approvisionnement post-approbation et la gestion du cycle de vie. Les sponsors augmentent l’externalisation aux phases ultérieures pour assurer la préparation commerciale. L’atténuation des risques et la conformité réglementaire deviennent cruciales aux stades avancés. Les CDMO alignent la capacité avec la progression clinique.
Par indication
L’oncologie est en tête en raison de la forte adoption des thérapies CAR-T et des thérapies géniques modifiées. La cardiologie et la neurologie s’étendent grâce à des programmes régénératifs et basés sur les gènes. Les segments musculo-squelettiques et orthopédiques utilisent des échafaudages de génie tissulaire pour la réparation. Les maladies infectieuses et l’immunologie tirent parti de l’édition génique et de la modulation immunitaire. La dermatologie et l’ophtalmologie soutiennent des modèles de délivrance génique localisée. Les troubles endocriniens et génétiques reposent sur la correction génique durable. L’hématologie reste centrale pour la demande en vecteurs viraux et cellules souches. La gastroentérologie et d’autres indications créent des besoins de fabrication de niche.
Par service
Les offres de services vont du développement de processus au support logistique. Les services de développement de processus et d’analyse construisent des flux de travail évolutifs et conformes. La fabrication clinique de qualité cGMP soutient les essais de phases précoce et intermédiaire. La production à l’échelle commerciale nécessite des installations validées et des systèmes d’approvisionnement robustes. Le remplissage, l’emballage et l’étiquetage garantissent l’intégrité du produit. Le contrôle qualité et les tests réglementaires maintiennent les normes de conformité. La logistique de la chaîne du froid gère les matériaux sensibles à la température. Les modèles de services intégrés améliorent l’efficacité tout au long des cycles de développement.
- Par exemple, les services Patheon de Thermo Fisher Scientific ont introduit le programme Quick to Care™, intégrant la fabrication de substances médicamenteuses et de produits médicamenteux avec l’emballage clinique pour rationaliser les flux de travail de développement précoce. La plateforme permet aux entreprises biotechnologiques émergentes d’accélérer leur préparation pour l’approvisionnement clinique en consolidant des étapes qui nécessitent traditionnellement plusieurs partenaires de service.
Segmentation :
Par Produit
- Thérapie Génique
- Basée sur des Vecteurs Viraux
- Thérapie Cellulaire
- CAR-T
- Cellules Souches
- Non-Cellules Souches
- Autologue
- Allogénique
- Produits de Tissu Ingénierie
- Autres / ATMPs Combinés
- Gène-Cellule Hybride
- Échafaudages Biodégradables
Par Phase
- Pré-clinique / Développement Précoce
- Phase I
- Phase II
- Phase III
- Phase IV
Par Indication
- Oncologie
- Cardiologie
- Système Nerveux Central / Neurologie
- Musculosquelettique / Orthopédique
- Maladies Infectieuses
- Immunologie & Inflammation
- Dermatologie
- Troubles Endocriniens, Métaboliques, Génétiques
- Ophtalmologie
- Hématologie
- Gastroentérologie
- Autres
Par Service
- Développement de Processus & Services Analytiques
- Fabrication Clinique de Qualité cGMP
- Fabrication à l’Échelle Commerciale cGMP
- Remplissage, Emballage & Étiquetage
- Contrôle Qualité, Tests Réglementaires & de Libération
- Logistique, Chaîne du Froid & Services Auxiliaires
Par Région
- Amérique du Nord
- États-Unis
- Canada
- Mexique
- Europe
- Allemagne
- France
- Royaume-Uni
- Italie
- Espagne
- Reste de l’Europe
- Asie-Pacifique
- Chine
- Japon
- Inde
- Corée du Sud
- Asie du Sud-Est
- Reste de l’Asie-Pacifique
- Amérique latine
- Brésil
- Argentine
- Reste de l’Amérique latine
- Moyen-Orient & Afrique
- Pays du CCG
- Afrique du Sud
- Reste du Moyen-Orient et de l’Afrique
Analyse régionale :
L’Amérique du Nord détient la plus grande part du marché des produits médicinaux de thérapie avancée (ATMP) CDMO, représentant près de 45 % des revenus mondiaux. Un financement biotechnologique solide et une forte concentration de développeurs de thérapies géniques et cellulaires soutiennent cette domination. Les États-Unis mènent la croissance régionale avec une infrastructure GMP avancée et des voies réglementaires claires. Le Canada soutient l’expansion par le biais de subventions de recherche et de collaborations académiques. L’Europe capture environ 30 % du marché, portée par l’Allemagne, le Royaume-Uni et la France. Des cadres robustes de l’EMA et des programmes de recherche transfrontaliers renforcent la capacité régionale. La région bénéficie de pôles établis de vecteurs viraux et de traitement cellulaire.
L’Asie-Pacifique représente près de 20 % de la part mondiale et enregistre le taux d’expansion le plus rapide. La Chine et le Japon investissent massivement dans la production de thérapies géniques et l’innovation biotechnologique nationale. La Corée du Sud et l’Inde augmentent la capacité GMP grâce à des partenariats publics et privés. Les incitations gouvernementales encouragent le transfert de technologie et le développement des installations. Des coûts d’exploitation inférieurs attirent des contrats d’externalisation internationaux. La disponibilité d’une main-d’œuvre qualifiée améliore la production technique. Les acteurs régionaux poursuivent des alliances stratégiques avec des entreprises biotechnologiques occidentales.
L’Amérique latine et le Moyen-Orient & Afrique représentent collectivement près de 5 % du marché. Le Brésil et le Mexique mènent l’activité en Amérique latine grâce à des initiatives de recherche clinique. Les pays du CCG investissent dans des infrastructures de santé avancées et des parcs biotechnologiques. L’Afrique du Sud soutient les réseaux régionaux d’essais cliniques. La pénétration du marché reste limitée en raison des lacunes réglementaires et des contraintes de financement. Les partenariats locaux aident les CDMO mondiaux à entrer sur les marchés émergents. Des réformes politiques progressives visent à attirer les investissements étrangers.
Shape Your Report to Specific Countries or Regions & Enjoy 30% Off!
Analyse des acteurs clés :
- Lonza Group
- Catalent Inc.
- Thermo Fisher Scientific (Patheon)
- AGC Biologics
- FUJIFILM Diosynth Biotechnologies
- Charles River Laboratories
- Oxford Biomedica PLC
- WuXi Advanced Therapies
- Minaris Regenerative Medicine
- Aldevron
- Samsung Biologics
- Rentschler Biopharma SE
- CELONIC Group
- Eurofins Scientific SE
- RoslinCT
- Andelyn Biosciences
- BlueReg
- CGT Catapult
- Curia Global Inc.
- Bio Elpida by Polyplus
Analyse concurrentielle :
Le marché des produits médicinaux de thérapie avancée (ATMP) CDMO se compose d’un mélange de fabricants biotechnologiques spécialisés et de CDMO mondiaux diversifiés. Les principaux acteurs se concentrent sur l’augmentation de l’échelle des vecteurs viraux, l’automatisation de la thérapie cellulaire et les modèles de services intégrés. Les entreprises investissent dans l’expansion des capacités en Amérique du Nord et en Europe pour sécuriser des contrats à long terme. Les acquisitions stratégiques renforcent l’expertise technique dans les plateformes AAV et lentivirales. Les partenariats avec des startups biotechnologiques créent un accès précoce à des pipelines à fort potentiel. Les entreprises rivalisent sur le bilan réglementaire, le délai d’exécution et la conformité qualité. Les offres intégrées allant du développement de processus à la fabrication commerciale offrent un avantage fort. La concurrence sur les prix reste secondaire par rapport à la capacité technique et à la fiabilité. L’expansion des capacités et la diversification géographique façonnent le positionnement concurrentiel à long terme.
Développements récents :
- En janvier 2024, Pluri, une entreprise biotechnologique basée en Israël, a lancé PluriCDMO, une nouvelle division offrant des services de fabrication de thérapies cellulaires en tant qu’organisation de développement et de fabrication sous contrat (CDMO), avec une installation GMP de 47 000 pieds carrés.
- En janvier 2024, Charles River Laboratories International Inc. a introduit son offre de plasmides Rep/Cap prêts à l’emploi pour rationaliser les programmes de thérapie génique basés sur le virus adéno-associé (AAV).
Couverture du rapport :
Le rapport de recherche offre une analyse approfondie basée sur Produit, Phase, Indication, Service et Région. Il détaille les principaux acteurs du marché, fournissant un aperçu de leur activité, de leurs offres de produits, de leurs investissements, de leurs sources de revenus et de leurs applications clés. De plus, le rapport inclut des informations sur l’environnement concurrentiel, l’analyse SWOT, les tendances actuelles du marché, ainsi que les principaux moteurs et contraintes. En outre, il discute de divers facteurs qui ont stimulé l’expansion du marché ces dernières années. Le rapport explore également la dynamique du marché, les scénarios réglementaires et les avancées technologiques qui façonnent l’industrie. Il évalue l’impact des facteurs externes et des changements économiques mondiaux sur la croissance du marché. Enfin, il fournit des recommandations stratégiques pour les nouveaux entrants et les entreprises établies afin de naviguer dans les complexités du marché.
Perspectives d’avenir :
- La demande pour des plateformes intégrées de développement et de fabrication commerciale renforcera les partenariats d’externalisation à long terme.
- L’expansion des programmes de thérapie cellulaire allogénique améliorera l’évolutivité et la standardisation sur les sites de production.
- L’automatisation et les technologies de systèmes fermés amélioreront la cohérence des lots et réduiront le risque opérationnel.
- L’innovation en matière de vecteurs viraux augmentera l’efficacité de transduction et améliorera les rendements de fabrication.
- Les alliances stratégiques entre les CDMO et les startups biotechnologiques accéléreront les transitions des programmes en phase précoce.
- Les pôles de fabrication régionaux en Asie-Pacifique attireront des contrats d’approvisionnement clinique transfrontaliers.
- Les analyses avancées et les systèmes de qualité numériques soutiendront la conformité réglementaire et l’intégrité des données.
- L’investissement dans des installations GMP modulaires offrira une capacité flexible pour des pipelines multi-produits.
- La croissance des pipelines de maladies rares et d’oncologie soutiendra des contrats de services à haute valeur ajoutée.
- La logistique de la chaîne du froid et les réseaux de distribution spécialisés s’étendront pour soutenir la commercialisation mondiale.




