API合同制造市场概况:
预计API合同制造市场将从2024年的81.2亿美元增长到2032年的1262.321亿美元,2024年至2032年的复合年增长率(CAGR)为5.70%。
| 报告属性 |
详细信息 |
| 历史时期 |
2020-2023 |
| 基准年 |
2024 |
| 预测期 |
2025-2032 |
| 2024年API合同制造市场规模 |
81.2亿美元 |
| API合同制造市场,CAGR |
5.70% |
| 2032年API合同制造市场规模 |
1262.321亿美元 |
随着制药公司寻求降低固定成本和加快产品上市,外包API生产不断增长。发起者依赖于拥有GMP设施、验证流程和可扩展能力的合作伙伴。对高效能API、受控物质和复杂化学品的需求增加,提升了对专业化封闭和安全系统的需求。越来越多的小型和虚拟制药公司选择轻资产模式,更倾向于外部供应网络。合同制造商还支持生命周期需求,如路线优化、产量提升和杂质控制。稳定的供应保障和双重采购计划进一步推动长期制造协议。
由于创新者活动强劲、高临床试验量和严格的质量期望,北美处于领先地位,这些因素有利于经验丰富的合同合作伙伴。欧洲因成熟的监管体系、高价值专利药物和复杂合成的深厚专业知识而保持重要地位。亚太地区以印度和中国为首,凭借大规模产能和具有竞争力的成本结构,成为最快的增长引擎。日本和韩国对高质量、利基和高效能生产的需求增加。东南亚因公司将供应链多样化超越单一国家依赖而获得关注。区域扩张符合对弹性、更快交付和更贴近市场制造的需求。
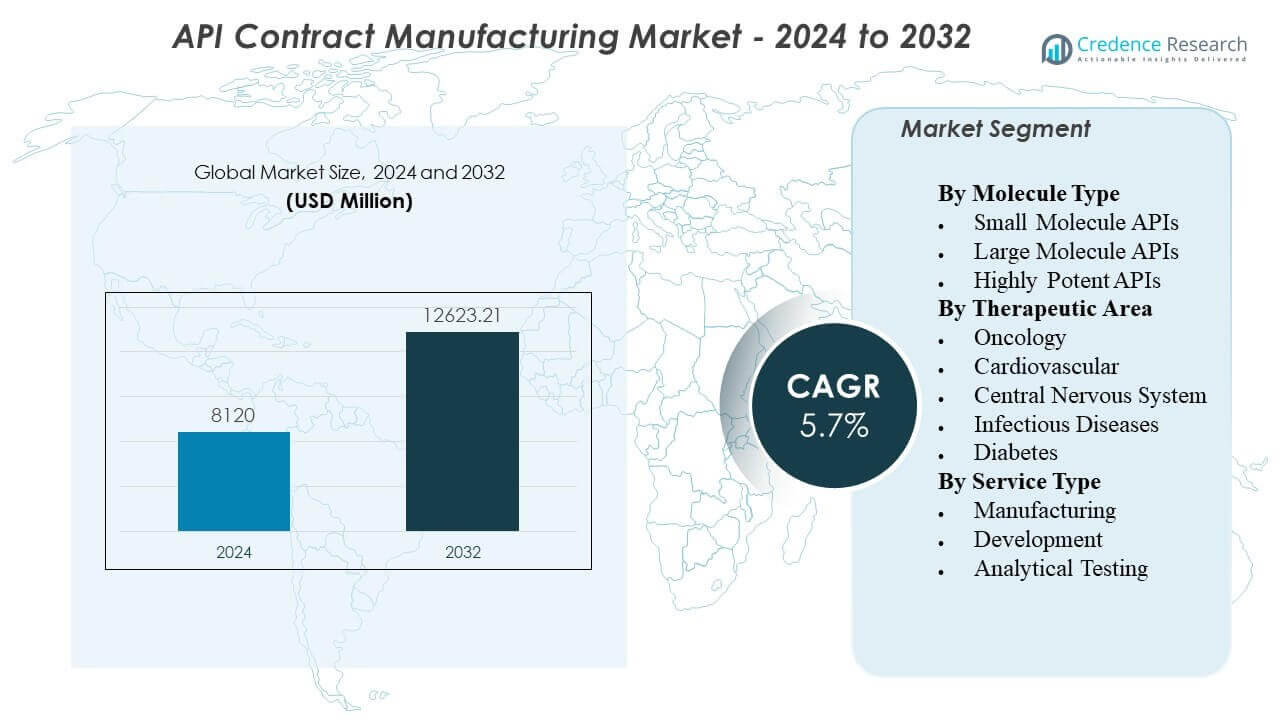
API 合同制造市场洞察:
- 亚太地区以35%的份额领先,北美紧随其后,占29%,欧洲因强大的制造基地、成熟的合规性和大量的赞助商需求占据20%。
- 拉丁美洲是增长最快的地区,占9%的份额,受供应商多样化、制药产量扩大和区域外包活动增加的推动。
- 细分市场偏向于化学合成API,其中有机占61%的份额,无机占27%,其他占12%。
- 终端用户分布显示制药行业占66%,研究机构占15%,其他占19%,这表明商业供应计划的需求强劲。
API 合同制造市场驱动因素:
外包需求上升以降低固定成本并提高上市速度
制药公司通过外包API生产来减少资本支出。API合同制造市场从这种运营模式的转变中受益。赞助商避免新建工厂,将资金转向研发。合同伙伴比新的内部生产线更快地提供批次准备。CMO提供训练有素的团队、合格的设施和经过审核的质量体系。赞助商还获得了根据产品阶段调整产量的灵活性。更快的技术转移支持更快的临床进展和上市计划。此驱动因素在品牌和仿制药组合中均保持强劲。
- 例如,赛默飞世尔科技(Patheon)利用其“Quick to Care”计划,将从API合成到临床药品供应的时间缩短至仅14周,与行业标准的6到9个月相比大幅减少。
Access crucial information at unmatched prices!
Request your sample report today & start making informed decisions powered by Credence Research Inc.!
Download Sample
更严格的监管期望推动赞助商转向成熟的质量体系
监管机构期望强大的数据完整性和经过验证的控制。赞助商更倾向于选择具有成熟GMP合规性和审核历史的CMO。设计质量实践减少了变异性并支持稳定供应。强大的杂质控制增强了对受监管市场的接受度。合作伙伴投资于验证、清洁验证和电子文档。赞助商利用这些能力来降低跨站点的合规风险。可靠的批次发布时间表支持下游配方计划。随着全球检查强度和更严格的报告规则,此驱动因素增长。
复杂分子和高效能API增加了对专业能力的需求
更多的管线包括强效和复杂的小分子。这些项目需要隔离、职业安全和精确的分析方法。CMO通过分隔的气流和封闭处理扩展HPAPI套件。专家工艺化学提高了产量并减少了副产品。先进的分析支持杂质分析和稳定性研究。赞助商选择能够管理多步合成和严格规格的合作伙伴。放大技术知识减少了实验室和商业批次之间的延迟。随着肿瘤学和特种药物的增长,此驱动因素上升。
- 例如,Piramal Pharma Solutions表示其高效能套件可以在千克实验室规模下处理OEL < 1 µg/m³的化合物,能力低至10 ng/m³,反应器体积高达50 L,处理能力高达2 kg。
供应链弹性需求鼓励双重采购和区域冗余
赞助商在最近的供应中断后优先考虑连续性。双重采购减少了对单一工厂或地区的依赖。CMO通过多个合格的站点支持网络策略。库存缓冲和可靠的原材料获取提高了服务水平。强大的供应商资格认证可以防止输入变量。赞助商还寻求缩短关键中间体的交货时间。更好的弹性支持长期供应协议和数量承诺。这个驱动因素对于基本药物和慢性治疗仍然是核心。
API合同制造市场趋势:
从路线设计到商业供应的端到端服务一体化转变
赞助商更倾向于在价值链中减少交接次数。CMO从API输出扩展到开发支持和技术转移。一个合作伙伴可以涵盖路线选择、放大和验证。这一趋势改善了化学、分析和质量团队之间的协调。更快的问题解决减少了周期时间和批次偏差风险。赞助商在里程碑和交付物方面获得更清晰的责任感。API合同制造市场反映了对全方位服务合作伙伴关系的更强需求。综合产品还支持生命周期优化和成本控制。
- 例如,Lonza宣布将CDMO重组为三个平台:综合生物制剂、先进合成和专业模式,以协调开发到商业跨度的服务。
更多使用数字质量系统和实时过程数据进行控制
CMO采用数字批记录和电子质量工作流程。实时数据改善了过程可见性和更快的偏差响应。预测性维护降低了关键设备的停机风险。数据完整性控制减少了手动错误和审计差距。高级仪表板支持首次正确的批次执行。赞助商重视透明的报告和更快的文件周转。数字工具还支持远程审计和供应商监督。随着更广泛的制药数字路线图,这一趋势加速。
越来越倾向于长期战略合作伙伴关系而非短期现货合同
赞助商在容量和供应规划中寻求稳定性。多年协议确保了临床和商业需求的时段。CMO通过专用生产线和优先调度模型作出回应。联合治理改善了沟通和变更控制。共享KPI对齐质量、交付和成本目标。赞助商还共同投资于特定化学品的设备。API合同制造市场看到更多基于合作伙伴关系的采购决策。这一趋势支持领先CMO的更强收入可见性。
- 例如,Novo Holdings同意以165亿美元收购Catalent,Novo Nordisk计划以110亿美元收购Catalent的三个灌装-终端站点,这显示了大型买家如何通过结构化交易锁定长期容量。
扩展多站点制造网络以更快地服务区域市场
CMO在关键地区建立或收购站点。网络覆盖减少了运输时间和海关复杂性。区域存在支持本地语言支持和监管机构的参与。赞助商重视邻近生产以应对敏感或时间紧迫的API。多站点策略还减少了地缘政治和物流风险。标准化流程使站点间的转移更加顺畅。这一趋势支持在市场需求变化时更快地扩大规模。网络扩展在欧洲、亚洲和北美仍然活跃。
API合同制造市场挑战分析:
监管审查和合规负担带来高成本和执行风险
当系统不达标时,检查可能导致延误。CMO必须保持强大的文档和数据完整性。小的差距可能导致警告信和合同丢失。验证和变更控制需要深厚的专业知识和纪律。赞助商要求频繁的审计和快速的纠正行动计划。质量岗位的人才短缺增加了运营压力。API合同制造市场面临满足多样化地区规则的压力。合规成本上升,而价格预期保持紧张。
原材料波动和产能限制可能扰乱时间表和利润率
关键起始材料面临价格波动和供应限制。当出现短缺时,单一来源的投入可能会停止生产。长交货期使多步骤合成的项目规划复杂化。需求高峰和活动重叠期间出现产能瓶颈。CMO必须平衡许多客户的不同优先需求。货运变动影响交付可靠性和成本。即使在输入不确定的情况下,赞助商也要求确定的日期。当输入迅速变化时,利润率控制变得更加困难。
API合同制造市场机会:
对特种和高效能API的需求增加开辟了高端服务领域
更多的肿瘤和罕见疾病药物使用高效能化合物。CMO可以通过先进的封闭和分析赢得项目。赞助商为经过验证的安全系统和一致的质量付费。快速扩展能力支持更快的临床时间表。强大的杂质控制有助于在严格市场中的批准。这一机会有利于具有差异化工艺化学的公司。API合同制造市场可以通过这些高端项目扩展。HPAPI套房的产能增加可以提升长期合同。
本地化和多元化制造策略创造新的区域增长路径
赞助商将供应多样化,超越单一国家依赖。CMO可以增加区域产能以支持近市场供应。本地站点减少物流风险并缩短交货时间。与区域供应商的合作改善了原材料获取。政府对国内制药的支持也推动了新项目。更快的监管参与改善了关键药物的市场进入。这一机会支持在关键枢纽的并购和新建投资。当CMO提供多区域冗余时,合同获胜增加。
API合同制造市场细分分析:
按分子类型
由于在慢性和急性治疗中的广泛使用以及强劲的仿制药量,小分子API引领需求。随着生物制剂的扩展和赞助商寻求专业的发酵、纯化和强大的质量控制,大分子API增长更快。由于肿瘤管线和需要高隔离套房、严格的OEL合规性和先进的杂质控制的特效药,高效能API的市场份额增加。
按 治疗领域
肿瘤学推动了高端外包,因为复杂、高效能的化合物需要严格的安全性和严格的规格。心血管项目保持稳定的产量,倾向于成本效益高、高通量的生产。由于治疗周期长,中枢神经系统API依赖于一致的质量和供应连续性。随着抗菌药物管理需求和偶发性疫情响应的增加,传染病的需求上升。糖尿病支持大规模、可预测的需求,倾向于能够提供稳定产出和可靠交货时间的合作伙伴。
- 例如,Lonza报告称,其负载-连接器制造套房可以处理低至1 ng/m³ OEL的化合物,反应器尺寸为1–50 L,温度范围为−80°C至+150°C,符合严格的肿瘤负载要求。
按 服务类型
制造仍然是核心收入来源,因为赞助商将批量生产、规模扩大和商业供应外包。随着客户需要路线选择、工艺优化和技术转移支持以减少周期时间,开发服务正在扩展。分析测试的重要性增加,因为监管机构期望有强有力的方法验证、杂质剖析和稳定性数据。
- 例如,NNIT报告称,Lonza的批次释放仪表板将批次释放时间减少了90%,将每日批次释放管理任务从30小时减少到30分钟,这显示了数字化工作流程如何加强质量保证执行和释放准备。
细分:
按分子类型
按治疗领域
按服务类型
按地区
区域分析:
亚太地区以大规模产能和出口驱动供应领先
亚太地区占有35%的市场份额,领先全球活动。API合同制造市场在此因成本效益生产和深厚的工艺化学人才而获得力量。印度和中国是仿制药和许多特种API的主要产出国。日本和韩国以强大的合规性支持高质量和利基API需求。赞助商利用该地区进行商业供应和快速扩展需求。政府对制药制造的支持也促进了产能扩张。大量的中间体供应商基地提高了采购灵活性。
北美通过创新和严格的质量期望保持强劲份额
北美占全球市场份额的29%。由于高研发活动和强大的临床管道,美国推动了需求。赞助商寻求拥有成熟GMP系统和可靠审计记录的合作伙伴。成熟的生态系统支持复杂项目,包括高效和特种API。质量期望偏向于具有强大分析深度的成熟CMO。供应链弹性计划也支持更多本地和双源策略。该地区受益于与赞助商的紧密联系和更快的协调。
欧洲仍是关键枢纽,而拉丁美洲和中东及非洲从较小的基础上扩展
欧洲占有20%的市场份额,得益于强大的监管框架和先进的制造标准。德国和瑞士仍然是高质量API生产和创新驱动项目的重要地点。拉丁美洲占有9%的份额,通过不断扩大的制药需求和近岸供应选项增长。巴西和墨西哥支持区域规模和合同生产需求。中东和非洲占有7%的份额,随着医疗投资和本地制造计划的增长而扩展。区域多元化战略帮助这些市场随着时间的推移吸引新的项目。
关键玩家分析:
- 龙沙集团
- Catalent公司
- 勃林格殷格翰
- 梯瓦制药工业
- 太阳制药工业
- 皮拉马尔制药解决方案
- 艾伯维公司
竞争分析:
API合同制造市场显示出全球CDMO与具有自有产能的综合制药公司之间的激烈竞争。大型企业通过多地点网络、成熟的GMP记录和深厚的工艺化学技能赢得合同。顶级公司投资于高效能隔离、先进分析和可扩展反应器,以支持复杂的管道。合同条款越来越倾向于长期合作伙伴关系,这提高了可靠交付和审核准备的价值。商品化小分子工作的价格压力持续存在,因此供应商在产量、周期时间和质量指标上竞争。由于验证成本、人才需求和客户资格审查时间表,新进入者面临高壁垒。它奖励那些结合技术深度、具有弹性采购和快速技术转移的供应商。
最新动态:
- 2026年2月,龙沙集团通过全面整合其抗体药物偶联物(ADC)技术平台(包括从Synaffix收购的专有GlycoConnect和toxSYN连接载体)加强了其高级合成产品组合。这一更新紧随2025年的里程碑事件,当时公司实现了21.7%的销售增长,主要得益于收购了加利福尼亚州瓦卡维尔的全球最大生物制剂生产基地之一,并在2026年初获得了第五个主要商业合同。
- 2026年1月,梯瓦重申其剥离活性药物成分(Teva api)业务的意图,在与之前买家的独家谈判终止后,启动了新的销售流程。虽然API部门仍然是“待售”资产,但梯瓦在2025年底成功在美国推出了首个仿制GLP-1(利拉鲁肽),利用其内部制造专业知识捕捉高增长的减肥市场。
- 2025年12月,太阳制药宣布投资3000亿卢比(3.6亿美元)在印度中央邦建设一个新的绿色地带制剂工厂,以加强其国内和全球供应链。2025年全年,公司积极扩展其合同研究和制造服务(CRAMS),将自己定位为全球创新者在新化学实体(NCEs)方面的主要合作伙伴。
Shape Your Report to Specific Countries or Regions & Enjoy 30% Off!
报告覆盖范围:
研究报告提供了基于分子类型、治疗领域、服务类型和地区的深入分析。它详细介绍了领先的市场参与者,提供了他们的业务概况、产品供应、投资、收入来源和关键应用。此外,报告还包括对竞争环境、SWOT分析、当前市场趋势以及主要驱动因素和限制因素的见解。此外,它讨论了近年来推动市场扩张的各种因素。报告还探讨了影响行业的市场动态、监管情景和技术进步。它评估了外部因素和全球经济变化对市场增长的影响。最后,它为新进入者和成熟公司提供了在市场复杂性中导航的战略建议。
未来展望:
- CDMO 扩大高封闭能力以处理高效能 API,特别是需要严格操作员安全和低交叉污染风险的肿瘤管线。
- 赞助商增加双重采购和多地点资格认证,以保护供应连续性,减少单一地区的风险,并满足长期合同承诺。
- 更多客户选择能够在一个质量体系和一个治理模式下处理路线选择、放大、验证和商业供应的综合合作伙伴。
- 分析测试获得战略价值,因为监管机构要求更强的杂质控制、方法验证、稳定性数据以及在审计和调查期间更快的响应。
- 数字质量工具、电子批记录和实时过程监控提高偏差控制,缩短发布周期,并加强数据完整性预期。
- 产能规划转向灵活的生产活动,可以更快地在产品之间切换,支持较小的临床批次,同时仍能满足商业量。
- 随着赞助商推动更高的产量、更低的溶剂使用和更严格的成本目标而不影响规格控制,工艺优化成为关键杠杆。
- 区域足迹扩大以支持近市场供应,降低物流风险,并改善与客户和当地监管机构的协调。
- 生物偶联和有效载荷-连接子工作扩展,提升对专业化学、隔离和高度敏感分析表征的需求。
- 人才发展变得至关重要,因为公司在争夺经验丰富的化学家、质量保证领导者和验证专家,以维持大规模的质量表现。




