Visión General del Mercado
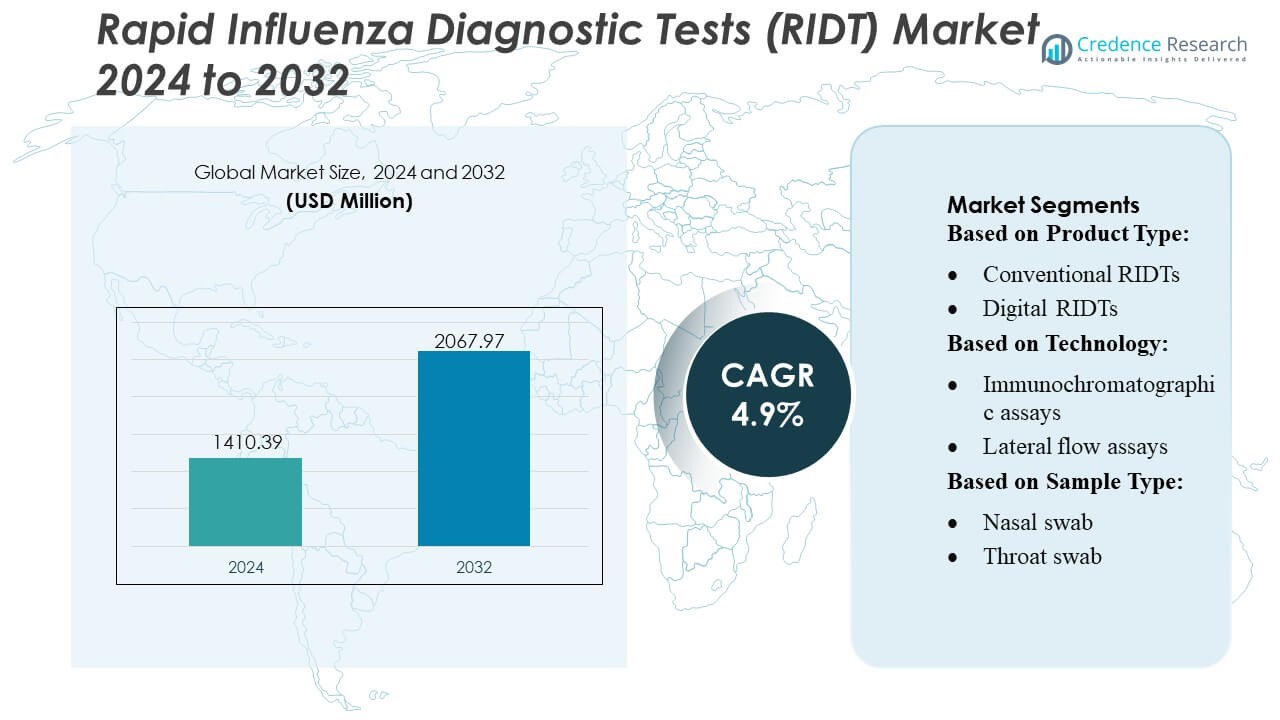
El tamaño del mercado de Pruebas de Diagnóstico Rápido de Influenza (RIDT) se valoró en USD 1410.39 millones en 2024 y se anticipa que alcanzará USD 2067.97 millones para 2032, con un CAGR del 4.9% durante el período de pronóstico.
| ATRIBUTO DEL INFORME |
DETALLES |
| Período Histórico |
2020-2023 |
| Año Base |
2024 |
| Período de Pronóstico |
2025-2032 |
| Tamaño del Mercado de Pruebas de Diagnóstico Rápido de Influenza (RIDT) 2024 |
USD 1410.39 Millones |
| Pruebas de Diagnóstico Rápido de Influenza (RIDT) Mercado, CAGR |
4.9% |
| Tamaño del Mercado de Pruebas de Diagnóstico Rápido de Influenza (RIDT) 2032 |
USD 2067.97 Millones |
El mercado de Pruebas de Diagnóstico Rápido de Influenza (RIDT) presenta una fuerte competencia entre los principales fabricantes de diagnósticos que se centran en tecnologías de detección rápida de antígenos, plataformas basadas en lectores digitales y soluciones de pruebas descentralizadas. Estas empresas fortalecen sus carteras a través de ensayos de alta sensibilidad, paneles respiratorios multiplex y kits de punto de atención diseñados para hospitales, clínicas minoristas y pruebas en el hogar. La inversión continua en I+D, las aprobaciones regulatorias y las redes de distribución ampliadas mejoran su presencia en el mercado. América del Norte lidera el mercado global de RIDT con una participación exacta del 38%, respaldada por una infraestructura de salud avanzada, altos volúmenes de pruebas y una fuerte adopción de sistemas de diagnóstico conectados que mejoran la vigilancia de la influenza y la toma de decisiones clínicas.
Access crucial information at unmatched prices!
Request your sample report today & start making informed decisions powered by Credence Research Inc.!
Download Sample
Perspectivas del Mercado
- El mercado se valoró en USD 1410.39 millones en 2024 y se proyecta que alcance USD 2067.97 millones para 2032, avanzando a un CAGR del 4.9% durante el período de pronóstico.
- El crecimiento del mercado está impulsado por el aumento de la incidencia de influenza, la fuerte adopción de pruebas de detección en el punto de atención y la creciente demanda de kits de detección de antígenos rápidos y de alta precisión en hospitales y clínicas minoristas.
- Las tendencias clave incluyen la expansión de RIDTs basados en lectores digitales, el desarrollo de paneles respiratorios multiplex y una mayor disponibilidad de pruebas rápidas de influenza en el hogar y OTC.
- La actividad competitiva se intensifica a medida que las empresas mejoran la sensibilidad de los ensayos, buscan aprobaciones regulatorias y expanden las redes de distribución para entornos de pruebas descentralizados.
- América del Norte lidera con una participación del 38%, mientras que las pruebas rápidas digitales capturan una creciente participación de segmento a nivel mundial; Asia-Pacífico sigue con una creciente adopción respaldada por la expansión de la infraestructura de diagnóstico y las necesidades de gestión de brotes estacionales.
 Análisis de Segmentación del Mercado:
Análisis de Segmentación del Mercado:
Por Tipo de Producto
El mercado de Pruebas de Diagnóstico Rápido de Influenza (RIDT) está liderado por RIDTs convencionales, capturando un estimado 58% de participación debido a su bajo costo, amplia adopción clínica y capacidad para entregar resultados en 10-15 minutos en entornos de atención primaria. Los hospitales y centros de atención urgente prefieren estos kits para pruebas estacionales de alto volumen, apoyando su continua dominancia. Las RIDTs digitales ganan terreno a medida que los lectores integrados mejoran la precisión de los resultados y reducen los errores de interpretación dependientes del usuario. La adopción aumenta en clínicas que implementan dispositivos con conectividad que apoyan la integración de registros electrónicos de salud y el monitoreo remoto de enfermedades infecciosas, pero su costo más alto limita la adopción inmediata a gran escala.
- Por ejemplo, la prueba Accula™ Flu A/Flu B de Thermo Fisher Scientific integra tecnología RT-PCR en una plataforma portátil del tamaño de la palma de la mano y generalmente entrega resultados confirmados en 30 minutos, mientras que su instrumentación soporta controles automáticos a bordo y lecturas digitales que reducen significativamente la variabilidad manual asociada con las pruebas de interpretación visual.
Por Tecnología
Los ensayos inmunocromatográficos dominan el mercado con una participación aproximada del 52%, impulsados por su rápido tiempo de respuesta, flujos de trabajo simplificados y compatibilidad con entornos de pruebas descentralizadas. Estos ensayos siguen siendo el estándar para el cribado de influenza en centros de salud comunitarios. Los ensayos de flujo lateral se expanden en pruebas ambulatorias y en farmacias debido a su facilidad de uso, mientras que las RIDTs basadas en PCR experimentan un fuerte crecimiento a medida que las plataformas moleculares logran tiempos de procesamiento más rápidos, inferiores a 20 minutos, con mayor sensibilidad. El aumento en el desarrollo de paneles moleculares multiplex y sistemas automatizados basados en cartuchos acelera aún más la adopción en entornos de atención de alta agudeza.
- Por ejemplo, la prueba OSOM® Ultra Flu A&B de SEKISUI Diagnostics es un inmunoensayo rápido sin instrumentos que entrega resultados visuales en 10 minutos e incorpora un sistema de anticuerpos monoclonales patentado diseñado para mejorar la afinidad de unión del antígeno.
Por Tipo de Muestra
Los hisopos nasales ocupan la posición de liderazgo con casi 64% de participación de mercado, apoyados por una mayor recuperación de carga viral, mejor sensibilidad diagnóstica y recomendaciones generalizadas de guías clínicas para pruebas de influenza. Su método de recolección no invasivo los hace preferidos en poblaciones pediátricas y adultas, impulsando una demanda constante en hospitales y centros ambulatorios. Los hisopos de garganta mantienen un uso de nicho pero enfrentan limitaciones de menor sensibilidad, limitando una adopción más amplia. Otros tipos de muestras, incluidos aspirados y lavados nasofaríngeos, siguen siendo relevantes en laboratorios de diagnóstico especializados donde se requiere una mayor precisión de detección, particularmente para infecciones graves o evaluaciones de pacientes inmunocomprometidos.
Principales Impulsores de Crecimiento
- Aumento de la Carga Global de Influenza y Demanda de Detección Rápida
El aumento de la incidencia de influenza estacional y pandémica impulsa fuertemente la demanda de Pruebas de Diagnóstico Rápido de Influenza (RIDTs), ya que los proveedores de atención médica priorizan la detección temprana para reducir la transmisión y las complicaciones. La alta afluencia de pacientes en clínicas ambulatorias, centros de atención urgente y departamentos de emergencia acelera la adopción de cribado rápido en el punto de atención. Los claros beneficios como el rápido tiempo de respuesta, el muestreo simplificado y la toma de decisiones clínicas inmediatas mejoran la penetración en el mercado. Los programas de vigilancia de influenza liderados por el gobierno y las campañas de vacunación refuerzan aún más la necesidad de herramientas de diagnóstico rápidas y confiables para manejar los picos anuales de influenza.
- Por ejemplo, F. Hoffmann-La Roche Ltd informa que su ensayo cobas® Liat® Influenza A/B proporciona resultados de RT-PCR totalmente automatizados en 20 minutos, con un sistema de preparación de muestras a bordo que procesa muestras de hisopos utilizando una arquitectura de tubo cerrado que minimiza el riesgo de contaminación y permite un tiempo de manipulación de menos de 1 minuto.
- Avances Tecnológicos que Mejoran la Precisión Diagnóstica
Los avances en ensayos inmunocromatográficos, lectores digitales y tecnologías de amplificación molecular mejoran significativamente la sensibilidad y especificidad de los RIDTs. Los fabricantes se centran en desarrollar plataformas que ofrezcan una precisión cercana a la PCR mientras mantienen la usabilidad en el punto de atención, permitiendo una mejor identificación de las cepas de influenza A y B. La integración de analizadores digitales minimiza los errores de interpretación humana y apoya la conectividad de datos para el soporte de decisiones clínicas. Las inversiones continuas en I+D, los materiales mejorados para la detección de antígenos y la estabilidad mejorada de los reactivos aumentan la confianza clínica en los RIDTs, impulsando una adopción más amplia en hospitales, farmacias y sitios de pruebas descentralizados.
- Por ejemplo, Abbott Laboratories informa que su ensayo ID NOW™ Influenza A & B 2 utiliza amplificación isotérmica de ácidos nucleicos para ofrecer resultados confirmados en 13 minutos, con detecciones positivas a menudo señaladas en menos de 6 minutos, y su instrumento portátil ejecuta controles internos automatizados en cada ejecución para mantener la integridad analítica.
- Expansión de Pruebas Descentralizadas y en el Hogar
La creciente adopción de modelos de pruebas descentralizadas impulsa el mercado a medida que los pacientes dependen cada vez más de pruebas rápidas fuera de los entornos de atención médica tradicionales. La expansión de clínicas minoristas, diagnósticos en el hogar y la disponibilidad de pruebas OTC fortalece la accesibilidad y fomenta el comportamiento de pruebas tempranas. La creciente conciencia del consumidor sobre el autoexamen después del COVID-19 apoya la aceptación de RIDTs intuitivos con métodos de muestreo simples. Los fabricantes innovan kits compactos y fáciles de usar que ofrecen resultados instantáneos y cumplen con los estándares regulatorios, acelerando el crecimiento del mercado. Este cambio hacia ecosistemas de pruebas convenientes y distribuidos complementa los servicios de telesalud y aumenta el consumo general de RIDTs.
Tendencias y Oportunidades Clave
- Creciente Integración de Plataformas Diagnósticas Digitales y Conectadas
Una tendencia importante se centra en el desarrollo de sistemas RIDT digitalmente conectados que capturan, almacenan y transmiten datos diagnósticos en tiempo real. Estas plataformas apoyan la interpretación automatizada de resultados, mejorando la precisión clínica mientras permiten el monitoreo remoto y la vigilancia de la influenza. La conectividad con registros electrónicos de salud y bases de datos de salud pública mejora el seguimiento de brotes y la asignación de recursos. La tendencia presenta oportunidades para que los fabricantes integren inteligencia artificial, lectores basados en teléfonos inteligentes y soluciones vinculadas a la nube, fortaleciendo el papel de los RIDTs en diagnósticos de precisión y monitoreo de infecciones a nivel poblacional.
- Por ejemplo, Meridian Bioscience, Inc. ofrece la plataforma molecular Alethia®, que archiva digitalmente los datos de ejecución de ensayos y proporciona resultados de influenza A/B en aproximadamente 1 hora mediante amplificación isotérmica mediada por bucle (LAMP).
- Creciente Oportunidad en Farmacias y Clínicas Minoristas
La rápida expansión de la infraestructura de atención médica minorista crea fuertes oportunidades comerciales para los RIDTs. Las farmacias y las clínicas sin cita previa ofrecen cada vez más pruebas de detección de influenza como parte de los servicios de diagnóstico en el punto de atención. Su alta accesibilidad, horarios de operación extendidos y menores costos de consulta atraen a pacientes que buscan pruebas inmediatas. A medida que las agencias reguladoras continúan apoyando los protocolos de diagnóstico dirigidos por farmacéuticos, la demanda de RIDTs compactos y de lectura rápida aumenta. Este cambio abre caminos para que los fabricantes colaboren con cadenas minoristas, co-desarrollen kits de prueba optimizados para el flujo de trabajo y expandan el alcance del mercado en áreas urbanas y suburbanas.
- Por ejemplo, Hologic, Inc. ofrece el ensayo Panther Fusion® Flu A/B/RSV, que procesa muestras utilizando PCR totalmente automatizada con resultados en 2.5 horas y cuenta con carga continua de muestras de hasta 120 especímenes, lo que permite a las farmacias y redes de clínicas escalar el rendimiento de las pruebas de influenza mientras mantienen un informe digital rastreable en sitios interconectados.
- Desarrollo de Paneles de Prueba Multiplex y Multi-Patógeno
Una oportunidad clave surge de la creciente demanda de ensayos multiplex capaces de detectar influenza junto con RSV, SARS-CoV-2 y otros patógenos respiratorios en una sola prueba. Los sistemas de salud prefieren estos paneles por su eficiencia, salida diagnóstica integral y reducción de la carga de recursos. La combinación de múltiples analitos mejora la precisión en la toma de decisiones clínicas y se alinea con la variabilidad de la temporada respiratoria. Los fabricantes que invierten en RIDTs compactos y multiobjetivo pueden obtener una ventaja competitiva significativa, especialmente en entornos de atención aguda y de pruebas de alto volumen.
Desafíos Clave
- Sensibilidad Limitada en Comparación con los Diagnósticos Moleculares
A pesar de las mejoras, muchos RIDTs convencionales aún muestran menor sensibilidad en comparación con los ensayos moleculares, especialmente durante las etapas tempranas de la infección o en condiciones de baja carga viral. Esta limitación aumenta el riesgo de falsos negativos, afectando la precisión de las decisiones clínicas y llevando a algunas instituciones a depender de pruebas confirmatorias de PCR. La variabilidad en la calidad de la recolección de muestras también impacta el rendimiento de la prueba. Estos desafíos restringen la adopción de RIDT en entornos clínicos de alto riesgo, obligando a los fabricantes a invertir en química de reactivos mejorada, lectores digitales y plataformas híbridas para mejorar la fiabilidad diagnóstica.
- Presiones de Cumplimiento Regulatorio y Estándares de Rendimiento
El fortalecimiento de los marcos regulatorios globales, incluidos requisitos de precisión más estrictos y protocolos de validación de calidad, plantea desafíos para los fabricantes. El cumplimiento de los estándares de rendimiento actualizados, las autorizaciones de uso de emergencia y las demandas de vigilancia post-mercado aumentan los costos y los plazos de desarrollo. Las empresas más pequeñas enfrentan mayores barreras para cumplir con los estándares de sensibilidad analítica y garantizar la consistencia en los lotes de producción. Además, la rápida evolución tecnológica requiere actualizaciones continuas para mantener la alineación regulatoria. Estas presiones complican la entrada al mercado y la competitividad a largo plazo, especialmente para los nuevos participantes en el ecosistema de pruebas diagnósticas.
Análisis Regional
América del Norte
América del Norte ocupa la posición dominante en el mercado de Pruebas Rápidas de Diagnóstico de Influenza (RIDT) con una participación estimada del 38%, respaldada por una infraestructura sanitaria avanzada, una fuerte adopción de pruebas descentralizadas y programas robustos de vigilancia de la influenza. Los altos volúmenes de pruebas en hospitales, centros de atención urgente y clínicas minoristas amplifican la demanda de productos, mientras que las estructuras de reembolso favorables fomentan el uso clínico generalizado. La región se beneficia de una fuerte supervisión regulatoria, una rápida adopción de tecnología y sostenidas inversiones en I+D que mejoran la precisión diagnóstica. La creciente conciencia sobre las pruebas autoadministradas y la integración de kits rápidos basados en lectores digitales fortalecen aún más la expansión del mercado en Estados Unidos y Canadá.
Europa
Europa representa aproximadamente el 27% del mercado de RIDT, impulsada por políticas de salud pública coordinadas, una alta cobertura de vacunación contra la influenza y un fuerte énfasis en la detección temprana de infecciones respiratorias. Países como Alemania, el Reino Unido y Francia lideran la adopción debido a redes de diagnóstico bien establecidas y una creciente penetración de plataformas de pruebas rápidas digitales. Los brotes de gripe estacionales y el envejecimiento de la población contribuyen a una mayor demanda de pruebas. El enfoque de la región en diagnósticos de alto rendimiento y estándares de calidad estrictos impulsa la innovación de los fabricantes. La expansión de los programas de pruebas en el punto de atención liderados por farmacias y las mejores vías de reembolso apoyan el continuo crecimiento del mercado en Europa Occidental y Oriental.
Asia-Pacífico
Asia-Pacífico captura casi el 24% del mercado de RIDT, respaldada por el aumento de la prevalencia de la influenza, la expansión de la infraestructura de diagnóstico y la rápida urbanización. Los principales mercados como China, Japón, Corea del Sur e India invierten fuertemente en plataformas de pruebas rápidas para abordar la alta densidad de población y los riesgos de brotes estacionales. La creciente conciencia sobre el diagnóstico temprano, el aumento del gasto en salud y los programas gubernamentales de vigilancia aceleran la adopción en instalaciones de atención primaria y a nivel comunitario. Los fabricantes se benefician de una fuerte demanda de RIDTs de bajo costo y alto rendimiento adaptados a diversos entornos clínicos. La gran base de pacientes de la región y los modelos de clínicas minoristas en evolución continúan expandiendo la penetración del mercado.
América Latina
América Latina representa aproximadamente el 7% del mercado de RIDT, impulsada por un creciente énfasis en la gestión de enfermedades infecciosas y el aumento de las tasas de pruebas de influenza en Brasil, México, Argentina y Chile. El crecimiento se acelera a medida que los gobiernos fortalecen la vigilancia de enfermedades respiratorias y mejoran la accesibilidad diagnóstica en instalaciones de salud públicas y privadas. Los hospitales urbanos lideran la adopción, mientras que las clínicas comunitarias expanden gradualmente el uso de pruebas rápidas inmunocromatográficas. La infraestructura de laboratorio limitada en áreas rurales aumenta la dependencia de RIDTs asequibles en el punto de atención. Las limitaciones económicas siguen siendo un desafío, pero los programas de adquisición ampliados y las asociaciones con empresas internacionales de diagnóstico apoyan el desarrollo constante del mercado.
Oriente Medio y África
La región de Oriente Medio y África representa una participación estimada del 4%, reflejando mejoras graduales en la capacidad sanitaria y una creciente conciencia sobre el cribado de la influenza. Países del Golfo como Arabia Saudita y los Emiratos Árabes Unidos invierten en tecnologías diagnósticas avanzadas y expanden las capacidades de pruebas rápidas en hospitales, aeropuertos e instalaciones de salud ocupacional. En África, la demanda está impulsada por la necesidad de RIDTs asequibles y fáciles de usar debido a la limitada infraestructura de pruebas moleculares. Las iniciativas internacionales de salud apoyan la distribución en clínicas primarias, mientras que el aumento de la inversión del sector privado acelera la adopción. Sin embargo, las limitaciones presupuestarias y las inconsistencias en la cadena de suministro moderan el crecimiento general del mercado.
Segmentaciones del Mercado:
Por Tipo de Producto:
- RIDTs Convencionales
- RIDTs Digitales
Por Tecnología:
- Ensayos inmunocromatográficos
- Ensayos de flujo lateral
Por Tipo de Muestra:
- Hisopo nasal
- Hisopo de garganta
Por Geografía
- América del Norte
- Europa
- Alemania
- Francia
- Reino Unido
- Italia
- España
- Resto de Europa
- Asia Pacífico
- China
- Japón
- India
- Corea del Sur
- Sudeste Asiático
- Resto de Asia Pacífico
- América Latina
- Brasil
- Argentina
- Resto de América Latina
- Oriente Medio y África
- Países del CCG
- Sudáfrica
- Resto de Oriente Medio y África
Panorama Competitivo
El panorama competitivo del mercado de Pruebas de Diagnóstico Rápido de Influenza (RIDT) incluye jugadores como Thermo Fisher Scientific, Inc., SEKISUI Diagnostics, F. Hoffmann-La Roche Ltd, Abbott Laboratories, Meridian Bioscience, Inc., Hologic, Inc., Quidel Corporation, SA Scientific Ltd, Becton, Dickinson and Company (BD), y 3M Company. El mercado de Pruebas de Diagnóstico Rápido de Influenza (RIDT) se define por avances continuos en tecnologías de detección rápida de antígenos, expansión de capacidades de pruebas en el punto de atención, y creciente integración de plataformas de diagnóstico digital. Las empresas se centran en mejorar la sensibilidad de las pruebas, permitiendo decisiones clínicas más rápidas y apoyando programas de vigilancia de la influenza a gran escala. La diferenciación de productos se centra en la precisión mejorada de los ensayos, formatos fáciles de usar y compatibilidad con entornos de prueba descentralizados como farmacias, centros de atención urgente y entornos domésticos. Las robustas inversiones en I+D, las aprobaciones regulatorias para kits rápidos de próxima generación y las colaboraciones estratégicas con proveedores de salud fortalecen la posición en el mercado. A medida que la gestión de enfermedades respiratorias evoluciona, los fabricantes priorizan la producción escalable, la expansión de canales de distribución y soluciones conectadas a datos para satisfacer la demanda global.
Análisis de Jugadores Clave
- Thermo Fisher Scientific, Inc.
- SEKISUI Diagnostics
- Hoffmann-La Roche Ltd
- Abbott Laboratories
- Meridian Bioscience, Inc.
- Hologic, Inc.
- Quidel Corporation
- SA Scientific Ltd
- Becton, Dickinson and Company (BD)
- 3M Company
Desarrollos Recientes
- En octubre de 2024, la FDA aprobó el Healgen Rapid Check COVID-19/Flu A&B Antigen Test para su comercialización. Esta prueba casera, que utiliza un hisopo nasal, puede detectar tanto COVID-19 como influenza A & B. Está disponible sin receta y ofrece resultados en solo 15 minutos. Esta es la primera prueba de gripe de venta libre que recibe autorización de comercialización fuera del uso de emergencia.
- En junio de 2024, el NIH a través de su Programa de Evaluación Independiente de Pruebas RADx Tech (ITAP), trabajó con fabricantes de diagnósticos para acelerar la revisión y aprobación de pruebas multiplex que detectan tanto COVID-19 como gripe A/B. Este esfuerzo tiene como objetivo aumentar la disponibilidad de pruebas rápidas, en el punto de atención (POC) y caseras, que son esenciales para un diagnóstico y tratamiento rápidos.
- En mayo de 2024, Danaher colaboró con la Universidad John Hopkins para desarrollar nuevos métodos para diagnosticar lesiones cerebrales traumáticas. Los científicos de la Universidad John Hopkins se centrarían en evaluar nuevos biomarcadores basados en sangre aprovechando la tecnología altamente sensible de Beckmann Coulter.
- En marzo de 2024, la empresa conjunta de Co-Diagnostics, Inc., CoSara, recibió la aprobación de los reguladores indios para su Prueba Multiplex PCR de Influenza. Esta prueba puede detectar múltiples cepas de influenza al mismo tiempo, convirtiéndola en una herramienta de diagnóstico más eficiente para los proveedores de atención médica. Esta aprobación es un paso significativo hacia la mejora del acceso a pruebas de diagnóstico avanzadas en India.
Shape Your Report to Specific Countries or Regions & Enjoy 30% Off!
Cobertura del Informe
El informe de investigación ofrece un análisis en profundidad basado en Tipo de Producto, Tecnología, Tipo de Muestra y Geografía. Detalla a los principales actores del mercado, proporcionando una visión general de su negocio, ofertas de productos, inversiones, fuentes de ingresos y aplicaciones clave. Además, el informe incluye perspectivas sobre el entorno competitivo, análisis FODA, tendencias actuales del mercado, así como los principales impulsores y restricciones. Asimismo, discute varios factores que han impulsado la expansión del mercado en los últimos años. El informe también explora la dinámica del mercado, escenarios regulatorios y avances tecnológicos que están moldeando la industria. Evalúa el impacto de factores externos y cambios económicos globales en el crecimiento del mercado. Por último, proporciona recomendaciones estratégicas para nuevos entrantes y empresas establecidas para navegar por las complejidades del mercado.
Perspectivas Futuras
- El mercado se expandirá a medida que los sistemas de salud prioricen la detección rápida y precisa de la influenza estacional y pandémica.
- La adopción de RIDTs digitales y basados en lectores aumentará para mejorar la precisión de la interpretación y la conectividad de datos.
- Los paneles respiratorios multiplex ganarán tracción ya que los médicos prefieren la detección de múltiples patógenos con una sola muestra.
- Las pruebas rápidas de influenza en el hogar y OTC verán un fuerte crecimiento impulsado por las crecientes tendencias de autodiagnóstico.
- Las farmacias y clínicas minoristas desempeñarán un papel más importante en las pruebas de influenza a través de la expansión de puntos de atención.
- Los fabricantes invertirán en ensayos de mayor sensibilidad para competir con las alternativas de pruebas moleculares.
- Los gobiernos fortalecerán los programas de vigilancia de la influenza, impulsando mayores volúmenes de adquisición de pruebas.
- Los mercados emergentes acelerarán la adopción a medida que mejoren la infraestructura diagnóstica y la concienciación.
- Aumentarán las colaboraciones estratégicas entre desarrolladores de diagnósticos y redes de salud.
- La sostenibilidad y la producción rentable se volverán importantes a medida que la demanda se desplace hacia kits rápidos para el mercado masivo.

 Análisis de Segmentación del Mercado:
Análisis de Segmentación del Mercado:

