Markedsoversigt:
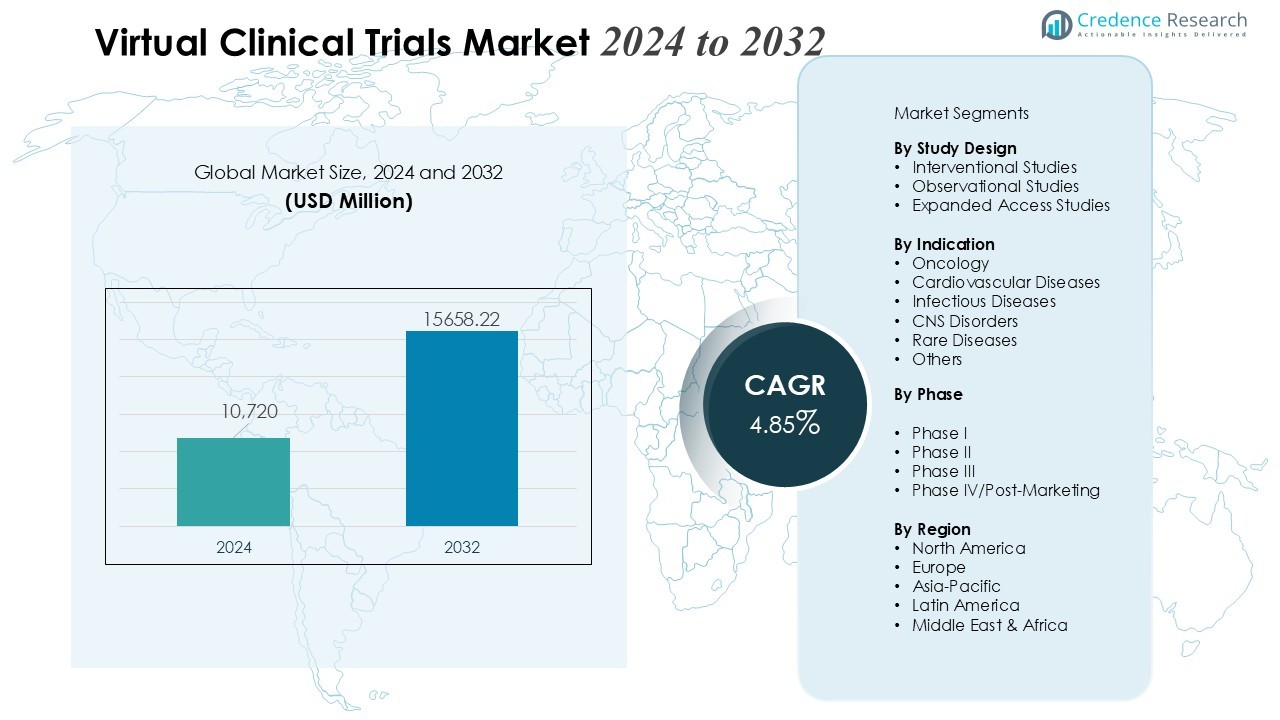
Markedet for virtuelle kliniske forsøg blev værdsat til 10.720 millioner USD i 2024 og forventes at nå 15.658,22 millioner USD i 2032, med en CAGR på 4,85 % i prognoseperioden.
| RAPPORT ATTRIBUT |
DETALJER |
| Historisk Periode |
2020-2023 |
| Basisår |
2024 |
| Prognoseperiode |
2025-2032 |
| Markedsstørrelse for Virtuelle Kliniske Forsøg 2024 |
USD 10.720 Millioner |
| Virtuelle Kliniske Forsøg, CAGR |
4,85% |
| Markedsstørrelse for Virtuelle Kliniske Forsøg 2032 |
USD 15.658,22 Millioner |
Flere drivkræfter former markedets momentum, ledet af behovet for at reducere forsøgsomkostninger, forbedre patientdiversitet og øge fastholdelsesrater. Sponsorer prioriterer virtuelle og hybride tilgange for at strømline dataindsamling, udvide geografisk rækkevidde og minimere patientbelastning. Fremskridt inden for bærbare biosensorer, realtidsdataanalyse og cloud-baserede elektroniske kliniske resultatvurderinger (eCOA) forbedrer dataens nøjagtighed og operationel effektivitet. Øget fokus på patientcentrerede forskningsmodeller og stigende støtte fra regulerende myndigheder fremmer yderligere adoption.
Regionalt har Nordamerika en førende andel på grund af stærk digital sundhedsinfrastruktur, høje investeringer i F&U og tidlig integration af decentraliserede forsøgsplatforme. Europa opretholder betydelig deltagelse drevet af støttende reguleringsharmonisering og udvidede fjernforsøgskapaciteter. Asien-Stillehavet registrerer den hurtigste vækst, understøttet af store patientpuljer, stigende internetpenetration og stigende farmaceutiske outsourcingaktiviteter.
Access crucial information at unmatched prices!
Request your sample report today & start making informed decisions powered by Credence Research Inc.!
Download Sample
Markeds Indsigt:
- Markedet for Virtuelle Kliniske Forsøg forventes at vokse fra USD 10.720 millioner i 2024 til USD 15.658,22 millioner i 2032, understøttet af en CAGR på 4,85%, hvilket afspejler en stabil global adoption af decentraliserede studiemodeller.
- Den stigende efterspørgsel efter patientcentreret forskning accelererer optagelsen, hvor fjernadgang forbedrer rekruttering, fastholdelse og diversitet på tværs af komplekse terapeutiske områder.
- Omkostningseffektivitetskrav driver stærk adoption, da decentraliserede designs reducerer siteomkostninger, strømliner arbejdsgange og forkorter forsøgsforløb for sponsorer.
- Fremskridt inden for digitale sundhedsteknologier—herunder wearables, telehealth, mobilapps og realtidsmonitorering—forbedrer datanøjagtighed og operationel synlighed.
- Reguleringsmyndigheder støtter i stigende grad decentraliserede og hybride modeller og tilbyder klarere vejledning om digitale endepunkter, eConsent og fjernindsamling af data.
- Væsentlige udfordringer vedvarer på grund af regulatoriske forskelle, bekymringer om dataintegritet, begrænset standardisering og inkonsekvent digital infrastruktur på tværs af globale regioner.
- Nordamerika fører i adoption, Europa udvider med stærk regulatorisk harmonisering, og Asien-Stillehavet registrerer den hurtigste vækst på grund af store patientpuljer og stigende digital konnektivitet.
 Markeds Drivere:
Markeds Drivere:
Stigende Efterspørgsel efter Patientcentrerede Forskningsmodeller
Markedet for Virtuelle Kliniske Forsøg får stærkt momentum fra branchens skift mod patientcentrering. Sponsorer sigter mod at reducere byrden ved rejser, lange sitebesøg og begrænset planlægningsfleksibilitet. Det understøtter bredere deltagelse ved at muliggøre fjernengagement og realtidskommunikation. Patientkomfort forbedrer rekrutteringsresultater og styrker fastholdelsesrater på tværs af komplekse terapeutiske områder.
- For eksempel brugte Sage Bionetworks’ mPower-studie en iPhone-app til sporing af Parkinsons sygdomsprogression og gennemførte hele det observationsbaserede forsøg eksternt med informeret samtykke og målinger. Initiativet engagerede 9.500 deltagere med succes.
Stigende Behov for Omkostningseffektivitet og Hurtigere Forsøgstidslinjer
Farmaceutiske og bioteknologiske virksomheder øger adoptionen af decentraliserede tilgange for at sænke driftsomkostningerne. Markedet for Virtuelle Kliniske Forsøg drager fordel af reducerede siteomkostninger, strømlinede arbejdsgange og optimeret ressourceallokering. Det accelererer datainsamlingscyklusser og forbedrer forsøgsoversigt for sponsorer og efterforskere. Hurtigere tilmelding og færre forsinkelser styrker den samlede udviklingsproduktivitet.
- For eksempel reducerede en sponsor i et fase II-forsøg ved brug af parallel siteaktivering, som beskrevet af Gen Li, sites fra 29 til 20, hvilket sparer over $250.000 i aktiverings- og vedligeholdelsesomkostninger.
Fremskridt inden for Digitale Sundhedsteknologier og Realtidsmonitorering
Integration af telehealth-platforme, biosensorer, mobilapplikationer og fjernmonitoreringsenheder transformerer forsøgsudførelse. Markedet for Virtuelle Kliniske Forsøg udnytter disse løsninger til at forbedre datanøjagtighed og patientoverholdelse. Det muliggør kontinuerlig sporing af fysiologiske markører og leverer rigere evidenssæt til klinisk evaluering. Forbedret interoperabilitet og cloud-baserede systemer skaber stærkere digitale økosystemer til storskala studier.
Regulatorisk Støtte og Udvidet Global Accept af Decentraliserede Modeller
Regulerende myndigheder på tværs af større markeder opfordrer til hybride og fuldt virtuelle protokoller for at forbedre forsøgsadgang og modstandsdygtighed. Markedet for virtuelle kliniske forsøg drager fordel af klare vejledningsrammer, styrket datastyring og forbedrede valideringsstandarder for digitale værktøjer. Det fremmer bredere tillid i industrien og accelererer global implementering af decentraliserede tilgange. Harmoniserede standarder og grænseoverskridende samarbejde øger sponsorernes adoption på tværs af flere terapeutiske domæner.
Markedstendenser:
Udvidelse af hybride forsøgsmodeller og øget brug af fjernpatientteknologier
Hybride modeller repræsenterer en stor tendens på markedet for virtuelle kliniske forsøg, understøttet af bredere integration af fjern- og stedbaserede processer. Sponsorer implementerer fleksible forsøgsrammer for at balancere digital bekvemmelighed med nødvendige personlige vurderinger. Det styrker rekruttering blandt forskellige patientgrupper og udvider studieadgang på tværs af geografisk spredte befolkninger. Wearables, mobile sundhedsapps og fjern-diagnostiske værktøjer forbedrer dataflow og reducerer opfølgningshuller. Realtidsindsigt i patientfremskridt muliggør hurtigere beslutningstagning for forskningsteams. Vækst i cloud-tilsluttede endpoints understøtter også protokoloverholdelse og reducerer operationel friktion.
- For eksempel indskrev Pfizers primære globale fase II/III COVID-19-vaccineforsøg (BNT162b2) over 44.000 deltagere på cirka 150 steder og overvågede sikkerhed ved hjælp af en kombination af metoder, herunder deltager-rapporterede elektroniske dagbøger for forventede reaktioner og løbende, observatør-blindet klinisk overvågning af stedets personale og en uafhængig data- og sikkerhedsovervågningskomité for alle bivirkninger og alvorlige bivirkninger.
Adoption af AI-drevne analyser, automatisering og avancerede datavalideringsteknikker
Kunstig intelligens, maskinlæring og automatiserede datastyringssystemer former den næste fase af markedet for virtuelle kliniske forsøg. Sponsorer anvender prædiktive analyser til at optimere patientmatchning, identificere risikomønstre og forfine protokolkompleksitet. Det fremskynder datakvalitetskontroller og forbedrer pålideligheden af resultatvurderinger. Automatisering reducerer manuel indgriben og styrker overholdelse af regulatoriske forventninger. Digitale platforme introducerer stærkere valideringslag for eCOA, ePRO og sensorbaserede datasæt. Bredere integration af decentraliserede platforme understøtter global forsøgsudvidelse og øger tilliden til fjernbevisgenerering.
- For eksempel integrerer Clinions AI-drevne platform flere datakilder, reducerer forsøgsforløb gennem intelligent automatisering, samtidig med at dataintegriteten opretholdes på tværs af 100+ globale studier.
Markedsudfordringer Analyse:
Regulatoriske kompleksiteter, dataintegritetsbekymringer og begrænset standardisering
Markedet for virtuelle kliniske forsøg står over for vedvarende udfordringer på grund af varierende regulatoriske fortolkninger på tværs af regioner. Sponsorer håndterer forskellige forventninger til digitale endpoints, fjernsamtykke og enhedsvalidering. Det øger behovet for præcis dokumentation og stærkere revisionsspor. Dataintegritetsbekymringer opstår, når flere digitale værktøjer opererer på tværs af fragmenterede systemer. Begrænset standardisering for virtuelle arbejdsprocesser forsinker protokoltilpasning og øger overholdelsesrisici. Integrationsforsinkelser og inkonsekvente retningslinjer begrænser bredere adoption af fuldt decentraliserede modeller.
Teknologiske barrierer, patienternes digitale kløft og operationelle begrænsninger
Forskelle i digital læsefærdighed, enhedstilgang og forbindelsesmuligheder skaber store hindringer for patientdeltagelse. Interessenter i markedet for virtuelle kliniske forsøg identificerer mangler i træning, onboarding og teknisk support til forskellige befolkningsgrupper. Det kræver konsekvent fejlfinding og højere ressourceallokering for at opretholde patientengagement. Sponsorer står over for operationelle begrænsninger, når digitale platforme mangler interoperabilitet eller sikre dataudvekslingsveje. Cybersikkerhedsrisici kræver kontinuerlige opgraderinger og strenge styringsrammer. Begrænset parathed på stedet og ujævn teknologiinfrastruktur bremser momentum for store virtuelle implementeringer.
Markedsmuligheder:
Udvidelse af digitale terapier, fjernovervågningsmuligheder og præcisionsmedicinforsøg
Markedet for virtuelle kliniske forsøg skaber stærke muligheder gennem fremkomsten af digitale terapier og præcisionsbehandlingsmodeller. Sponsorer forfølger fjernovervågningsstrategier for at indfange rigere, kontinuerlige data fra forskellige patientgrupper. Det understøtter protokoldesign, der kræver hyppige vurderinger og personlige interventioner. Vækst i bærbar teknologi og AI-drevne analyser styrker evidensgenerering for kroniske og sjældne sygdomme. Bredere accept af decentraliserede modeller åbner adgang til globale befolkninger, som traditionelle forsøg ofte udelukker. Stærkere digitale økosystemer muliggør problemfri integration af eCOA, sensordata og telemedicinske tjenester.
Skalering af hybride forsøgsrammer, global rekrutteringsrækkevidde og realtidsdataplatforme
Hybride modeller leverer nye muligheder ved at kombinere site-baseret tilsyn med digitalt aktiveret engagement. Deltagere i markedet for virtuelle kliniske forsøg opnår fleksibilitet til at udvide sig ud over geografiske begrænsninger og rekruttere underrepræsenterede befolkningsgrupper. Det forbedrer studiens effektivitet ved at understøtte kontinuerlig kommunikation og fjernopfølgning. Realtidsdataplatforme muliggør hurtigere fortolkning af kliniske endepunkter og fremskynder beslutningstagning. Stærkere interoperabilitet understøtter multinationale forsøg og reducerer operationelle forsinkelser. Digital modenhed på tværs af sundhedssystemer baner vejen for bredere implementering af decentraliserede tilgange.
Markedssegmenteringsanalyse:
Efter studiedesign
Markedet for virtuelle kliniske forsøg registrerer stærk adoption på tværs af observations-, interventions- og udvidede adgangsmodeller. Sponsorer prioriterer observationsstudier på grund af minimale krav til stedet og bredere patientrækkevidde. Interventionsstudier vinder momentum med forbedrede fjernovervågningsværktøjer og strukturerede dataarbejdsgange. Det understøtter protokolovertagelse, mens det reducerer deltagerbyrden. Udvidede adgangsprogrammer drager fordel af hurtigere tilmelding og bredere geografisk inklusion.
- For eksempel integrerer Science 37’s RPM-suite med wearables til realtidsmonitorering af vitale tegn i decentraliserede forsøg, hvilket muliggør AI-drevne advarsler, der identificerer tidlige risikosignaler på tværs af globale fase II–IV studier.
Efter indikation
Kroniske sygdomme, onkologi og sjældne lidelser dominerer indikationslandskabet på grund af høj efterspørgsel efter kontinuerlig datainfangelse og patientcentrerede modeller. Markedet for virtuelle kliniske forsøg oplever stærk tiltrækning i onkologi, hvor komplekse endepunkter kræver realtidsmonitorering. Det forbedrer patientoverholdelse og udvider berettigelsen blandt fjerntliggende eller mobilitetsbegrænsede grupper. Kroniske sygdomsforsøg drager fordel af bærbare biosensorer og digitale overholdelsesværktøjer. Sjældne sygdomsstudier får adgang til globale befolkninger, som traditionelle steder sjældent når.
- For eksempel opnåede Dexcom G6 kontinuerlig glukosemonitor en gennemsnitlig absolut relativ forskel (MARD) på 9,0% i glukosemålinger for diabetesstyringsforsøg.
Efter fase
Tidlige og sene faseforsøg udnytter begge decentraliserede tilgange for effektivitet og forbedret evidensgenerering. Markedet for virtuelle kliniske forsøg ser stærk deltagelse i fase II og fase III studier, understøttet af store stikprøvestørrelser og behov for langsigtet opfølgning. Det muliggør hurtigere dataverifikation og stabile fastholdelsesrater. Fase I studier anvender hybride designs for at balancere sikkerhedstilsyn med digitale værktøjer. Post-marketing studier anvender virtuelle platforme til at overvåge virkelige resultater på tværs af forskellige befolkninger.
Segmenteringer:
Efter studiedesign
- Interventionelle studier
- Observationsstudier
- Udvidede adgangsstudier
Efter indikation
- Onkologi
- Kardiovaskulære sygdomme
- Infektionssygdomme
- CNS-lidelser
- Sjældne sygdomme
- Andre
Efter fase
- Fase I
- Fase II
- Fase III
- Fase IV/Post-marketing
Efter region
- Nordamerika
- Europa
- Tyskland
- Frankrig
- Storbritannien
- Italien
- Spanien
- Resten af Europa
- Asien og Stillehavsområdet
- Kina
- Japan
- Indien
- Sydkorea
- Sydøstasien
- Resten af Asien og Stillehavsområdet
- Latinamerika
- Brasilien
- Argentina
- Resten af Latinamerika
- Mellemøsten & Afrika
- GCC-lande
- Sydafrika
- Resten af Mellemøsten og Afrika
Regional analyse:
Stærkt markedslederskab i Nordamerika med høj integration af digital sundhed
Nordamerika opretholder en førende position på markedet for virtuelle kliniske forsøg, understøttet af stærk digital sundhedsinfrastruktur og høje R&D-udgifter fra store farmaceutiske virksomheder. Sponsorer i USA fremskynder adoptionen af decentraliserede og hybride modeller for at forbedre rekruttering og reducere forsinkelser i forsøg. Det drager fordel af modne telehealth-netværk, bred EHR-integration og stærke interoperabilitetsstandarder. Regulatorisk klarhed fra FDA styrker industriens tillid og udvider accepten af virtuelle protokoller. Avanceret brug af AI-drevne analyser, realtidsmonitoreringsværktøjer og forbundne medicinske enheder understøtter storskala implementering. Canada bidrager med stabil vækst gennem samarbejdende forskningsnetværk og forbedret digital parathed på tværs af sundhedsinstitutioner.
Udvidet regulatorisk støtte og hurtig decentralisering på tværs af Europa
Europa registrerer betydelig deltagelse drevet af harmoniserede regulatoriske rammer og stærke nationale sundhedssystemer. Regionen fremmer decentraliserede modeller for at forbedre patientadgang og strømline grænseoverskridende forsøgsudførelse. Interessenter på markedet for virtuelle kliniske forsøg drager fordel af regionens vægt på datastyring og sikre digitale platforme. Det drager fordel af stærk optagelse i Tyskland, Storbritannien og Norden på grund af høj digital modenhed. Vækst i fjernovervågningsværktøjer og eConsent-platforme understøtter effektive studiearbejdsgange. Stigende investeringer i præcisionsmedicin og forskning i sjældne sygdomme udvider mulighederne for virtuelle og hybride forsøgsdesigns.
Hurtigst vækst i Asien og Stillehavsområdet understøttet af store patientgrupper og udvidet konnektivitet
Asien-Stillehavet leverer den højeste vækstrate understøttet af store, forskelligartede patientpopulationer og stigende efterspørgsel efter tilgængelig klinisk forskning. Lande som Kina, Japan, Indien og Sydkorea styrker den digitale sundhedsinfrastruktur for at fremskynde adoptionen af decentraliserede forsøg. Deltagere på markedet for virtuelle kliniske forsøg udnytter regionens stærke rekrutteringspotentiale og hurtige urbanisering. Det drager fordel af forbedret bredbåndsadgang, højere smartphone-penetration og udvidede telemedicinnetværk. Regeringsinitiativer og offentligt-private samarbejder understøtter generering af digitale beviser og forbedrer regulatorisk tilpasning. Voksende outsourcing-aktiviteter og stigende biopharma-investeringer positionerer Asien-Stillehavet som et strategisk knudepunkt for udvidelse af virtuelle forsøg.
Nøglespilleranalyse:
- ICON, plc
- Parexel International Corporation
- IQVIA
- Covance
- PRA Health Sciences
- LEO Innovation Lab
- Medidata
- Oracle
- CRF Health
- Clinical Ink
- Medable, Inc.
- Signant Health
- Halo Health Systems
- Croprime
Konkurrenceanalyse:
Konkurrencelandskabet på markedet for virtuelle kliniske forsøg omfatter store CRO’er, teknologileverandører og digitale sundhedsinnovatører, der udvider decentraliserede kapaciteter gennem avancerede platforme og stærke globale netværk. Nøglespillere inkluderer ICON plc, Parexel International Corporation, IQVIA, Covance, PRA Health Sciences, LEO Innovation Lab og Medidata. Disse virksomheder investerer i AI-drevne analyser, fjernovervågningsværktøjer og samlede eClinical-platforme for at styrke forsøgets effektivitet og datanøjagtighed. Det understøtter hurtigere tilmelding, bredere geografisk rækkevidde og forbedret patientfastholdelse på tværs af komplekse terapeutiske områder. Strategiske partnerskaber med biotekfirmaer, enhedsproducenter og teknologileverandører hjælper med at udvide serviceporteføljer og forbedre leveringen af virtuelle protokoller. Konkurrencefokus centrerer sig om interoperabilitet, regulatorisk tilpasning og differentierede patientengagementværktøjer, der forbedrer skalerbarhed og styrker markedslederskab.
Seneste udviklinger:
- I august 2025 annoncerede IQVIA et langsigtet klinisk og kommercielt partnerskab med Veeva Systems.
- I oktober 2025 udvidede Parexel sit Global Site Alliance Program og opnåede 40% hurtigere site-aktivering og fire gange flere patienttilmeldinger pr. site.
Shape Your Report to Specific Countries or Regions & Enjoy 30% Off!
Rapportdækning:
Forskningsrapporten tilbyder en dybdegående analyse baseret på studiedesign, indikation, fase og region. Den beskriver førende markedsaktører og giver et overblik over deres forretning, produkttilbud, investeringer, indtægtsstrømme og nøgleapplikationer. Derudover inkluderer rapporten indsigter i det konkurrenceprægede miljø, SWOT-analyse, aktuelle markedstendenser samt de primære drivkræfter og begrænsninger. Endvidere diskuterer den forskellige faktorer, der har drevet markedsudvidelse i de seneste år. Rapporten udforsker også markedsdynamik, regulatoriske scenarier og teknologiske fremskridt, der former industrien. Den vurderer virkningen af eksterne faktorer og globale økonomiske ændringer på markedsvækst. Endelig giver den strategiske anbefalinger til nye aktører og etablerede virksomheder for at navigere i markedets kompleksiteter.
Fremtidsperspektiv:
- Stigningen i hybride og fuldt decentraliserede modeller vil styrke den langsigtede adoption på tværs af terapeutiske områder.
- Udvidelsen af fjernovervågningsenheder og AI-værktøjer vil forbedre datakvaliteten og fremskynde beslutningscyklusser.
- Global rekrutteringsrækkevidde vil forbedres, når sponsorer engagerer forskellige patientpopulationer gennem digitale platforme.
- Interoperabilitet blandt eClinical-systemer vil fremme og understøtte problemfri evidensintegration.
- Regulatoriske rammer vil udvikle sig mod klarere valideringsstandarder for digitale endepunkter og fjernprocedurer.
- Væksten i præcisionsmedicinske forsøg vil øge efterspørgslen efter højfrekvent, realtidsdatainnsamling.
- Investering i cybersikkerhed og tillidsskabende teknologier vil forbedre interessenternes tillid til virtuelle modeller.
- Stærkere samarbejde mellem CRO’er, teknologileverandører og biopharma-virksomheder vil drive innovation.
- Patientengagementplatforme vil forbedre fastholdelse og reducere protokolafvigelsesrater i komplekse studier.
- Udvidelse på nye markeder vil fremskynde skalerbarheden af virtuelle forsøg og øge global implementering.

 Markeds Drivere:
Markeds Drivere:

