Introduction
1.1. Description du Rapport
1.2. Objectif du Rapport
1.3. USP & Offres Clés
1.4. Principaux Avantages pour les Parties Prenantes
1.5. Public Cible
1.6. Portée du Rapport
1.7. Portée Régionale
Portée et Méthodologie
2.1. Objectifs de l’Étude
2.2. Parties Prenantes
2.3. Sources de Données
2.3.1. Sources Primaires
2.3.2. Sources Secondaires
2.4. Estimation du Marché
2.4.1. Approche Ascendante
2.4.2. Approche Descendante
2.5. Méthodologie de Prévision
Résumé Exécutif
Introduction
4.1. Aperçu
4.2. Principales Tendances de l’Industrie
Marché Mondial des Essais Cliniques Virtuels
5.1. Aperçu du Marché
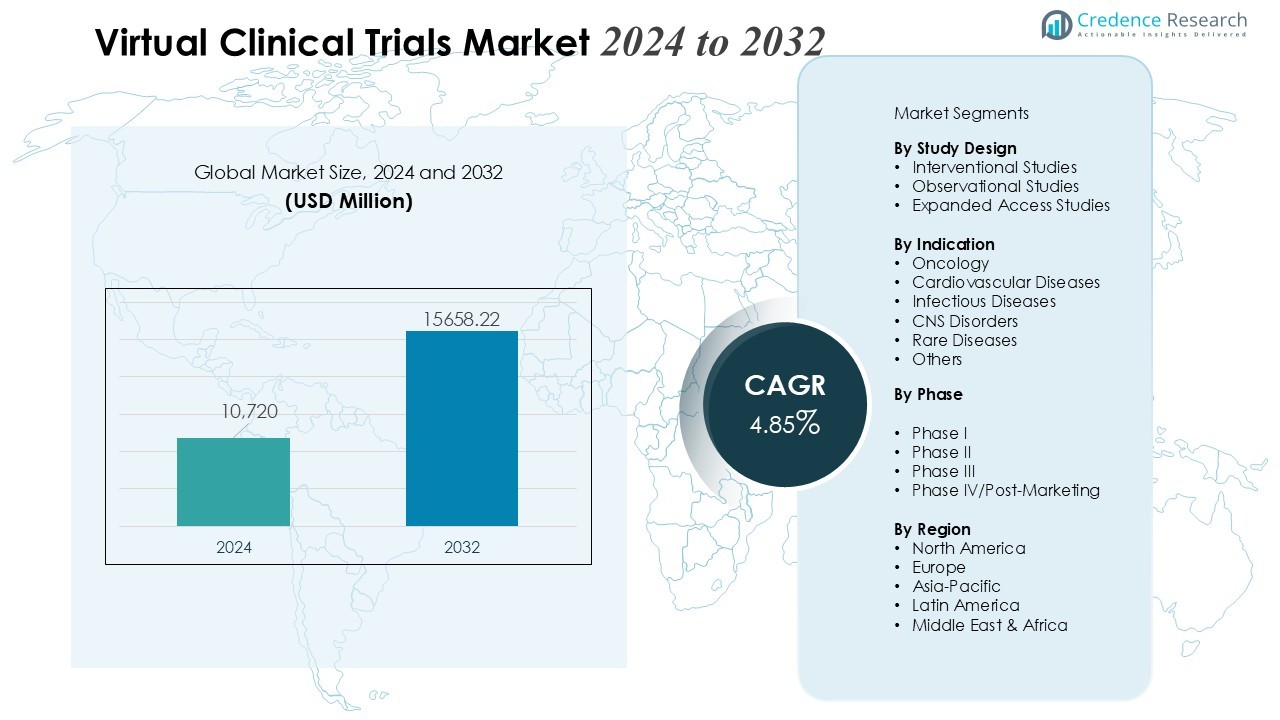
5.2. Performance du Marché
5.3. Impact de la COVID-19
5.4. Prévisions du Marché
6. Répartition du Marché par Conception d’Étude
6.1. Études Interventionnelles
6.1.1. Tendances du Marché
6.1.2. Prévisions du Marché
6.1.3. Part de Revenu
6.1.4. Opportunité de Croissance des Revenus
6.2. (Pas de données fournies)
6.2.1. Tendances du Marché
6.2.2. Prévisions du Marché
6.2.3. Part de Revenu
6.2.4. Opportunité de Croissance des Revenus
6.3. Études Observationnelles
6.3.1. Tendances du Marché
6.3.2. Prévisions du Marché
6.3.3. Part de Revenu
6.3.4. Opportunité de Croissance des Revenus
6.4. 6.4.1. Tendances du Marché
6.4.2. Prévisions du Marché
6.4.3. Part de Revenu
6.4.4. Opportunité de Croissance des Revenus
6.5. Études d’Accès Élargi
6.5.1. Tendances du Marché
6.5.2. Prévisions du Marché
6.5.3. Part de Revenu
6.5.4. Opportunité de Croissance des Revenus
6.6. 6.6.1. Tendances du Marché
6.6.2. Prévisions du Marché
6.6.3. Part de Revenu
6.6.4. Opportunité de Croissance des Revenus
6.7. 6.7.1. Tendances du Marché
6.7.2. Prévisions du Marché
6.7.3. Part de Revenu
6.7.4. Opportunité de Croissance des Revenus
7. Répartition du Marché par Indication
7.1. Oncologie
7.1.1. Tendances du Marché
7.1.2. Prévisions du Marché
7.1.3. Part de Revenu
7.1.4. Opportunité de Croissance des Revenus
7.2. 7.2.1. Tendances du Marché
7.2.2. Prévisions du marché
7.2.3. Part de revenu
7.2.4. Opportunité de croissance des revenus
7.3. Maladies cardiovasculaires
7.3.1. Tendances du marché
7.3.2. Prévisions du marché
7.3.3. Part de revenu
7.3.4. Opportunité de croissance des revenus
7.4. 7.4.1. Tendances du marché
7.4.2. Prévisions du marché
7.4.3. Part de revenu
7.4.4. Opportunité de croissance des revenus
7.5. Maladies infectieuses
7.5.1. Tendances du marché
7.5.2. Prévisions du marché
7.5.3. Part de revenu
7.5.4. Opportunité de croissance des revenus
7.6. 7.6.1. Tendances du marché
7.6.2. Prévisions du marché
7.6.3. Part de revenu
7.6.4. Opportunité de croissance des revenus
7.7. Troubles du SNC
7.7.1. Tendances du marché
7.7.2. Prévisions du marché
7.7.3. Part de revenu
7.7.4. Opportunité de croissance des revenus
7.8. Maladies rares
7.8.1. Tendances du marché
7.8.2. Prévisions du marché
7.8.3. Part de revenu
7.8.4. Opportunité de croissance des revenus
8. Répartition du marché par application
8.1. Phase I
8.1.1. Tendances du marché
8.1.2. Prévisions du marché
8.1.3. Part de revenu
8.1.4. Opportunité de croissance des revenus
8.2. 8.2.1. Tendances du marché
8.2.2. Prévisions du marché
8.2.3. Part de revenu
8.2.4. Opportunité de croissance des revenus
8.3. Phase II
8.3.1. Tendances du marché
8.3.2. Prévisions du marché
8.3.3. Part de revenu
8.3.4. Opportunité de croissance des revenus
8.4. 8.4.1. Tendances du marché
8.4.2. Prévisions du marché
8.4.3. Part de revenu
8.4.4. Opportunité de croissance des revenus
8.5. Phase III
8.5.1. Tendances du marché
8.5.2. Prévisions du marché
8.5.3. Part de revenu
8.5.4. Opportunité de croissance des revenus
8.6. —
8.6.1. Tendances du marché
8.6.2. Prévisions du marché
8.6.3. Part de revenu
8.6.4. Opportunité de croissance des revenus
8.7. Phase IV / Post-commercialisation
8.7.1. Tendances du marché
8.7.2. Prévisions du marché
8.7.3. Part de revenu
8.7.4. Opportunité de croissance des revenus
8.8. Immunologie (segment supplémentaire fourni)
8.8.1. Tendances du marché
8.8.2. Prévisions du marché
8.8.3. Part de revenu
8.8.4. Opportunité de croissance des revenus
9. Répartition du marché par région
(Conservé selon le modèle)
10–15. Sections standard du rapport
Analyse SWOT
Analyse de la chaîne de valeur
Analyse des cinq forces de Porter
Analyse des prix
Paysage concurrentiel
14.1. Structure du marché
14.2. Acteurs clés
14.3. Profils des acteurs clés
14.3 Profils des acteurs clés
Ci-dessous, tous les acteurs clés que vous avez fournis sont insérés séquentiellement :
14.3.1. ICON plc
14.3.2. Parexel International Corporation
14.3.3. IQVIA
14.3.4. Covance
14.3.5. PRA Health Sciences
14.3.6. LEO Innovation Lab
14.3.7. Medidata
14.3.8. Oracle
14.3.9. CRF Health
14.3.10. Clinical Ink
14.3.11. Medable, Inc.
14.3.12. Signant Health
14.3.13. Halo Health Systems
14.3.14. Croprime
14.3.15. NeuroSky
Chaque profil comprend :
- Présentation de l’entreprise
- Portefeuille de produits
- Données financières
- Analyse SWOT

 Moteurs du Marché :
Moteurs du Marché :

