Panoramica del Mercato CDMO dei Prodotti Medicinali di Terapia Avanzata (ATMP):
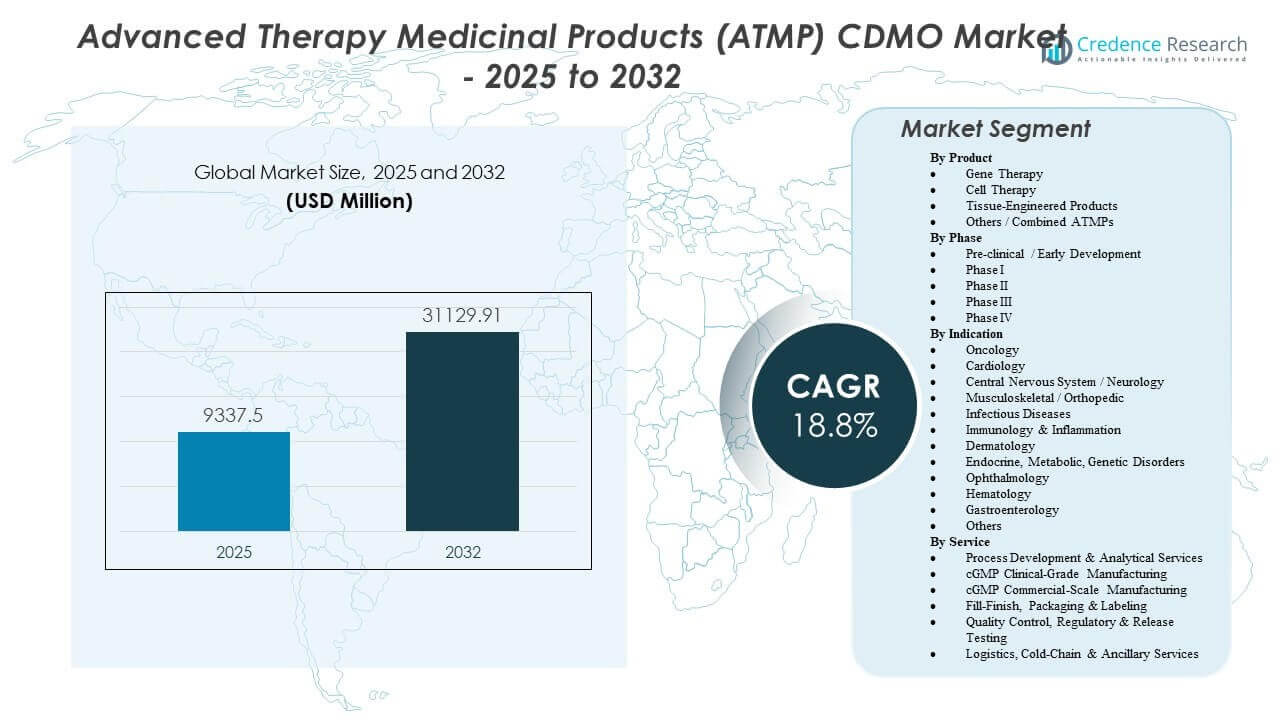
Il mercato CDMO dei Prodotti Medicinali di Terapia Avanzata (ATMP) è previsto crescere da 9.337,5 milioni di USD nel 2025 a un valore stimato di 31.129,91 milioni di USD entro il 2032, con un tasso di crescita annuale composto (CAGR) del 18,8% dal 2025 al 2032.
| ATTRIBUTO DEL RAPPORTO |
DETTAGLI |
| Periodo Storico |
2020-2024 |
| Anno Base |
2025 |
| Periodo di Previsione |
2026-2032 |
| Dimensione del Mercato CDMO dei Prodotti Medicinali di Terapia Avanzata (ATMP) 2025 |
9.337,5 milioni di USD |
| Mercato CDMO dei Prodotti Medicinali di Terapia Avanzata (ATMP), CAGR |
18,8% |
| Dimensione del Mercato CDMO dei Prodotti Medicinali di Terapia Avanzata (ATMP) 2032 |
31.129,91 milioni di USD |
Approfondimenti sul Mercato CDMO dei Prodotti Medicinali di Terapia Avanzata (ATMP):
- Forti pipeline cliniche e crescente commercializzazione degli ATMP alimentano la domanda di vettori virali, produzione scalabile di terapie cellulari e servizi GMP specializzati tra gli sviluppatori globali.
- Alti bisogni di capitale, competenze interne limitate e requisiti normativi complessi rimangono vincoli chiave che spingono gli sponsor verso l’esternalizzazione ma creano sfide operative per le aziende più piccole.
- Il Nord America guida il mercato grazie a un ecosistema biotecnologico maturo e capacità di produzione avanzate, mentre l’Europa segue con solidi quadri normativi e hub di vettori consolidati.
- L’Asia Pacifico emerge come la regione in più rapida crescita, supportata dall’espansione delle infrastrutture GMP, investimenti strategici e crescente coinvolgimento degli attori biotecnologici regionali nello sviluppo degli ATMP.
Fattori Trainanti del Mercato CDMO dei Prodotti Medicinali di Terapia Avanzata (ATMP)
Rapida Espansione dei Programmi Clinici di Terapia Cellulare e Genica in Principali Aree Terapeutiche
Le pipeline di terapia cellulare e genica continuano ad espandersi in oncologia e malattie rare. Gli sponsor avanzano più candidati nelle fasi II e III dei trial. Questo cambiamento aumenta la domanda di capacità di produzione clinica e commerciale. Il mercato CDMO dei Prodotti Medicinali di Terapia Avanzata (ATMP) guadagna slancio da questa profondità di pipeline. Gli sviluppatori richiedono piattaforme scalabili per vettori virali e processi cellulari. La prontezza commerciale richiede sistemi di produzione convalidati e riproducibili. Contratti a lungo termine garantiscono la continuità della fornitura per terapie approvate. Un forte supporto degli investitori alimenta ulteriormente l’attività di esternalizzazione.
- Ad esempio, Novartis ha riportato oltre 6.000 pazienti globali trattati con la sua terapia CAR-T Kymriah®, riflettendo una crescente domanda clinica e commerciale.
Access crucial information at unmatched prices!
Request your sample report today & start making informed decisions powered by Credence Research Inc.!
Download Sample
Capacità di Produzione Interna Limitate tra le Aziende Biotecnologiche Emergenti
Molte piccole e medie imprese biotecnologiche mancano di infrastrutture GMP. Le strutture di produzione interne richiedono un alto capitale iniziale e competenze regolatorie. Gli sponsor preferiscono CDMO esperti per gestire flussi di produzione complessi. L’outsourcing riduce il rischio operativo e accelera i tempi di sviluppo. Partner specializzati forniscono supporto nell’ingegneria dei vettori e nelle analisi. La capacità flessibile consente ai clienti di adattarsi ai risultati delle sperimentazioni. Le partnership strategiche migliorano l’efficienza in tutte le fasi di sviluppo. Strategie asset-light rafforzano la disciplina finanziaria.
Requisiti Normativi Complessi E Standard Di Qualità Rigorosi
I prodotti ATMP affrontano una rigorosa supervisione normativa nei principali mercati. La documentazione richiede una convalida dettagliata e dati di qualità. I CDMO offrono conoscenze normative e prontezza all’ispezione. Gli sponsor si affidano a sistemi di qualità consolidati per ridurre il rischio di approvazione. Procedure standardizzate supportano prestazioni di prodotto coerenti. L’esperienza in conformità migliora la credibilità con le autorità. La mitigazione del rischio diventa centrale nelle fasi cliniche avanzate. Solidi quadri di qualità guidano la preferenza per l’outsourcing.
Crescente Commercializzazione Delle Terapie Avanzate Approvate
Le terapie geniche e cellulari approvate si espandono in programmi di accesso più ampio per i pazienti. La fornitura commerciale richiede una capacità di produzione stabile e ad alto volume. I CDMO investono in suite GMP ampliate per soddisfare questa esigenza. Gli sponsor danno priorità a partner di produzione affidabili. Il trasferimento tecnologico dalla scala clinica a quella commerciale richiede competenza. La gestione del ciclo di vita supporta una presenza di mercato sostenuta. Gli impegni post-approvazione aumentano la complessità operativa. La crescita commerciale sostiene la domanda a lungo termine per i CDMO.
- Ad esempio, Catalent Cell & Gene Therapy ha ampliato la produzione di AAV per Zolgensma presso la sua struttura di Harmans, Maryland, un sito di 200.000 piedi quadrati dotato di 18 suite cGMP che supportano i programmi di terapia genica globale di Novartis.
Tendenze Del Mercato CDMO Dei Prodotti Medicinali Di Terapia Avanzata (ATMP)
Spostamento Verso Offerte Di Servizi Integrati End-To-End
I clienti cercano partner unici che gestiscano lo sviluppo fino alla commercializzazione. I CDMO ampliano i portafogli per includere analisi, riempimento-finitura e logistica. I modelli integrati migliorano il coordinamento tra le fasi del progetto. Gli sponsor riducono la frammentazione dei fornitori e l’onere di supervisione. I servizi completi rafforzano la fidelizzazione dei clienti. L’integrazione verticale migliora la differenziazione competitiva. Le alleanze strategiche pluriennali sostituiscono i contratti a breve termine. I modelli di servizio consolidati migliorano l’efficienza operativa.
Adozione Di Automazione E Piattaforme Di Produzione Chiuse
L’automazione migliora la precisione nell’espansione cellulare e nella produzione di vettori. I sistemi chiusi riducono il rischio di contaminazione e la variabilità manuale. La robotica migliora la riproducibilità tra i lotti specifici per il paziente. I controlli digitali rafforzano la supervisione dei processi. L’automazione riduce la dipendenza dall’intervento manuale. I sistemi standardizzati supportano la produzione allogenica scalabile. Gli aggiornamenti tecnologici aumentano l’utilizzo delle strutture. L’efficienza operativa migliora grazie agli strumenti di produzione intelligenti.
Diversificazione Geografica Dell’Impronta Di Produzione
Le CDMO si espandono nell’Asia Pacifico e nei centri biotecnologici emergenti. Le strutture regionali riducono il rischio logistico e i tempi di consegna. I governi supportano gli investimenti biotecnologici attraverso incentivi. La capacità locale rafforza la resilienza della catena di approvvigionamento. Gli sponsor cercano reti di produzione diversificate. Le partnership transfrontaliere accelerano l’ingresso nel mercato. L’esperienza regionale migliora l’allineamento normativo. La diffusione geografica migliora la competitività globale.
- Ad esempio, FUJIFILM Diosynth Biotechnologies ha ampliato le sue capacità globali acquisendo l’impianto di produzione di biologici su larga scala a Hillerød, Danimarca, che include sei bioreattori in acciaio inossidabile da 15.000 litri e supporta la produzione commerciale di biologici per clienti globali.
Investimento In Piattaforme Di Vettori E Cellule Di Nuova Generazione
L’innovazione nei sistemi AAV e lentivirali aumenta l’efficienza. Le piattaforme di produzione ad alto rendimento migliorano la scalabilità. Le terapie cellulari allogeniche attirano attenzione per un uso più ampio. Le analisi avanzate migliorano l’ottimizzazione dei processi. I sistemi di bioreattori innovativi migliorano la coerenza dei risultati. Le tecnologie di piattaforma riducono i tempi di sviluppo. Il miglioramento continuo guida la differenziazione del servizio. L’attenzione all’innovazione garantisce un potenziale di crescita a lungo termine.
- Ad esempio, AGC Biologics ha introdotto le piattaforme BravoAAV™ e ProntoLVV™, utilizzando bioprocessi di sospensione scalabili fino a 2.000 L per AAV e 1.000 L per LVV per aumentare l’efficienza della produzione di vettori. Questi sistemi predefiniti riducono i tempi di prontezza GMP a circa nove mesi, supportando un avanzamento più rapido dei programmi di terapia genica.
Analisi Delle Sfide Del Mercato CDMO Dei Prodotti Medicinali Di Terapia Avanzata (ATMP)
Vincoli Di Capacità E Collo Di Bottiglia Nella Produzione Di Vettori Virali
L’offerta di vettori virali rimane limitata in diverse regioni. I tempi di consegna per plasmidi e materie prime estendono le tempistiche dei progetti. L’espansione delle strutture richiede ispezioni e validazioni normative. Il mercato CDMO dei Prodotti Medicinali di Terapia Avanzata (ATMP) è sotto pressione per soddisfare la domanda urgente. La logistica della catena del freddo aggiunge complessità alla distribuzione globale. La carenza di personale specializzato rallenta i piani di espansione. Gli standard di conformità alla qualità rimangono rigorosi e richiedono molte risorse. Gli sponsor si aspettano una rapida esecuzione e risultati costanti. Bilanciare domanda e offerta rimane una sfida chiave.
Variabilità Normativa E Strutture Di Costi Elevati Nei Mercati Globali
I percorsi normativi differiscono tra le principali regioni. Gli standard di documentazione richiedono dati di validazione estensivi. Gli audit di conformità richiedono team di qualità dedicati. I costi operativi elevati influenzano le strategie di prezzo. I piccoli sviluppatori affrontano pressioni di finanziamento durante i ritardi clinici. La volatilità delle valute influenza i contratti transfrontalieri. I rischi di proprietà intellettuale complicano le partnership. Le negoziazioni contrattuali coinvolgono termini dettagliati di condivisione del rischio. Questi fattori aumentano la pressione operativa sui CDMO.
Opportunità Del Mercato CDMO Dei Prodotti Medicinali Di Terapia Avanzata (ATMP)
Espansione Nei Centri Biotecnologici Emergenti E Piattaforme Di Produzione Regionali
I cluster biotecnologici emergenti investono in infrastrutture avanzate per i biologici. I governi forniscono incentivi per attrarre strutture ATMP. Il mercato CDMO dei Prodotti Medicinali di Terapia Avanzata (ATMP) può espandersi attraverso partnership regionali. La produzione locale riduce il rischio e il costo logistico. I siti GMP regionali supportano un accesso più rapido per i pazienti. Le joint venture creano modelli di investimento condivisi. I programmi di trasferimento tecnologico rafforzano l’expertise locale. L’ingresso anticipato nei nuovi mercati garantisce contratti a lungo termine. La diversificazione geografica migliora la resilienza.
Crescita delle Piattaforme Allogeniche e delle Tecnologie dei Vettori di Nuova Generazione
Le terapie allogeniche mirano a una produzione scalabile pronta all’uso. Le linee cellulari standardizzate semplificano i flussi di lavoro di produzione. Le nuove piattaforme vettoriali migliorano l’efficienza di trasduzione. I sistemi di sospensione ad alta capacità aumentano la produzione. Le analisi avanzate riducono i tempi di rilascio. Le tendenze della medicina personalizzata supportano la produzione di terapie di nicchia. I gemelli digitali migliorano l’ottimizzazione dei processi. Gli investimenti strategici nell’innovazione creano differenziazione. Questi sviluppi aprono nuovi percorsi di entrate per i CDMO.
Analisi della Segmentazione del Mercato CDMO dei Prodotti Medicinali di Terapia Avanzata (ATMP):
Per Prodotto
Il panorama dei prodotti copre la terapia genica, la terapia cellulare, i prodotti ingegnerizzati tissutali e gli ATMP combinati. Nel mercato CDMO dei Prodotti Medicinali di Terapia Avanzata (ATMP), la terapia genica ha una forte domanda grazie a piattaforme basate su vettori virali come i sistemi AAV e lentivirali. Questi vettori supportano pipeline per malattie rare e oncologia. La terapia cellulare include formati CAR-T, cellule staminali e non staminali nei modelli autologhi e allogenici. Le terapie autologhe richiedono una produzione specifica per il paziente, mentre le piattaforme allogeniche mirano alla scala. I prodotti ingegnerizzati tissutali si basano su impalcature e matrici per la riparazione strutturale. Le terapie ibride gene-cellula e le impalcature biodegradabili ampliano le opzioni di trattamento complesso.
- Ad esempio, WuXi Advanced Therapies ha lanciato la tecnologia OXGENE TESSA™ per la produzione di AAV, che elimina la necessità di trasfezione con plasmidi e ha dimostrato un aumento di 10 volte nella resa di AAV rispetto ai metodi tradizionali di tripla trasfezione.
Per Fase
Le fasi di sviluppo vanno dal pre-clinico e dallo sviluppo iniziale alla Fase I fino alla Fase IV. I programmi in fase iniziale si concentrano sulla progettazione del processo e sulla validazione della sicurezza. Le Fasi I e II enfatizzano l’ottimizzazione della dose e la produzione controllata in lotti. La Fase III richiede volumi maggiori e sistemi GMP validati. La Fase IV supporta la fornitura post-approvazione e la gestione del ciclo di vita. Gli sponsor aumentano l’outsourcing nelle fasi successive per garantire la prontezza commerciale. La mitigazione del rischio e la conformità normativa diventano critiche nelle fasi avanzate. I CDMO allineano la capacità con la progressione clinica.
Per Indicazione
L’oncologia guida grazie all’elevata adozione di terapie CAR-T e modificate geneticamente. La cardiologia e la neurologia si espandono attraverso programmi rigenerativi e basati sui geni. I segmenti muscoloscheletrici e ortopedici utilizzano impalcature ingegnerizzate tissutali per la riparazione. Le malattie infettive e l’immunologia sfruttano l’editing genetico e la modulazione immunitaria. La dermatologia e l’oftalmologia supportano modelli di consegna genica localizzata. I disturbi endocrini e genetici si basano su correzioni geniche durature. L’ematologia rimane centrale per la domanda di vettori virali e cellule staminali. La gastroenterologia e altre indicazioni creano esigenze di produzione di nicchia.
Per Servizio
Le offerte di servizi spaziano dallo sviluppo dei processi al supporto logistico. I servizi di sviluppo dei processi e analitici costruiscono flussi di lavoro scalabili e conformi. La produzione clinica di grado cGMP supporta le sperimentazioni in fase iniziale e intermedia. La produzione su scala commerciale richiede strutture validate e sistemi di approvvigionamento robusti. Il riempimento, il confezionamento e l’etichettatura garantiscono l’integrità del prodotto. Il controllo qualità e i test normativi mantengono gli standard di conformità. La logistica della catena del freddo gestisce materiali sensibili alla temperatura. I modelli di servizio integrati migliorano l’efficienza nei cicli di sviluppo.
- Ad esempio, i servizi Patheon di Thermo Fisher Scientific hanno introdotto il programma Quick to Care™, integrando la produzione di sostanze e prodotti farmaceutici con il confezionamento clinico per semplificare i flussi di lavoro dello sviluppo iniziale. La piattaforma consente alle aziende biotecnologiche emergenti di accelerare la prontezza per la fornitura clinica consolidando passaggi che tradizionalmente richiedono più partner di servizio.
Segmentazione:
Per Prodotto
- Terapia Genica
- Basata su Vettori Virali
- Terapia Cellulare
- CAR-T
- Cellule Staminali
- Non Cellule Staminali
- Autologa
- Allogenica
- Prodotti di Ingegneria Tissutale
- Altri / ATMP Combinati
- Gene-Cellulare Ibrido
- Scaffold Biodegradabili
Per Fase
- Pre-clinica / Sviluppo Iniziale
- Fase I
- Fase II
- Fase III
- Fase IV
Per Indicazione
- Oncologia
- Cardiologia
- Sistema Nervoso Centrale / Neurologia
- Muscoloscheletrico / Ortopedico
- Malattie Infettive
- Immunologia & Infiammazione
- Dermatologia
- Disturbi Endocrini, Metabolici, Genetici
- Oftalmologia
- Ematologia
- Gastroenterologia
- Altri
Per Servizio
- Sviluppo dei Processi & Servizi Analitici
- Produzione Clinica di Grado cGMP
- Produzione su Scala Commerciale cGMP
- Riempimento, Confezionamento & Etichettatura
- Controllo Qualità, Normativa & Test di Rilascio
- Logistica, Catena del Freddo & Servizi Ausiliari
Per Regione
- Nord America
- Stati Uniti
- Canada
- Messico
- Europa
- Germania
- Francia
- Regno Unito
- Italia
- Spagna
- Resto d’Europa
- Asia Pacifico
- Cina
- Giappone
- India
- Corea del Sud
- Sud-est asiatico
- Resto dell’Asia Pacifico
- America Latina
- Brasile
- Argentina
- Resto dell’America Latina
- Medio Oriente & Africa
- Paesi del GCC
- Sud Africa
- Resto del Medio Oriente e Africa
Analisi Regionale:
Il Nord America detiene la quota maggiore del mercato dei Prodotti Medicinali di Terapia Avanzata (ATMP) CDMO, rappresentando quasi il 45% delle entrate globali. Il forte finanziamento biotecnologico e l’alta concentrazione di sviluppatori di terapie geniche e cellulari supportano questa dominanza. Gli Stati Uniti guidano la crescita regionale con infrastrutture GMP avanzate e chiari percorsi normativi. Il Canada supporta l’espansione attraverso sovvenzioni per la ricerca e collaborazioni accademiche. L’Europa cattura circa il 30% del mercato, trainata da Germania, Regno Unito e Francia. Solidi quadri EMA e programmi di ricerca transfrontalieri rafforzano la capacità regionale. La regione beneficia di hub consolidati per vettori virali e processi cellulari.
L’Asia Pacifico rappresenta quasi il 20% della quota globale e registra il tasso di espansione più rapido. Cina e Giappone investono pesantemente nella produzione di terapie geniche e nell’innovazione biotecnologica domestica. Corea del Sud e India espandono la capacità GMP attraverso partenariati pubblici e privati. Gli incentivi governativi incoraggiano il trasferimento tecnologico e lo sviluppo di strutture. I costi operativi più bassi attraggono contratti di outsourcing internazionali. La disponibilità di una forza lavoro qualificata migliora la produzione tecnica. Gli attori regionali perseguono alleanze strategiche con aziende biotecnologiche occidentali.
L’America Latina e il Medio Oriente & Africa rappresentano collettivamente quasi il 5% del mercato. Brasile e Messico guidano l’attività in America Latina attraverso iniziative di ricerca clinica. I paesi del GCC investono in infrastrutture sanitarie avanzate e parchi biotecnologici. Il Sud Africa supporta reti regionali di sperimentazione clinica. La penetrazione del mercato rimane limitata a causa di lacune normative e vincoli di finanziamento. Le partnership locali aiutano i CDMO globali ad entrare nei mercati emergenti. Riforme politiche graduali mirano ad attrarre investimenti esteri.
Shape Your Report to Specific Countries or Regions & Enjoy 30% Off!
Analisi dei Giocatori Chiave:
- Lonza Group
- Catalent Inc.
- Thermo Fisher Scientific (Patheon)
- AGC Biologics
- FUJIFILM Diosynth Biotechnologies
- Charles River Laboratories
- Oxford Biomedica PLC
- WuXi Advanced Therapies
- Minaris Regenerative Medicine
- Aldevron
- Samsung Biologics
- Rentschler Biopharma SE
- CELONIC Group
- Eurofins Scientific SE
- RoslinCT
- Andelyn Biosciences
- BlueReg
- CGT Catapult
- Curia Global Inc.
- Bio Elpida by Polyplus
Analisi Competitiva:
Il mercato dei Prodotti Medicinali per Terapie Avanzate (ATMP) CDMO presenta un mix di produttori biotecnologici specializzati e CDMO globali diversificati. I principali attori si concentrano sull’espansione dei vettori virali, l’automazione della terapia cellulare e modelli di servizio integrati. Le aziende investono nell’espansione della capacità in Nord America ed Europa per assicurarsi contratti a lungo termine. Acquisizioni strategiche rafforzano l’expertise tecnica nelle piattaforme AAV e lentivirali. Le partnership con startup biotecnologiche creano accesso anticipato a pipeline ad alto potenziale. Le aziende competono su esperienza regolatoria, tempi di consegna e conformità alla qualità. Offerte integrate che spaziano dallo sviluppo del processo alla produzione commerciale forniscono un forte vantaggio. La competizione sui prezzi rimane secondaria rispetto alla capacità tecnica e affidabilità. L’espansione della capacità e la diversificazione geografica modellano il posizionamento competitivo a lungo termine.
Sviluppi Recenti:
- A gennaio 2024, Pluri, un’azienda biotecnologica israeliana, ha lanciato PluriCDMO, una nuova divisione che offre servizi di produzione di terapie cellulari come organizzazione di sviluppo e produzione a contratto (CDMO), con una struttura GMP di 47.000 piedi quadrati.
- A gennaio 2024, Charles River Laboratories International Inc. ha introdotto la sua offerta di plasmidi Rep/Cap pronti all’uso per semplificare i programmi di terapia genica basati su virus adeno-associati (AAV).
Copertura del Rapporto:
Il rapporto di ricerca offre un’analisi approfondita basata su Prodotto, Fase, Indicazione, Servizio e Regione. Dettaglia i principali attori del mercato, fornendo una panoramica delle loro attività, offerte di prodotti, investimenti, flussi di entrate e applicazioni chiave. Inoltre, il rapporto include approfondimenti sull’ambiente competitivo, analisi SWOT, tendenze di mercato attuali, nonché i principali fattori trainanti e vincoli. Inoltre, discute vari fattori che hanno guidato l’espansione del mercato negli ultimi anni. Il rapporto esplora anche le dinamiche di mercato, gli scenari regolatori e i progressi tecnologici che stanno modellando l’industria. Valuta l’impatto dei fattori esterni e dei cambiamenti economici globali sulla crescita del mercato. Infine, fornisce raccomandazioni strategiche per i nuovi entranti e le aziende consolidate per navigare nelle complessità del mercato.
Prospettive Future:
- La domanda di piattaforme integrate di sviluppo e produzione commerciale rafforzerà le partnership di outsourcing a lungo termine.
- L’espansione dei programmi di terapia cellulare allogenica migliorerà la scalabilità e la standardizzazione nei siti di produzione.
- L’automazione e le tecnologie a sistema chiuso miglioreranno la coerenza dei lotti e ridurranno il rischio operativo.
- L’innovazione nei vettori virali aumenterà l’efficienza di trasduzione e migliorerà i rendimenti di produzione.
- Le alleanze strategiche tra CDMO e startup biotecnologiche accelereranno le transizioni dei programmi in fase iniziale.
- I centri di produzione regionali nell’Asia Pacifico attireranno contratti di fornitura clinica transfrontaliera.
- Le analisi avanzate e i sistemi di qualità digitali supporteranno la conformità normativa e l’integrità dei dati.
- Gli investimenti in strutture GMP modulari forniranno capacità flessibile per pipeline multi-prodotto.
- La crescita nelle pipeline di malattie rare e oncologia sosterrà contratti di servizio ad alto valore.
- La logistica della catena del freddo e le reti di distribuzione specializzate si espanderanno per supportare la commercializzazione globale.




