市场概述:
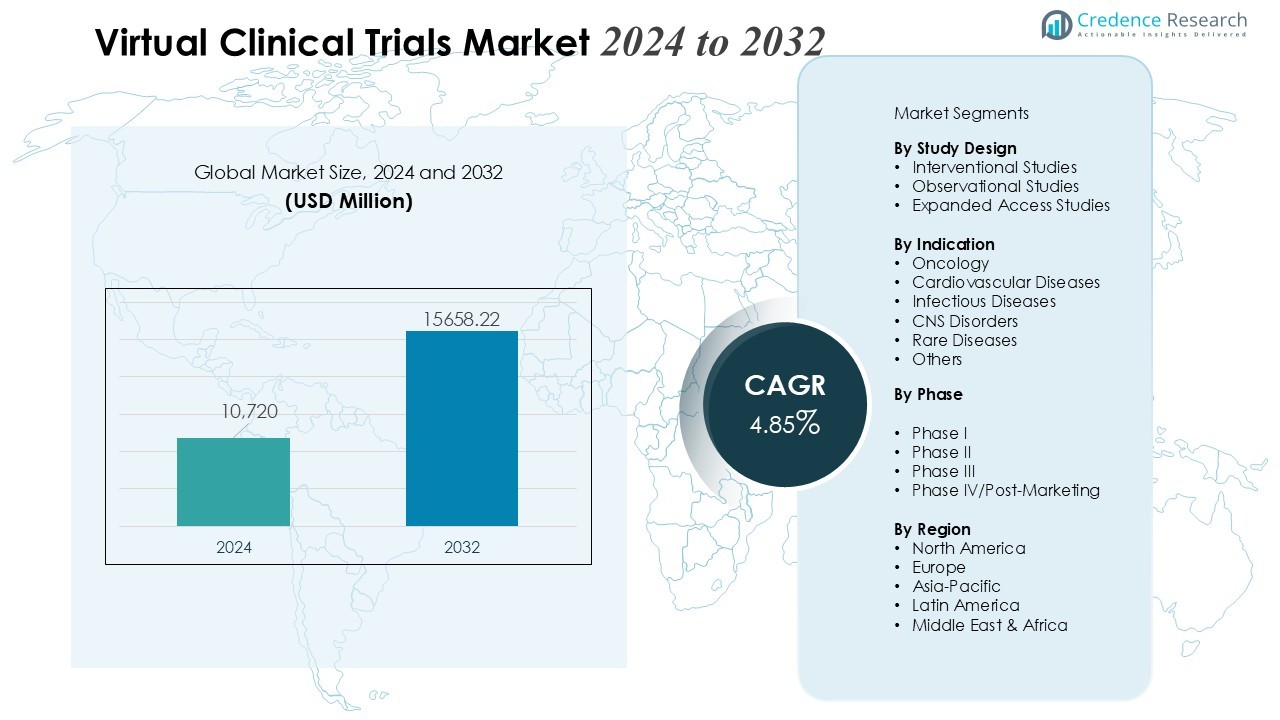
虚拟临床试验市场规模在2024年估值为10,720百万美元,预计到2032年将达到15,658.22百万美元,预测期内的年复合增长率为4.85%。
| 报告属性 |
详细信息 |
| 历史时期 |
2020-2023 |
| 基准年 |
2024 |
| 预测期 |
2025-2032 |
| 2024年虚拟临床试验市场规模 |
10,720百万美元 |
| 虚拟临床试验市场年复合增长率 |
4.85% |
| 2032年虚拟临床试验市场规模 |
15,658.22百万美元 |
多种驱动因素影响市场动向,其中包括降低试验成本、提高患者多样性和增强保留率的需求。赞助商优先采用虚拟和混合方法,以简化数据收集、扩大地理范围并减少患者负担。可穿戴生物传感器、实时数据分析和基于云的电子临床结果评估(eCOA)的进步提高了数据准确性和运营效率。对以患者为中心的研究模型的重视增加以及监管机构的支持进一步提升了采用率。
在区域方面,由于强大的数字健康基础设施、高研发投资和去中心化试验平台的早期整合,北美占据领先份额。欧洲在支持性的监管协调和扩展的远程试验能力的推动下,保持了显著的参与度。亚太地区由于庞大的患者群体、不断扩大的互联网普及率和日益增长的制药外包活动,记录了最快的增长。
Access crucial information at unmatched prices!
Request your sample report today & start making informed decisions powered by Credence Research Inc.!
Download Sample
市场洞察:
- 虚拟临床试验市场预计将从2024年的107.2亿美元增长到2032年的156.5822亿美元,受4.85%的复合年增长率支持,反映出全球对去中心化研究模型的稳步采用。
- 对以患者为中心的研究需求不断增长,加速了采纳率的提高,远程参与改善了复杂治疗领域的招募、保留和多样性。
- 成本效益压力推动了强劲的采用,因为去中心化设计减少了现场开销,简化了工作流程,并缩短了赞助商的试验时间表。
- 数字健康技术的进步——包括可穿戴设备、远程医疗、移动应用和实时监测——提高了数据准确性和运营可见性。
- 监管机构越来越支持去中心化和混合模型,提供了关于数字终点、电子同意和远程数据收集的更明确指导。
- 由于监管差异、数据完整性问题、标准化有限以及全球地区数字基础设施不一致,关键挑战依然存在。
- 北美在采用方面领先,欧洲在强有力的监管协调下扩展,而亚太地区由于庞大的患者群体和日益增长的数字连接性记录了最快的增长。
 市场驱动因素:
市场驱动因素:
对以患者为中心的研究模型的需求增长
虚拟临床试验市场因行业向以患者为中心的转变而获得强劲动力。赞助商旨在减少旅行负担、冗长的现场访问和有限的日程灵活性。通过实现远程参与和实时沟通,它支持更广泛的参与。患者便利性改善了招募结果,并在复杂治疗领域加强了保留率。
- 例如,Sage Bionetworks的mPower研究利用iPhone应用程序跟踪帕金森病的进展,整个观察性试验远程进行,获得知情同意和测量。该项目成功吸引了9500名参与者。
对成本效益和更快试验时间表的需求上升
制药和生物技术公司增加了去中心化方法的采用,以降低运营成本。虚拟临床试验市场受益于减少的现场开销、简化的工作流程和优化的资源分配。它加速了数据收集周期,提高了赞助商和研究人员的试验可见性。更快的入组和更少的延迟加强了整体开发生产力。
- 例如,正如Gen Li所述,在一项使用并行现场激活的II期试验中,赞助商将现场从29个减少到20个,节省了超过25万美元的激活和维护成本。
数字健康技术和实时监测的进步
远程医疗平台、生物传感器、移动应用和远程监测设备的整合改变了试验执行。虚拟临床试验市场利用这些解决方案提高数据准确性和患者依从性。它实现了生理标记的连续跟踪,并为临床评估提供了更丰富的证据集。增强的互操作性和基于云的系统为大规模研究创建了更强大的数字生态系统。
监管支持和去中心化模型的全球接受度扩大
主要市场的监管机构鼓励采用混合和完全虚拟的协议,以提高试验的可及性和弹性。虚拟临床试验市场受益于明确的指导框架、加强的数据治理以及改进的数字工具验证标准。这促进了更广泛的行业信心,加速了去中心化方法的全球部署。协调的标准和跨境合作增加了在多个治疗领域的赞助商采用率。
市场趋势:
混合试验模型的扩展和远程患者技术的增加使用
混合模型代表了虚拟临床试验市场中的一大趋势,得到了远程和现场流程更广泛整合的支持。赞助商实施灵活的试验框架,以平衡数字便利性与必要的面对面评估。它加强了在不同患者群体中的招募,并扩大了地理分散人群的研究访问。可穿戴设备、移动健康应用和远程诊断工具改善了数据流动并减少了随访间隙。对患者进展的实时可见性使研究团队能够更快地做出决策。云连接端点的增长也支持协议遵从性并降低运营摩擦。
- 例如,辉瑞的全球主要II/III期COVID-19疫苗试验(BNT162b2)在大约150个地点招募了超过44,000名参与者,并使用多种方法监测安全性,包括参与者报告的电子日记记录预期反应,以及现场工作人员和独立的数据和安全监测委员会对所有不良和严重不良事件进行的持续、观察者盲法临床监测。
AI驱动的分析、自动化和高级数据验证技术的采用
人工智能、机器学习和自动化数据管理系统塑造了虚拟临床试验市场的下一个阶段。赞助商部署预测分析以优化患者匹配、识别风险模式并优化协议复杂性。它加速了数据质量检查并提高了结果评估的可靠性。自动化减少了人工干预并加强了对监管期望的合规性。数字平台为eCOA、ePRO和基于传感器的数据集引入了更强的验证层。去中心化平台的更广泛整合支持全球试验的可扩展性,并提升了对远程证据生成的信心。
- 例如,Clinion的AI驱动平台整合了多个数据源,通过智能自动化缩短试验时间,同时在100多个全球研究中保持数据完整性。
市场挑战分析:
监管复杂性、数据完整性问题和标准化有限
由于各地区对法规的不同解释,虚拟临床试验市场面临持续的挑战。赞助商管理对数字终点、远程同意和设备验证的多样化期望。这增加了对精确文档和更强审计跟踪的需求。当多个数字工具在分散的系统中运行时,会出现数据完整性问题。虚拟工作流程的标准化有限,减缓了协议对齐并增加了合规风险。集成延迟和不一致的指南限制了完全去中心化模型的更广泛采用。
技术障碍、患者数字鸿沟和运营限制
数字素养、设备访问和连接性的差异为患者参与创造了重大障碍。虚拟临床试验市场的利益相关者识别出在培训、入职和技术支持方面对不同人群的差距。这需要持续的故障排除和更高的资源分配来维持患者的参与。当数字平台缺乏互操作性或安全的数据交换路径时,赞助商面临操作限制。网络安全风险需要持续升级和严格的治理框架。有限的站点准备和不均衡的技术基础设施减缓了大规模虚拟部署的势头。
市场机会:
数字治疗、远程监控能力和精准医学试验的扩展
虚拟临床试验市场通过数字治疗和精准治疗模型的兴起创造了强大的机会。赞助商追求远程监控策略,以从不同患者群体中捕获更丰富、连续的数据。它支持需要高频评估和个性化干预的协议设计。可穿戴技术和AI驱动的分析的增长加强了慢性病和罕见病的证据生成。去中心化模型的更广泛接受为传统试验经常排除的全球人群提供了访问。更强大的数字生态系统允许eCOA、传感器数据和远程医疗服务的无缝集成。
混合试验框架的扩展、全球招募范围和实时数据平台
混合模型通过结合基于站点的监督和数字化参与提供了新的机会。虚拟临床试验市场参与者获得了超越地理限制和招募代表性不足人群的灵活性。它通过支持持续沟通和远程跟进提高了研究效率。实时数据平台允许更快地解释临床终点并加速决策。更强的互操作性支持多国试验并减少操作延迟。医疗系统的数字成熟度为更广泛部署去中心化方法铺平了道路。
市场细分分析:
按研究设计
虚拟临床试验市场在观察性、干预性和扩展访问模型中记录了强劲的采用。由于站点要求最低和更广泛的患者覆盖,赞助商优先考虑观察性研究。随着改进的远程监控工具和结构化数据工作流程,干预性研究正在获得动力。它支持协议遵从性,同时减少参与者负担。扩展访问计划受益于更快的注册和更广泛的地理包容性。
- 例如,Science 37的RPM套件与可穿戴设备集成,用于去中心化试验中的实时生命体征监测,使AI驱动的警报能够识别全球II-IV期研究中的早期风险信号。
按适应症
慢性病、肿瘤学和罕见疾病在适应症领域占主导地位,因为对连续数据捕获和以患者为中心的模型的需求很高。虚拟临床试验市场在肿瘤学领域表现出强劲的吸引力,因为复杂的终点需要实时监控。它提高了患者的依从性,并扩大了远程或行动受限群体的资格。慢性病试验受益于可穿戴生物传感器和数字依从性工具。罕见病研究获得了传统站点很少到达的全球人群的访问。
- 例如,Dexcom G6连续血糖监测仪在糖尿病管理试验中的葡萄糖读数中实现了9.0%的平均绝对相对差异(MARD)。
按阶段
早期阶段和晚期阶段的试验都利用去中心化的方法来提高效率和改善证据生成。虚拟临床试验市场在第二阶段和第三阶段研究中有着强劲的参与,得益于大样本量和长期随访需求。它能够加快数据验证并保持稳定的保留率。第一阶段研究采用混合设计,以平衡安全监督和数字工具。上市后研究利用虚拟平台来监测不同人群的真实世界结果。
细分:
按研究设计
按适应症
- 肿瘤学
- 心血管疾病
- 传染病
- 中枢神经系统疾病
- 罕见病
- 其他
按阶段
按地区
区域分析:
北美市场领导地位强劲,数字健康整合度高
北美在虚拟临床试验市场中保持领先地位,得益于强大的数字健康基础设施和主要制药公司的高研发支出。美国的赞助商加速采用去中心化和混合模型,以提高注册率并减少试验延误。它受益于成熟的远程医疗网络、广泛的电子健康记录整合和强大的互操作性标准。美国食品药品监督管理局的监管明确性增强了行业信心,并扩大了虚拟协议的接受度。先进的AI驱动分析、实时监测工具和联网医疗设备支持大规模部署。加拿大通过协作研究网络和改进的数字化准备度在医疗机构中贡献了稳定的增长。
欧洲的监管支持扩大和快速去中心化
欧洲的参与显著,得益于协调的监管框架和强大的国家医疗系统。该地区推进去中心化模型,以改善患者访问并简化跨境试验执行。虚拟临床试验市场利益相关者从该地区对数据治理和安全数字平台的重视中获益。由于数字成熟度高,德国、英国和北欧国家的接受度强劲。远程监测工具和电子同意平台的增长支持了高效的研究工作流程。对精准医学和罕见病研究的投资增加,为虚拟和混合试验设计拓展了机会。
亚太地区的快速增长得益于庞大的患者群体和不断扩展的连接性
亚太地区通过庞大多样的患者群体和对便捷临床研究的需求增长,提供了最高的增长率。中国、日本、印度和韩国等国家加强数字健康基础设施,以加速去中心化试验的采用。虚拟临床试验市场参与者利用该地区强大的招募潜力和快速城市化。该地区受益于宽带接入的改善、更高的智能手机普及率和扩展的远程医疗网络。政府举措和公私合作支持数字证据生成并增强监管一致性。不断增长的外包活动和生物制药投资使亚太地区成为虚拟试验扩展的战略枢纽。
关键参与者分析:
- ICON, plc
- Parexel International Corporation
- IQVIA
- Covance
- PRA Health Sciences
- LEO Innovation Lab
- Medidata
- Oracle
- CRF Health
- Clinical Ink
- Medable, Inc.
- Signant Health
- Halo Health Systems
- Croprime
竞争分析:
虚拟临床试验市场的竞争格局包括主要的CRO、技术提供商和数字健康创新者,这些公司通过先进的平台和强大的全球网络扩展去中心化能力。关键参与者包括ICON plc、Parexel International Corporation、IQVIA、Covance、PRA Health Sciences、LEO Innovation Lab和Medidata。这些公司投资于AI支持的分析、远程监控工具和统一的电子临床平台,以加强试验效率和数据准确性。它支持更快的招募、更广泛的地理覆盖范围和在复杂治疗领域中提高的患者保留率。与生物技术公司、设备制造商和技术供应商的战略合作伙伴关系有助于扩展服务组合并增强虚拟协议交付。竞争重点集中在互操作性、监管一致性和差异化的患者参与工具上,这些工具提高了可扩展性并加强了市场领导地位。
最新发展:
- 2025年8月,IQVIA宣布与Veeva Systems建立长期临床和商业合作伙伴关系。
- 2025年10月,Parexel扩展了其全球站点联盟计划,实现了40%更快的站点激活和每个站点四倍的患者招募。
Shape Your Report to Specific Countries or Regions & Enjoy 30% Off!
报告覆盖范围:
研究报告基于研究设计、适应症、阶段和地区提供深入分析。它详细介绍了主要市场参与者,概述了他们的业务、产品供应、投资、收入来源和关键应用。此外,报告还包括对竞争环境的见解、SWOT分析、当前市场趋势以及主要驱动因素和限制因素。此外,它讨论了近年来推动市场扩张的各种因素。报告还探讨了塑造行业的市场动态、监管情景和技术进步。它评估了外部因素和全球经济变化对市场增长的影响。最后,它为新进入者和成熟公司提供了战略建议,以应对市场的复杂性。
未来展望:
- 混合和完全去中心化模型的兴起将加强在治疗领域的长期采用。
- 远程监控设备和人工智能工具的扩展将提升数据质量并加速决策周期。
- 随着赞助商通过数字平台吸引多样化的患者群体,全球招募范围将得到改善。
- eClinical系统之间的互操作性将得到提升,并支持无缝证据整合。
- 监管框架将朝着更清晰的数字终点和远程程序验证标准演变。
- 精准医学试验的增长将增加对高频、实时数据收集的需求。
- 对网络安全和信任增强技术的投资将提高利益相关者对虚拟模型的信心。
- CROs、技术供应商和生物制药公司之间更强的合作将推动创新。
- 患者参与平台将改善保留率并减少复杂研究中的方案偏差率。
- 新兴市场的扩展将加速虚拟试验的可扩展性并增加全球部署。

 市场驱动因素:
市场驱动因素:

