Descripción General del Mercado de Validación de Bioprocesos:
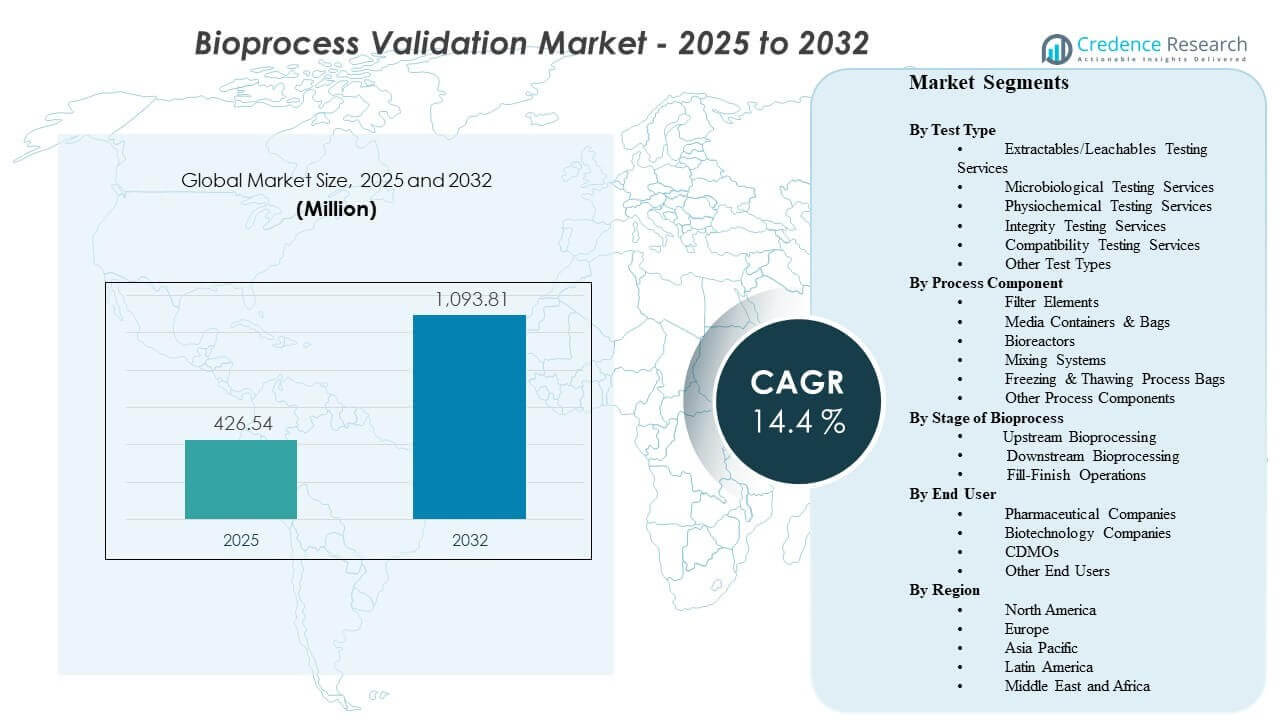
El tamaño del mercado global de Validación de Bioprocesos se estimó en USD 426.54 millones en 2025 y se espera que alcance los USD 1093.81 millones para 2032, creciendo a una tasa compuesta anual (CAGR) del 14.4% de 2025 a 2032. El crecimiento está impulsado principalmente por expectativas más estrictas de calidad y control de contaminación en la fabricación de biológicos, lo que amplía el alcance y la frecuencia de la validación en pasos críticos del proceso y materiales de contacto. La demanda se ve además respaldada por adiciones de capacidad y el crecimiento de la subcontratación que aumentan el volumen de ciclos de calificación, validación de métodos y documentación en redes de fabricación globales.
| ATRIBUTO DEL INFORME |
DETALLES |
| Período Histórico |
2020-2024 |
| Año Base |
2025 |
| Período de Pronóstico |
2026-2032 |
| Tamaño del Mercado de Validación de Bioprocesos 2025 |
USD 426.54 millones |
| Mercado de Validación de Bioprocesos, CAGR |
14.4% |
| Tamaño del Mercado de Validación de Bioprocesos 2032 |
USD 1093.81 millones |
Tendencias y Perspectivas Clave del Mercado
- Se proyecta que el mercado se expanda de USD 426.54 millones (2025) a USD 1093.81 millones (2032) con un CAGR del 14.4% (2025–2032).
- América del Norte representó el 46.9% en 2025, respaldada por una fabricación de biológicos madura y una alta intensidad de cumplimiento.
- Los Servicios de Pruebas de Extractables/Lixiviables tuvieron una participación del 37.4% en 2025, reflejando la amplia adopción de sistemas de un solo uso y expectativas de control de riesgos de impurezas.
- Los Elementos de Filtro representaron el 25.6% de participación en 2025, subrayando el papel central de la garantía estéril y la verificación de integridad en la producción validada.
- Las Empresas Farmacéuticas y Biotecnológicas (combinadas) capturaron el 57.3% de participación en 2025, ya que los patrocinadores mantienen una supervisión directa de actividades críticas de calidad y validación habilitantes para la liberación.
Análisis de Segmentos
La validación de bioprocesos se trata cada vez más como un programa integral que abarca la validación de métodos, la estrategia de control de contaminación y la documentación lista para auditoría en lugar de un conjunto de pruebas aisladas. A medida que las líneas de productos se diversifican y los cambios de proceso ocurren con mayor frecuencia en la ampliación y gestión del ciclo de vida, los paquetes de validación deben ser repetibles, basados en riesgos y compatibles con cronogramas de desarrollo más rápidos. Esto desplaza la demanda hacia protocolos estandarizados, vínculos más estrictos de control de cambios y sistemas de datos que apoyan la trazabilidad en sitios y socios contratados.
Los diseños de adopción de un solo uso y procesamiento intensificado están elevando la importancia de la compatibilidad de materiales, los perfiles de extractables/lixiviables y las pruebas de integridad en todos los componentes de contacto con fluidos. Paralelamente, las expectativas de fabricación estéril en operaciones avanzadas aumentan la carga de validación en las transferencias de aguas arriba a aguas abajo y en los entornos de llenado y acabado. La subcontratación continúa expandiéndose por razones de pruebas especializadas y capacidad, pero los patrocinadores generalmente mantienen la gobernanza interna sobre los criterios de aceptación, desviaciones y documentación dirigida a la regulación.
Access crucial information at unmatched prices!
Request your sample report today & start making informed decisions powered by Credence Research Inc.!
Download Sample
Por Información de Tipo de Prueba
Los Servicios de Pruebas de Extractables/Lixiviables representaron la mayor participación de 37.4% en 2025. Su liderazgo refleja la necesidad de caracterizar posibles impurezas de los materiales de contacto y asegurar la compatibilidad en ensamblajes de un solo uso y rutas de proceso. Los programas de validación requieren cada vez más perfiles defendibles que puedan ser referenciados en cambios de proceso, actualizaciones de proveedores y transiciones de escala. A medida que los plazos de desarrollo se comprimen, los compradores prefieren proveedores que puedan combinar una cobertura analítica robusta con informes claros alineados a las necesidades de documentación de calidad.
Por Información de Componente de Proceso
Los Elementos de Filtro representaron la mayor participación de 25.6% en 2025. Los filtros son centrales para el control de contaminación y la garantía estéril, lo que impulsa la calificación recurrente, las pruebas de integridad y la verificación de lote a lote en la fabricación validada. El segmento se beneficia de la alta frecuencia de uso de filtros en operaciones de aguas arriba y aguas abajo y de la necesidad de validar el rendimiento bajo rangos operativos definidos. Los compradores priorizan la consistencia, la trazabilidad y las afirmaciones de rendimiento bien documentadas que respaldan auditorías y revisiones de calidad internas.
Por Información de Etapa del Bioproceso
El Bioprocesamiento de Aguas Arriba representó la mayor participación de 51.6% en 2025. Las operaciones de aguas arriba suelen experimentar la mayor tasa de ajuste de procesos y cambios de escala, lo que expande la actividad de validación para métodos, planes de muestreo y estrategias de control. Los riesgos de variabilidad en los pasos de etapa temprana también aumentan la dependencia de la validación para demostrar un rendimiento consistente en ejecuciones y sitios. A medida que las organizaciones adoptan enfoques de procesamiento intensificado y cerrado, la validación de aguas arriba enfatiza cada vez más el monitoreo robusto, el control de contaminación y los paquetes de documentación repetibles.
Por Información de Usuario Final
Las Compañías Farmacéuticas y las Compañías de Biotecnología (combinadas) representaron la mayor participación de 57.3% en 2025. Los patrocinadores a menudo retienen la gobernanza central de validación para mantener el control directo sobre los criterios de aceptación, desviaciones y paquetes de evidencia dirigidos a la regulación. Los equipos internos también gestionan decisiones de transferencia de métodos, consideraciones de comparabilidad y actualizaciones de ciclo de vida que desencadenan revalidación. Incluso con una subcontratación más amplia, los patrocinadores generalmente esperan que los socios externos entreguen resultados estandarizados que se integren sin problemas en los sistemas de calidad internos y procesos de auditoría.
Impulsores del Mercado de Validación de Bioprocesos
Expansión de la Fabricación de Biológicos y Adiciones de Capacidad
El crecimiento de la producción de biológicos aumenta el número de instalaciones, líneas y sitios que deben cumplir con las expectativas de estado validado. Cada expansión introduce ciclos de calificación y validación en equipos, servicios y pasos críticos del proceso. Las estrategias de suministro en múltiples sitios aumentan la demanda de paquetes de validación estandarizados y documentación consistente. A medida que las organizaciones escalan más rápido, dependen de marcos de validación repetibles y basados en riesgos para reducir retrasos y evitar interrupciones en los lotes.
- Por ejemplo, Samsung Biologics completó la construcción de la Planta 5 en abril de 2025, añadiendo 180,000 litros de capacidad de biomanufactura y llevando la capacidad total de producción global de la empresa a 845,000 litros en su sitio de Songdo y la instalación recién adquirida de 60,000 litros en Rockville, Maryland, convirtiéndola en la CDMO más grande del mundo por capacidad instalada.
Aumento de las Expectativas de Cumplimiento para el Control de Contaminación y Aseguramiento Estéril
Los requisitos estériles y de baja carga biológica aumentan la intensidad de la validación en los controles de proceso, la verificación de integridad y las estrategias ambientales. Los equipos de calidad esperan cada vez más evidencia de que los riesgos de contaminación están controlados a lo largo de todo el camino del proceso, no solo en los pasos finales. Esto amplía las necesidades de pruebas en microbiología, pruebas de integridad y verificaciones de compatibilidad que respaldan los programas de control de contaminación. La documentación sólida y la trazabilidad son fundamentales para cumplir con las expectativas de auditoría.
Adopción de Uso Único Impulsando la Validación de Materiales y Compatibilidad
El cambio hacia ensamblajes de un solo uso aumenta la necesidad de validar los materiales de contacto, el riesgo de lixiviables y la compatibilidad del proceso en condiciones operativas. La validación debe abordar la variación del proveedor, los cambios en la configuración del ensamblaje y las actualizaciones del ciclo de vida. Los compradores buscan métodos de prueba e informes que puedan reutilizarse en productos y líneas donde sea posible para reducir el esfuerzo repetido. Esta dinámica apoya la demanda sostenida de servicios de pruebas de extractables/lixiviables y compatibilidad.
- Por ejemplo, FUJIFILM Diosynth Biotechnologies replicó con éxito su plataforma de biomanufactura de un solo uso desde Carolina del Norte, EE. UU., a su instalación en Billingham, Reino Unido, en solo 14 meses, entregando la primera instalación de manufactura de un solo uso cGMP del Reino Unido y comenzando operaciones tres meses antes del cronograma original del proyecto, habilitado por paquetes de calificación estandarizados y transferencia de conocimientos entre sitios.
Crecimiento de la Subcontratación y la Necesidad de Capacidad de Validación Escalable
Los patrocinadores utilizan cada vez más socios externos para gestionar las limitaciones de capacidad, métodos especializados y demandas de tiempo de respuesta. La subcontratación puede reducir los cuellos de botella en el desarrollo y el soporte comercial, especialmente durante la ampliación y las transiciones de productos. Sin embargo, las organizaciones de calidad de los patrocinadores aún requieren entregables estandarizados que se ajusten a las necesidades internas de gobernanza y auditoría. Esto impulsa a los proveedores de servicios a diferenciarse en madurez de cumplimiento, calidad de documentación y ejecución consistente.
Desafíos del Mercado de Validación de Bioprocesos
Los programas de validación pueden volverse intensivos en recursos a medida que los menús de pruebas se expanden y aumentan los requisitos de documentación en sitios y socios. Las organizaciones a menudo luchan con la alineación de criterios de aceptación, control de cambios y paquetes de evidencia entre equipos internos y laboratorios subcontratados, lo que puede generar retrabajo y retrasos. Las transferencias de métodos y los cambios de proveedores introducen ciclos adicionales de verificación que son difíciles de estandarizar en huellas de fabricación heterogéneas. Gestionar los plazos sin comprometer la calidad sigue siendo una tensión operativa persistente.
La complejidad también aumenta a medida que las líneas de productos se diversifican y los procesos evolucionan a través de cambios en el ciclo de vida, aumentando la frecuencia de actualizaciones que pueden desencadenar una revalidación parcial. Las expectativas de integridad y trazabilidad de los datos requieren sistemas más sólidos, registros controlados y preparación para auditorías, lo que aumenta los costos generales tanto para los patrocinadores como para los proveedores de servicios. La variabilidad en las expectativas regulatorias regionales y el enfoque de inspección pueden complicar aún más la estandarización global. Estas presiones aumentan la necesidad de gobernanza, plantillas y manuales de validación repetibles.
- Por ejemplo, Bristol Myers Squibb enfrentó la consecuencia operativa directa de la fragmentación del sistema cuando necesitó consolidar un CTMS heredado de Celgene y un CTMS heredado de BMS, dos plataformas separadas con arquitecturas de documentación distintas, en un único sistema de gestión de ensayos unificado a nivel global; la implementación completa en las operaciones globales de la compañía se completó en menos de 20 meses.
Tendencias y Oportunidades del Mercado de Validación de Bioprocesos
Las organizaciones se están moviendo hacia paquetes de validación integrados que vinculan los resultados de pruebas analíticas, microbiológicas y de integridad en estructuras de evidencia listas para auditorías. Esto favorece a los proveedores con amplias capacidades y sistemas de calidad sólidos que pueden ofrecer informes estandarizados en métodos y sitios. También hay una creciente demanda de tiempos de respuesta más rápidos y estructuras de documentación más claras que apoyen ciclos de revisión más rápidos y decisiones de liberación. La habilitación digital para el seguimiento, la tendencia y el control de la documentación se está convirtiendo en un diferenciador práctico en la selección de proveedores.
- Por ejemplo, Eurofins BioPharma Product Testing opera una red de 46 laboratorios GMP armonizados en más de 20 países, todos gobernados por un único Manual de Política de Calidad Global y una plataforma unificada eLIMS-BPT, Cuadernos de Laboratorio Electrónicos (ELN) y un portal centralizado LabAccess℠ para clientes que abarca 28 ubicaciones en todo el mundo, una configuración que permite documentación estandarizada entre sitios e informes listos para auditorías a gran escala.
La expansión de un solo uso y los diseños de procesamiento intensificado están creando oportunidades para marcos de calificación de materiales repetibles que pueden aprovecharse en múltiples productos y plataformas. A medida que la subcontratación se expande, los CDMO y los proveedores de pruebas especializadas pueden crecer ofreciendo soporte de validación de extremo a extremo que reduce la carga de trabajo del patrocinador y comprime los plazos. También está aumentando la demanda de enfoques de validación armonizados que faciliten las transferencias entre múltiples sitios y las actualizaciones del ciclo de vida. Estas tendencias apoyan el crecimiento de las empresas que pueden combinar capacidad con ejecución consistente y de alta conformidad.
Perspectivas Regionales
Norteamérica
América del Norte representó el 46.9% de los ingresos en 2025, respaldada por la fabricación de biológicos establecida, ecosistemas densos de CDMO y alta intensidad de cumplimiento. La demanda regional está impulsada por la frecuente ampliación de escala y la actividad de gestión del ciclo de vida que desencadena la revalidación y las actualizaciones de métodos. Los compradores tienden a priorizar la documentación lista para auditorías, tiempos de respuesta predecibles y ejecución consistente en múltiples instalaciones. La región también apoya una fuerte demanda de pruebas de integridad y flujos de trabajo de validación alineados con el control de contaminación.
Europa
Europa representó el 22.4% de los ingresos en 2025, respaldada por una amplia presencia de fabricación regulada y redes de producción transfronterizas. La demanda de validación se fortalece por la necesidad de paquetes de evidencia estandarizados que puedan utilizarse en cadenas de suministro de múltiples países. Los compradores a menudo enfatizan procedimientos armonizados, sistemas de calidad sólidos y documentación robusta de control de cambios. Los centros de biológicos maduros y los CDMO sostienen una demanda constante en todos los tipos de pruebas y componentes del proceso.
Asia Pacífico
Asia Pacífico contribuyó con el 21.3% de los ingresos en 2025, reflejando la expansión de la capacidad y la creciente participación en redes globales de subcontratación y fabricación. El crecimiento está respaldado por la construcción de nuevas instalaciones, la expansión de plataformas y el aumento de la adopción de sistemas de calidad estandarizados. Los patrocinadores y CDMO en la región buscan cada vez más capacidades de validación escalables con formatos de documentación claros que se alineen con auditorías globales. La demanda es particularmente fuerte donde la adopción de un solo uso y la rápida ampliación de escala aumentan las necesidades de validación de materiales e integridad.
América Latina
América Latina representó el 5.6% de los ingresos en 2025, con la demanda concentrada en torno a la fabricación localizada, actividades de calidad vinculadas a importaciones y centros de producción regionales. Las necesidades de validación a menudo están moldeadas por adiciones de capacidad basadas en proyectos y la mejora de los sistemas de calidad. Los compradores típicamente se enfocan en asegurar documentación conforme y ejecución confiable bajo restricciones de recursos más estrictas. A medida que las capacidades se expanden, se espera que la demanda de validación subcontratada y paquetes de prueba estandarizados se fortalezca.
Oriente Medio y África
Oriente Medio y África representaron el 3.8% de los ingresos en 2025, reflejando una base instalada más pequeña pero un interés creciente en la fabricación localizada y el desarrollo de capacidades estériles. La demanda de validación está típicamente vinculada a nuevos proyectos, mejoras de instalaciones e iniciativas para fortalecer la infraestructura de producción regulada. Los compradores priorizan sistemas de calidad fundamentales, manuales de validación repetibles y apoyo de socios para la preparación de documentación. Se espera que el crecimiento siga el ritmo de la inversión en fabricación y el desarrollo de capacidades.
Panorama Competitivo
La competencia se define por la amplitud de capacidades, la madurez en el cumplimiento, el rendimiento en los plazos de entrega y la capacidad de entregar documentación estandarizada y lista para auditorías que se integra en los sistemas de calidad del patrocinador. Los proveedores se diferencian al ofrecer flujos de trabajo de validación agrupados en pruebas analíticas, microbiológicas y de integridad, junto con soporte de consultoría para el control de cambios y actualizaciones del ciclo de vida. La escala, las redes de laboratorios geográficos y la ejecución consistente en todos los sitios son clave para los grandes programas biofarmacéuticos y las estrategias de fabricación en múltiples sitios. Los proveedores de servicios también compiten en especialización en áreas de alta escrutinio, como el control de contaminación, la compatibilidad de materiales y las pruebas de soporte de liberación.
Thermo Fisher Scientific Inc. está posicionada en tecnologías y servicios habilitadores que apoyan el bioprocesamiento validado, con fortaleza en flujos de trabajo integrados que abarcan la bioproducción, los análisis y el soporte de calidad. El enfoque de la empresa generalmente enfatiza la amplitud del portafolio y la capacidad de apoyar prácticas estandarizadas en entornos de desarrollo y fabricación. Esto se alinea bien con la demanda de los compradores de marcos de validación repetibles que se pueden aplicar en diferentes sitios y productos. Las capacidades de escala e integración pueden apoyar un despliegue más rápido de soluciones de validación y estructuras de documentación consistentes.
El informe de investigación y crecimiento de la industria incluye análisis detallados del panorama competitivo del mercado e información sobre empresas clave, incluyendo:
Se ha realizado un análisis cualitativo y cuantitativo de las empresas para ayudar a los clientes a comprender el entorno empresarial más amplio, así como las fortalezas y debilidades de los principales actores de la industria. Los datos se analizan cualitativamente para categorizar a las empresas como de juego puro, enfocadas en categorías, enfocadas en la industria y diversificadas; se analizan cuantitativamente para categorizar a las empresas como dominantes, líderes, fuertes, tentativas y débiles.
Shape Your Report to Specific Countries or Regions & Enjoy 30% Off!
Desarrollos Recientes
- En abril de 2025, Sartorius Stedim Biotech entró en una asociación estratégica con Tulip Interfaces para acelerar la transformación digital en la fabricación biofarmacéutica. Sartorius dijo que la colaboración está destinada a reducir los errores de procesos manuales, mejorar la visibilidad de la biomanufactura de extremo a extremo y apoyar el cumplimiento regulatorio en entornos de bioprocesamiento de un solo uso.
- En marzo de 2025, Cytiva amplió su cartera de la plataforma Xcellerex X añadiendo nuevos biorreactores de 500L y 2,000L. Cytiva dijo que la plataforma más amplia ayuda a los científicos a escalar más suavemente de 50L a 2,000L con una mejor fiabilidad, flexibilidad y eficiencia, lo que apoya la consistencia del proceso para la biomanufactura regulada.
- En febrero de 2025, Thermo Fisher Scientific anunció un acuerdo definitivo para adquirir el negocio de Purificación y Filtración de Solventum por aproximadamente $4.1 mil millones en efectivo. La compañía dijo que la adquisición es altamente complementaria a su negocio de bioproducción y fortalecerá sus capacidades en los flujos de trabajo de biológicos upstream y downstream, que están estrechamente vinculados a las necesidades de validación de bioprocesos.
- En enero de 2025, Repligen lanzó el Sistema CTech SoloVPE PLUS, una nueva plataforma de medición de concentración UV-Vis en línea para aplicaciones de bioprocesamiento. Repligen declaró que el producto está diseñado para ofrecer mayor precisión, velocidad y facilidad de uso, ayudando a los clientes a tomar decisiones de proceso más rápidas y mejorar el control analítico durante la fabricación.
Alcance del Informe
| Atributo del Informe |
Detalles |
| Valor del tamaño del mercado en 2025 |
USD 426.54 millones |
| Pronóstico de ingresos en 2032 |
USD 1093.81 millones |
| Tasa de crecimiento (CAGR) |
14.4% (2025–2032) |
| Año base |
2025 |
| Período de pronóstico |
2026-2032 |
| Unidades cuantitativas |
USD millones |
| Segmentos cubiertos |
Por Tipo de Prueba; Por Componente del Proceso; Por Etapa del Bioproceso; Por Usuario Final |
| Alcance regional |
América del Norte, Europa, Asia Pacífico, América Latina, Medio Oriente y África |
| Empresas clave perfiladas |
Thermo Fisher Scientific Inc.; Merck KGaA; Sartorius AG; SGS SA; Eurofins Scientific; Pall Corporation; Charles River Laboratories; WuXi AppTec; Nelson Laboratories; TÜV SÜD |
| Número de páginas |
332 |
Segmentación
Por Tipo de Prueba
- Servicios de Pruebas de Extractables/Eluibles
- Servicios de Pruebas Microbiológicas
- Servicios de Pruebas Fisicoquímicas
- Servicios de Pruebas de Integridad
- Servicios de Pruebas de Compatibilidad
- Otros Tipos de Pruebas
Por Componente del Proceso
- Elementos de Filtro
- Contenedores de Medios y Bolsas
- Biorreactores
- Sistemas de Mezcla
- Bolsas para Procesos de Congelación y Descongelación
- Otros Componentes del Proceso
Por Etapa del Bioproceso
- Bioprocesamiento Upstream
- Bioprocesamiento Downstream
- Operaciones de Llenado y Acabado
Por Usuario Final
- Empresas Farmacéuticas
- Empresas de Biotecnología
- CDMOs
- Otros Usuarios Finales
Por Región
- Norteamérica
- Europa
- Alemania
- Francia
- Reino Unido
- Italia
- España
- Resto de Europa
- Asia Pacífico
- China
- Japón
- India
- Corea del Sur
- Sudeste Asiático
- Resto de Asia Pacífico
- América Latina
- Brasil
- Argentina
- Resto de América Latina
- Oriente Medio y África
- Países del CCG
- Sudáfrica
- Resto de Oriente Medio y África




