Aperçu du marché de la validation des bioprocédés :
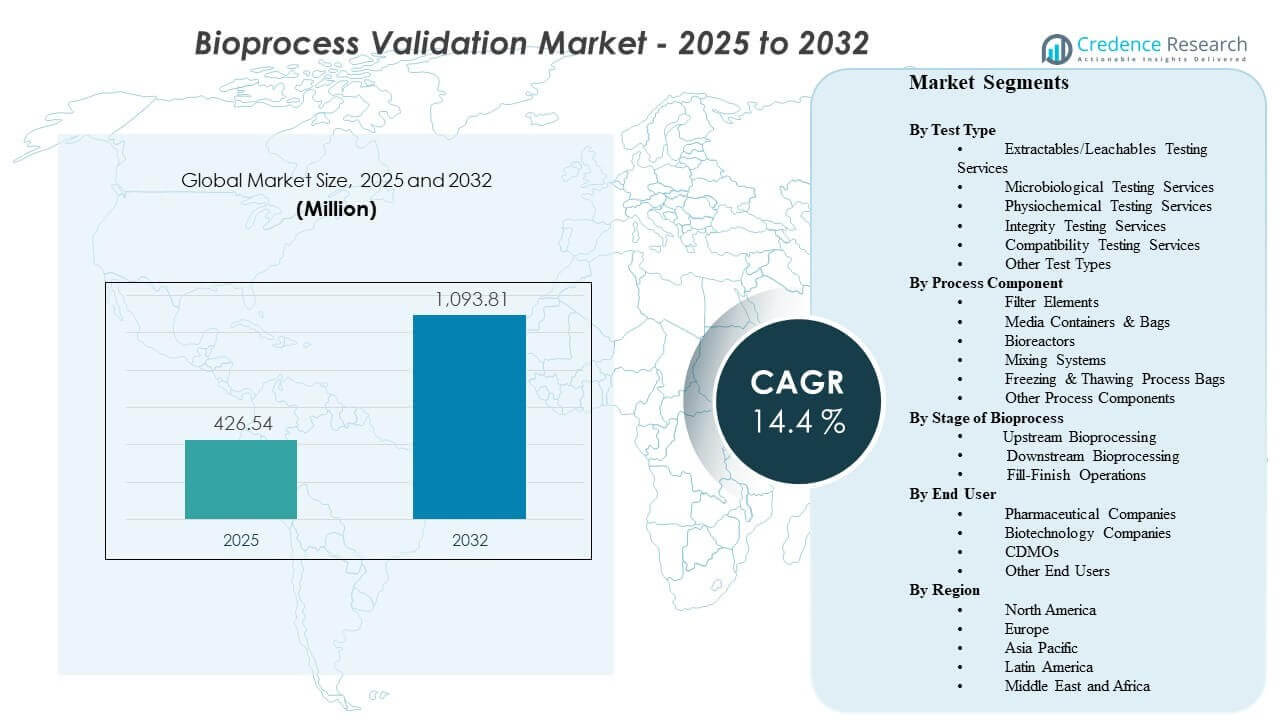
La taille du marché mondial de la validation des bioprocédés était estimée à 426,54 millions USD en 2025 et devrait atteindre 1093,81 millions USD d’ici 2032, avec un TCAC de 14,4 % de 2025 à 2032. La croissance est principalement motivée par des attentes plus strictes en matière de qualité et de contrôle de la contamination dans la fabrication de produits biologiques, ce qui élargit la portée et la fréquence de la validation à travers les étapes critiques du processus et les matériaux de contact. La demande est en outre soutenue par des ajouts de capacité et une croissance de l’externalisation qui augmentent le volume de qualification, de validation des méthodes et de cycles de documentation à travers les réseaux de fabrication mondiaux.
| ATTRIBUT DU RAPPORT |
DÉTAILS |
| Période Historique |
2020-2024 |
| Année de Base |
2025 |
| Période de Prévision |
2026-2032 |
| Taille du Marché de la Validation des Bioprocédés 2025 |
426,54 millions USD |
| Marché de la Validation des Bioprocédés, TCAC |
14,4% |
| Taille du Marché de la Validation des Bioprocédés 2032 |
1093,81 millions USD |
Tendances et Aperçus Clés du Marché
- Le marché devrait passer de 426,54 millions USD (2025) à 1093,81 millions USD (2032) avec un TCAC de 14,4 % (2025–2032).
- L’Amérique du Nord représentait 46,9 % en 2025, soutenue par une fabrication de produits biologiques mature et une intensité de conformité élevée.
- Les services de tests d’extractibles/lixiviables détenaient une part de 37,4 % en 2025, reflétant une adoption large des systèmes à usage unique et des attentes en matière de contrôle des risques d’impuretés.
- Les éléments filtrants représentaient 25,6 % de part en 2025, soulignant le rôle central de l’assurance stérile et de la vérification de l’intégrité dans la production validée.
- Les entreprises pharmaceutiques et biotechnologiques (combinées) ont capturé 57,3 % de part en 2025, les sponsors conservant une supervision directe des activités de validation critiques pour la qualité et la libération.
Analyse des Segments
La validation des bioprocédés est de plus en plus considérée comme un programme de bout en bout englobant la validation des méthodes, la stratégie de contrôle de la contamination et la documentation prête pour l’audit plutôt qu’un ensemble de tests isolés. À mesure que les pipelines se diversifient et que les changements de processus se produisent plus fréquemment à travers la montée en échelle et la gestion du cycle de vie, les packages de validation doivent être répétables, basés sur les risques et compatibles avec des délais de développement plus rapides. Cela déplace la demande vers des protocoles standardisés, des liens de contrôle des changements plus stricts et des systèmes de données qui soutiennent la traçabilité à travers les sites et les partenaires contractuels.
Les conceptions d’adoption à usage unique et de traitement intensifié augmentent l’importance de la compatibilité des matériaux, des profils d’extractibles/lixiviables et des tests d’intégrité à travers les composants en contact avec les fluides. En parallèle, les attentes en matière de fabrication stérile dans les opérations de fin de cycle augmentent la charge de validation concernant les transferts en amont et en aval et les environnements de remplissage-finition. L’externalisation continue de s’étendre pour des raisons de tests spécialisés et de capacité, mais les sponsors maintiennent généralement une gouvernance interne sur les critères d’acceptation, les écarts et la documentation à destination des régulateurs.
Access crucial information at unmatched prices!
Request your sample report today & start making informed decisions powered by Credence Research Inc.!
Download Sample
Par Aperçus du Type de Test
Les services de tests d’extractibles/lixiviables ont représenté la plus grande part de 37,4% en 2025. Leur leadership reflète le besoin de caractériser les impuretés potentielles provenant des matériaux de contact et d’assurer la compatibilité à travers les assemblages à usage unique et les voies de traitement. Les programmes de validation exigent de plus en plus des profils défendables qui peuvent être référencés lors des changements de processus, des mises à jour des fournisseurs et des transitions d’échelle. À mesure que les délais de développement se compressent, les acheteurs privilégient les fournisseurs capables de combiner une couverture analytique robuste avec des rapports clairs alignés sur les besoins de documentation de qualité.
Par Aperçus du Composant de Processus
Les éléments filtrants ont représenté la plus grande part de 25,6% en 2025. Les filtres sont centraux pour le contrôle de la contamination et l’assurance stérile, ce qui entraîne une qualification récurrente, des tests d’intégrité et une vérification lot par lot dans la fabrication validée. Le segment bénéficie de la haute fréquence d’utilisation des filtres à travers les opérations en amont et en aval et du besoin de valider la performance sous des plages de fonctionnement définies. Les acheteurs priorisent la cohérence, la traçabilité et les revendications de performance bien documentées qui soutiennent les audits et les examens de qualité internes.
Par Aperçus de l’Étape du Bioprocédé
Le biotraitement en amont a représenté la plus grande part de 51,6% en 2025. Les opérations en amont connaissent généralement le taux le plus élevé d’ajustement de processus et de changement d’échelle, ce qui élargit l’activité de validation pour les méthodes, les plans d’échantillonnage et les stratégies de contrôle. Les risques de variabilité dans les étapes précoces augmentent également la dépendance à la validation pour démontrer une performance cohérente à travers les séries et les sites. À mesure que les organisations adoptent des approches de traitement intensifiées et fermées, la validation en amont met de plus en plus l’accent sur une surveillance robuste, le contrôle de la contamination et des ensembles de documentation répétables.
Par Aperçus de l’Utilisateur Final
Les entreprises pharmaceutiques et les entreprises de biotechnologie (combinées) ont représenté la plus grande part de 57,3% en 2025. Les sponsors conservent souvent la gouvernance centrale de la validation pour maintenir un contrôle direct sur les critères d’acceptation, les écarts et les ensembles de preuves à destination des régulateurs. Les équipes internes gèrent également les décisions de transfert de méthode, les considérations de comparabilité et les mises à jour du cycle de vie qui déclenchent une re-validation. Même avec une externalisation plus large, les sponsors s’attendent généralement à ce que les partenaires externes fournissent des résultats standardisés qui s’intègrent harmonieusement dans les systèmes de qualité internes et les processus d’audit.
Moteurs du Marché de la Validation des Bioprocédés
Expansion de la Fabrication de Biologiques et Ajouts de Capacité
La croissance de la production de produits biologiques augmente le nombre d’installations, de lignes et de sites qui doivent répondre aux attentes d’un état validé. Chaque expansion introduit des cycles de qualification et de validation à travers les équipements, les utilités et les étapes critiques du processus. Les stratégies d’approvisionnement multi-sites augmentent encore la demande de packages de validation standardisés et de documentation cohérente. À mesure que les organisations se développent plus rapidement, elles s’appuient sur des cadres de validation répétables et basés sur les risques pour réduire les retards et éviter les perturbations de lots.
- Par exemple, Samsung Biologics a achevé la construction de l’usine 5 en avril 2025, ajoutant 180 000 litres de capacité de bioproduction et portant la capacité totale de production mondiale de l’entreprise à 845 000 litres sur son site de Songdo et l’installation nouvellement acquise de 60 000 litres à Rockville, Maryland — en faisant le plus grand CDMO au monde par capacité installée.
Augmentation des Attentes de Conformité pour le Contrôle de la Contamination et l’Assurance Stérile
Les exigences stériles et à faible charge biologique augmentent l’intensité de la validation à travers les contrôles de processus, la vérification de l’intégrité et les stratégies environnementales. Les équipes de qualité attendent de plus en plus des preuves que les risques de contamination sont contrôlés tout au long du chemin du processus, et pas seulement aux étapes finales. Cela élargit les besoins en tests à travers la microbiologie, les tests d’intégrité et les vérifications de compatibilité qui soutiennent les programmes de contrôle de la contamination. Une documentation solide et une traçabilité sont essentielles pour répondre aux attentes des audits.
L’Adoption de l’Usage Unique Stimule la Validation des Matériaux et de la Compatibilité
Le passage aux assemblages à usage unique augmente le besoin de valider les matériaux de contact, le risque de substances lixiviables et la compatibilité des processus dans des conditions de fonctionnement. La validation doit aborder la variation des fournisseurs, les changements de configuration des assemblages et les mises à jour du cycle de vie. Les acheteurs recherchent des méthodes de test et des rapports qui peuvent être réutilisés à travers les produits et les lignes lorsque cela est possible pour réduire les efforts répétés. Cette dynamique soutient une demande soutenue pour les services de tests d’extractibles/lixiviables et de compatibilité.
- Par exemple, FUJIFILM Diosynth Biotechnologies a réussi à répliquer sa plateforme de bioproduction à usage unique de Caroline du Nord, États-Unis, à son installation de Billingham, Royaume-Uni en seulement 14 mois, livrant la première installation de fabrication à usage unique cGMP du Royaume-Uni et commençant les opérations trois mois avant le calendrier initial du projet, grâce à des packages de qualification standardisés et au transfert de connaissances entre les sites.
Croissance de l’Externalisation et Besoin de Capacité de Validation Évolutive
Les commanditaires utilisent de plus en plus des partenaires externes pour gérer les contraintes de capacité, les méthodes spécialisées et les exigences de temps de rotation. L’externalisation peut réduire les goulots d’étranglement dans le développement et le soutien commercial, en particulier lors de la montée en échelle et des transitions de produits. Cependant, les organisations de qualité des commanditaires exigent toujours des livrables standardisés qui correspondent aux besoins de gouvernance interne et d’audit. Cela pousse les prestataires de services à se différencier par la maturité de la conformité, la qualité de la documentation et l’exécution cohérente.
Défis du marché de la validation des bioprocédés
Les programmes de validation peuvent devenir gourmands en ressources à mesure que les menus de tests s’élargissent et que les exigences de documentation augmentent sur les sites et chez les partenaires. Les organisations ont souvent du mal à aligner les critères d’acceptation, le contrôle des changements et les ensembles de preuves entre les équipes internes et les laboratoires externalisés, ce qui peut entraîner des reprises et des retards. Les transferts de méthode et les changements de fournisseurs introduisent des cycles supplémentaires de vérification difficiles à standardiser sur des empreintes de fabrication hétérogènes. Gérer les délais sans compromettre la qualité reste une tension opérationnelle persistante.
La complexité augmente également à mesure que les pipelines se diversifient et que les processus évoluent à travers les changements de cycle de vie, augmentant la fréquence des mises à jour pouvant déclencher une revalidation partielle. Les attentes en matière d’intégrité et de traçabilité des données nécessitent des systèmes plus robustes, des dossiers contrôlés et une préparation aux audits, ce qui augmente les frais généraux pour les sponsors et les prestataires de services. La variabilité des attentes réglementaires régionales et de l’accent mis sur les inspections peut compliquer davantage la standardisation mondiale. Ces pressions augmentent le besoin de gouvernance, de modèles et de manuels de validation reproductibles.
- Par exemple, Bristol Myers Squibb a fait face à la conséquence opérationnelle directe de la fragmentation des systèmes lorsqu’il a dû consolider un CTMS Celgene hérité et un CTMS BMS hérité, deux plateformes distinctes avec des architectures de documentation distinctes, en un système de gestion d’essais unifié à l’échelle mondiale ; la mise en œuvre complète à travers les opérations mondiales de l’entreprise a été achevée en moins de 20 mois.
Tendances et opportunités du marché de la validation des bioprocédés
Les organisations se dirigent vers des packages de validation intégrés qui lient les résultats des tests analytiques, microbiologiques et d’intégrité dans des structures de preuves prêtes pour l’audit. Cela favorise les prestataires ayant de larges capacités et de solides systèmes de qualité capables de fournir des rapports standardisés à travers les méthodes et les sites. Il y a également une demande croissante pour des délais d’exécution plus rapides et des structures de documentation plus claires qui soutiennent des cycles de révision plus rapides et des décisions de libération. La numérisation pour le suivi, la tendance et le contrôle de la documentation devient un différenciateur pratique dans la sélection des fournisseurs.
- Par exemple, Eurofins BioPharma Product Testing exploite un réseau de 46 laboratoires GMP harmonisés dans plus de 20 pays, tous régis par un seul manuel de politique de qualité mondiale et une plateforme eLIMS-BPT unifiée, des cahiers de laboratoire électroniques (ELN) et un portail client centralisé LabAccess℠ couvrant 28 sites dans le monde entier, une configuration qui permet une documentation inter-sites standardisée et des rapports prêts pour l’audit à grande échelle.
L’expansion des systèmes à usage unique et les conceptions de traitement intensifié créent des opportunités pour des cadres de qualification de matériaux reproductibles pouvant être exploités sur plusieurs produits et plateformes. À mesure que l’externalisation s’étend, les CDMO et les prestataires de tests spécialisés peuvent croître en offrant un support de validation de bout en bout qui réduit la charge de travail des sponsors et compresse les délais. La demande augmente également pour des approches de validation harmonisées qui facilitent les transferts multi-sites et les mises à jour du cycle de vie. Ces tendances soutiennent la croissance des entreprises capables de combiner capacité et exécution cohérente et conforme.
Aperçus régionaux
Amérique du Nord
L’Amérique du Nord représentait 46,9% des revenus en 2025, soutenue par une fabrication de produits biologiques bien établie, des écosystèmes CDMO denses et une intensité de conformité élevée. La demande régionale est stimulée par des activités fréquentes de montée en échelle et de gestion du cycle de vie qui déclenchent des re-validations et des mises à jour de méthodes. Les acheteurs ont tendance à privilégier la documentation prête pour l’audit, des délais prévisibles et une exécution cohérente sur plusieurs installations. La région soutient également une forte demande pour des tests d’intégrité et des flux de travail de validation alignés sur le contrôle de la contamination.
Europe
L’Europe représentait 22,4% des revenus en 2025, soutenue par une empreinte large de fabrication réglementée et des réseaux de production transfrontaliers. La demande de validation est renforcée par le besoin de packages de preuves standardisés pouvant être utilisés dans des chaînes d’approvisionnement multi-pays. Les acheteurs mettent souvent l’accent sur des procédures harmonisées, des systèmes de qualité solides et une documentation robuste de contrôle des changements. Les pôles de produits biologiques matures et les CDMO soutiennent une demande constante à travers les types de tests et les composants de processus.
Asie-Pacifique
L’Asie-Pacifique a contribué à 21,3% des revenus en 2025, reflétant une capacité en expansion et une participation croissante aux réseaux mondiaux d’externalisation et de fabrication. La croissance est soutenue par la construction de nouvelles installations, l’expansion des plateformes et l’adoption croissante de systèmes de qualité standardisés. Les sponsors et les CDMO de la région recherchent de plus en plus des capacités de validation évolutives avec des formats de documentation clairs alignés sur les audits mondiaux. La demande est particulièrement forte là où l’adoption de l’utilisation unique et la montée en échelle rapide augmentent les besoins en validation des matériaux et de l’intégrité.
Amérique latine
L’Amérique latine détenait 5,6% des revenus en 2025, avec une demande concentrée autour de la fabrication localisée, des activités de qualité liées à l’importation et des pôles de production régionaux. Les besoins en validation sont souvent façonnés par des ajouts de capacité basés sur des projets et la mise à niveau des systèmes de qualité. Les acheteurs se concentrent généralement sur l’assurance d’une documentation conforme et d’une exécution fiable sous des contraintes de ressources plus strictes. À mesure que les capacités s’étendent, la demande pour une validation externalisée et des packages de tests standardisés devrait se renforcer.
Moyen-Orient & Afrique
Le Moyen-Orient et l’Afrique représentaient 3,8% des revenus en 2025, reflétant une base installée plus petite mais un intérêt croissant pour la fabrication localisée et le développement de capacités stériles. La demande de validation est généralement liée à de nouveaux projets, des mises à niveau d’installations et des initiatives pour renforcer l’infrastructure de production réglementée. Les acheteurs priorisent les systèmes de qualité fondamentaux, les manuels de validation répétables et le soutien des partenaires pour la préparation de la documentation. La croissance devrait suivre le rythme des investissements dans la fabrication et le développement des capacités.
Paysage concurrentiel
La concurrence est façonnée par l’étendue des capacités, la maturité de la conformité, la performance de rotation et la capacité à fournir une documentation standardisée, prête pour l’audit, qui s’intègre dans les systèmes de qualité des sponsors. Les fournisseurs se différencient en offrant des flux de travail de validation groupés couvrant les tests analytiques, microbiologiques et d’intégrité, ainsi qu’un support de conseil pour le contrôle des changements et les mises à jour du cycle de vie. L’échelle, les réseaux de laboratoires géographiques et l’exécution cohérente sur les sites sont essentiels pour les grands programmes biopharmaceutiques et les stratégies de fabrication multi-sites. Les prestataires de services rivalisent également sur la spécialisation dans des domaines à haute surveillance tels que le contrôle de la contamination, la compatibilité des matériaux et les tests de support de libération.
Thermo Fisher Scientific Inc. est positionné sur les technologies et services permettant de soutenir le biotraitement validé, avec une force dans les flux de travail intégrés couvrant la bioproduction, l’analyse et le support qualité. L’approche de l’entreprise met généralement l’accent sur l’étendue du portefeuille et la capacité à soutenir des pratiques standardisées dans les environnements de développement et de fabrication. Cela s’aligne bien avec la demande des acheteurs pour des cadres de validation répétables pouvant être appliqués sur différents sites et produits. Les capacités d’échelle et d’intégration peuvent soutenir un déploiement plus rapide des solutions de validation et des structures de documentation cohérentes.
Le rapport de recherche et de croissance de l’industrie comprend des analyses détaillées du paysage concurrentiel du marché et des informations sur les principales entreprises, notamment :
Une analyse qualitative et quantitative des entreprises a été réalisée pour aider les clients à comprendre l’environnement commercial plus large ainsi que les forces et faiblesses des principaux acteurs de l’industrie. Les données sont analysées qualitativement pour catégoriser les entreprises comme pure player, axées sur une catégorie, axées sur l’industrie et diversifiées ; elles sont analysées quantitativement pour catégoriser les entreprises comme dominantes, leaders, fortes, provisoires et faibles.
Shape Your Report to Specific Countries or Regions & Enjoy 30% Off!
Développements Récents
- En avril 2025, Sartorius Stedim Biotech a conclu un partenariat stratégique avec Tulip Interfaces pour accélérer la transformation numérique dans la fabrication biopharmaceutique. Sartorius a déclaré que la collaboration vise à réduire les erreurs de processus manuels, améliorer la visibilité de la bioproduction de bout en bout et soutenir la conformité réglementaire dans les environnements de biotraitement à usage unique.
- En mars 2025, Cytiva a élargi son portefeuille Xcellerex X-platform en ajoutant de nouveaux bioréacteurs de 500L et 2 000L. Cytiva a déclaré que la plateforme élargie aide les scientifiques à passer plus facilement de 50L à 2 000L avec une fiabilité, une flexibilité et une efficacité améliorées, ce qui soutient la cohérence des processus pour la bioproduction réglementée.
- En février 2025, Thermo Fisher Scientific a annoncé un accord définitif pour acquérir l’activité de Purification & Filtration de Solventum pour environ 4,1 milliards de dollars en espèces. La société a déclaré que l’acquisition est hautement complémentaire à son activité de bioproduction et renforcera ses capacités à travers les flux de travail en amont et en aval des produits biologiques, qui sont étroitement liés aux besoins de validation des bioprocédés.
- En janvier 2025, Repligen a lancé le système CTech SoloVPE PLUS, une nouvelle plateforme de mesure de concentration UV-Vis en ligne pour les applications de biotraitement. Repligen a déclaré que le produit est conçu pour offrir une plus grande précision, rapidité et facilité d’utilisation, aidant les clients à prendre des décisions de processus plus rapides et à améliorer le contrôle analytique pendant la fabrication.
Portée du Rapport
| Attribut du Rapport |
Détails |
| Valeur de la taille du marché en 2025 |
USD 426,54 millions |
| Prévision des revenus en 2032 |
USD 1093,81 millions |
| Taux de croissance (CAGR) |
14,4% (2025–2032) |
| Année de base |
2025 |
| Période de prévision |
2026-2032 |
| Unités quantitatives |
USD million |
| Segments couverts |
Par Type de Test; Par Composant de Processus; Par Étape de Bioprocédé; Par Utilisateur Final |
| Portée régionale |
Amérique du Nord, Europe, Asie-Pacifique, Amérique Latine, Moyen-Orient & Afrique |
| Principales entreprises profilées |
Thermo Fisher Scientific Inc.; Merck KGaA; Sartorius AG; SGS SA; Eurofins Scientific; Pall Corporation; Charles River Laboratories; WuXi AppTec; Nelson Laboratories; TÜV SÜD |
| Nombre de Pages |
332 |
Segmentation
Par Type de Test
- Services de tests d’extractibles/lessivables
- Services de tests microbiologiques
- Services de tests physico-chimiques
- Services de tests d’intégrité
- Services de tests de compatibilité
- Autres types de tests
Par composant de processus
- Éléments filtrants
- Contenants et sacs pour médias
- Bioréacteurs
- Systèmes de mélange
- Sacs de processus de congélation et de décongélation
- Autres composants de processus
Par étape du bioprocédé
- Biotraitement en amont
- Biotraitement en aval
- Opérations de remplissage-finition
Par utilisateur final
- Entreprises pharmaceutiques
- Entreprises de biotechnologie
- CDMOs
- Autres utilisateurs finaux
Par région
- Amérique du Nord
- États-Unis
- Canada
- Mexique
- Europe
- Allemagne
- France
- Royaume-Uni
- Italie
- Espagne
- Reste de l’Europe
- Asie-Pacifique
- Chine
- Japon
- Inde
- Corée du Sud
- Asie du Sud-Est
- Reste de l’Asie-Pacifique
- Amérique latine
- Brésil
- Argentine
- Reste de l’Amérique latine
- Moyen-Orient & Afrique
- Pays du CCG
- Afrique du Sud
- Reste du Moyen-Orient et de l’Afrique




