Oversigt over Bioprocesvalideringsmarkedet:
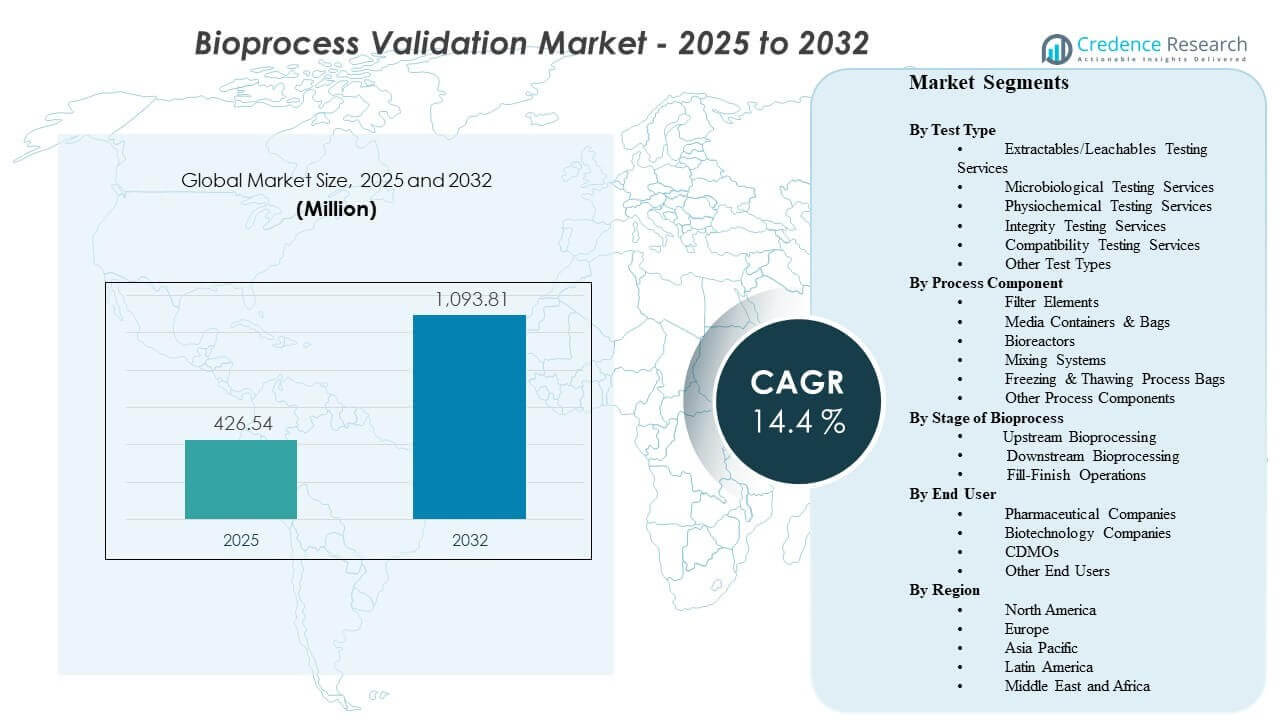
Den globale størrelse på bioprocesvalideringsmarkedet blev estimeret til USD 426,54 millioner i 2025 og forventes at nå USD 1093,81 millioner i 2032, med en vækst på en CAGR på 14,4% fra 2025 til 2032. Væksten drives primært af strammere kvalitets- og kontaminationskontrolforventninger på tværs af biologiske produktionsprocesser, hvilket udvider omfanget og frekvensen af validering på tværs af kritiske procestrin og kontaktmaterialer. Efterspørgslen understøttes yderligere af kapacitetsudvidelser og outsourcingvækst, der øger volumenet af kvalifikation, metodevalidering og dokumentationscyklusser på tværs af globale produktionsnetværk.
| RAPPORT ATTRIBUTE |
DETALJER |
| Historisk Periode |
2020-2024 |
| Basisår |
2025 |
| Prognoseperiode |
2026-2032 |
| Bioprocesvalideringsmarkedets Størrelse 2025 |
USD 426,54 millioner |
| Bioprocesvalideringsmarkedet, CAGR |
14,4% |
| Bioprocesvalideringsmarkedets Størrelse 2032 |
USD 1093,81 millioner |
Vigtige Markedstendenser & Indsigter
- Markedet forventes at ekspandere fra USD 426,54 millioner (2025) til USD 1093,81 millioner (2032) med en CAGR på 14,4% (2025–2032).
- Nordamerika tegnede sig for 46,9% i 2025, understøttet af moden biologisk produktion og høj overholdelsesintensitet.
- Extractables/Leachables Testtjenester havde en andel på 37,4% i 2025, hvilket afspejler bred adoption af engangssystemer og forventninger til kontrol af urenhedsrisici.
- Filterelementer repræsenterede en andel på 25,6% i 2025, hvilket understreger den centrale rolle af steril sikkerhed og integritetsverifikation i valideret produktion.
- Farmaceutiske & Bioteknologiske Virksomheder (kombineret) fangede en andel på 57,3% i 2025, da sponsorer bevarer direkte tilsyn med kritiske kvalitets- og frigivelsesmuliggørende valideringsaktiviteter.
Segmentanalyse
Bioprocesvalidering behandles i stigende grad som et end-to-end program, der spænder over metodevalidering, kontaminationskontrolstrategi og audit-klar dokumentation snarere end et sæt isolerede tests. Efterhånden som pipelines diversificeres og procesændringer forekommer hyppigere på tværs af opskalering og livscyklusstyring, skal valideringspakker være gentagelige, risikobaserede og kompatible med hurtigere udviklingstidslinjer. Dette flytter efterspørgslen mod standardiserede protokoller, strammere ændringskontrollink og datasystemer, der understøtter sporbarhed på tværs af steder og kontraktpartnere.
Engangsadoption og intensiverede forarbejdningsdesign øger vigtigheden af materialekompatibilitet, ekstraktables/lækbare profiler og integritetstest på tværs af komponenter, der er i kontakt med væsker. Parallelt med dette øger forventningerne til steril produktion i sene faser valideringsbyrden omkring overgange fra opstrøms til nedstrøms og fyld-finish miljøer. Outsourcing fortsætter med at udvide sig af specialiserede test- og kapacitetsårsager, men sponsorer opretholder typisk intern styring over acceptkriterier, afvigelser og dokumentation rettet mod regulering.
Access crucial information at unmatched prices!
Request your sample report today & start making informed decisions powered by Credence Research Inc.!
Download Sample
Indsigter efter Testtype
Ekstraktables/Lækbare Testtjenester tegnede sig for den største andel på 37,4% i 2025. Dens førerposition afspejler behovet for at karakterisere potentielle urenheder fra kontaktmaterialer og sikre kompatibilitet på tværs af engangsmonteringer og procesveje. Valideringsprogrammer kræver i stigende grad forsvarlige profiler, der kan refereres på tværs af procesændringer, leverandøropdateringer og skaleringsovergange. Efterhånden som udviklingstidslinjer komprimeres, foretrækker købere leverandører, der kan kombinere robust analytisk dækning med klar rapportering, der er tilpasset kvalitetsdokumentationsbehov.
Indsigter efter Proceskomponent
Filterelementer tegnede sig for den største andel på 25,6% i 2025. Filtre er centrale for kontaminationskontrol og steril sikkerhed, hvilket driver tilbagevendende kvalifikation, integritetstest og batch-til-batch verifikation i valideret produktion. Segmentet drager fordel af den høje frekvens af filterbrug på tværs af opstrøms og nedstrøms operationer og behovet for at validere ydeevne under definerede driftsområder. Købere prioriterer konsistens, sporbarhed og veldokumenterede ydeevnekrav, der understøtter revisioner og interne kvalitetsgennemgange.
Indsigter efter Bioprocesstadie
Opstrøms Bioprocessering tegnede sig for den største andel på 51,6% i 2025. Opstrøms operationer oplever typisk den højeste grad af procesjustering og opskalering, hvilket udvider valideringsaktiviteten for metoder, prøveudtagningsplaner og kontrolstrategier. Variabilitetsrisici i tidlige trin øger også afhængigheden af validering for at demonstrere ensartet ydeevne på tværs af kørsel og steder. Efterhånden som organisationer adopterer intensiverede og lukkede forarbejdningsmetoder, lægger opstrøms validering i stigende grad vægt på robust overvågning, kontaminationskontrol og gentagelige dokumentationspakker.
Indsigter efter Slutbruger
Farmaceutiske Selskaber og Bioteknologiske Selskaber (kombineret) tegnede sig for den største andel på 57,3% i 2025. Sponsorer bevarer ofte kernevalideringsstyring for at opretholde direkte kontrol over acceptkriterier, afvigelser og reguleringsrettede evidenspakker. Interne teams håndterer også beslutninger om metodeoverførsel, sammenlignelighedsovervejelser og livscyklusopdateringer, der udløser re-validering. Selv med bredere outsourcing forventer sponsorer typisk, at eksterne partnere leverer standardiserede output, der integreres problemfrit i interne kvalitetssystemer og revisionsprocesser.
Drivere for Bioprocesvalideringsmarkedet
Udvidelse af Biologisk Produktion og Kapacitetsforøgelser
Væksten i produktion af biologiske lægemidler øger antallet af faciliteter, produktionslinjer og steder, der skal opfylde forventningerne til valideret tilstand. Hver udvidelse introducerer kvalifikations- og valideringscyklusser på tværs af udstyr, forsyninger og kritiske procestrin. Multi-site forsyningsstrategier øger yderligere behovet for standardiserede valideringspakker og ensartet dokumentation. Efterhånden som organisationer skalerer hurtigere, stoler de på gentagelige, risikobaserede valideringsrammer for at reducere forsinkelser og undgå afbrydelser i batchproduktion.
- For eksempel afsluttede Samsung Biologics opførelsen af Plant 5 i april 2025, hvilket tilføjede 180.000 liter bioproduktionskapacitet og bragte virksomhedens samlede globale produktionskapacitet til 845.000 liter på tværs af sit Songdo-sted og den nyligt erhvervede 60.000-liters facilitet i Rockville, Maryland — hvilket gør det til verdens største CDMO målt på installeret kapacitet.
Stigende Overholdelsesforventninger for Kontaminationskontrol og Steril Sikring
Sterile og lav-biobyrde krav øger valideringsintensiteten på tværs af proceskontroller, integritetsverifikation og miljøstrategier. Kvalitetsteams forventer i stigende grad bevis for, at kontaminationsrisici er kontrolleret på tværs af hele procesvejen, ikke kun i de sidste trin. Dette udvider testbehovene inden for mikrobiologi, integritetstest og kompatibilitetskontroller, der understøtter kontaminationskontrolprogrammer. Stærk dokumentation og sporbarhed er centrale for at opfylde revisionsforventninger.
Enkeltbrugsadoption Driver Materiale- og Kompatibilitetsvalidering
Overgangen til enkeltbrugsanordninger øger behovet for at validere kontaktmaterialer, udvaskningsrisiko og proceskompatibilitet på tværs af driftsbetingelser. Validering skal adressere leverandørvariation, ændringer i samlingskonfiguration og livscyklusopdateringer. Købere søger testmetoder og rapportering, der kan genbruges på tværs af produkter og linjer, hvor det er muligt, for at reducere gentaget indsats. Denne dynamik understøtter en vedvarende efterspørgsel efter ekstraktions-/udvaskningstests og kompatibilitetstesttjenester.
- For eksempel replikerede FUJIFILM Diosynth Biotechnologies med succes sin enkeltbrugs bioproduktionsplatform fra North Carolina, USA, til sin facilitet i Billingham, UK på kun 14 måneder, hvilket leverede Storbritanniens første cGMP enkeltbrugsproduktionsfacilitet og påbegyndte driften tre måneder forud for den oprindelige projektplan, muliggjort af standardiserede kvalifikationspakker og vidensoverførsel på tværs af steder.
Outsourcing Vækst og Behovet for Skalerbar Valideringskapacitet
Sponsorer bruger i stigende grad eksterne partnere til at håndtere kapacitetsbegrænsninger, specialiserede metoder og krav til gennemløbstid. Outsourcing kan reducere flaskehalse i udvikling og kommerciel støtte, især under opskalering og produktovergange. Dog kræver sponsorernes kvalitetsorganisationer stadig standardiserede leverancer, der passer til intern styring og revisionsbehov. Dette presser serviceudbydere til at differentiere sig på overholdelsesmodenhed, dokumentationskvalitet og ensartet udførelse.
Udfordringer på markedet for bioprocesvalidering
Valideringsprogrammer kan blive ressourcekrævende, efterhånden som testmenuer udvides, og dokumentationskravene øges på tværs af steder og partnere. Organisationer kæmper ofte med at tilpasse acceptkriterier, ændringskontrol og dokumentationspakker på tværs af interne teams og eksterne laboratorier, hvilket kan skabe genarbejde og forsinkelser. Metodeoverførsler og leverandørskift introducerer yderligere verifikationscyklusser, der er svære at standardisere på tværs af heterogene produktionsenheder. At styre tidsplaner uden at gå på kompromis med kvaliteten forbliver en vedvarende operationel spænding.
Kompleksiteten stiger også, efterhånden som pipelines diversificeres, og processer udvikler sig gennem livscyklusændringer, hvilket øger hyppigheden af opdateringer, der kan udløse delvis re-validering. Forventninger til dataintegritet og sporbarhed kræver stærkere systemer, kontrollerede optegnelser og audit-parathed, hvilket øger omkostningerne for både sponsorer og tjenesteudbydere. Variabilitet i regionale regulatoriske forventninger og inspektionsfokus kan yderligere komplicere global standardisering. Disse pres øger behovet for styring, skabeloner og gentagelige valideringsmanualer.
- For eksempel stod Bristol Myers Squibb over for den direkte operationelle konsekvens af systemfragmentering, da det var nødvendigt at konsolidere en ældre Celgene CTMS og en ældre BMS CTMS, to separate platforme med forskellige dokumentationsarkitekturer, til et enkelt globalt forenet forsøgsstyringssystem; den fulde implementering på tværs af virksomhedens globale operationer blev gennemført på under 20 måneder.
Trends og muligheder på markedet for bioprocesvalidering
Organisationer bevæger sig mod integrerede valideringspakker, der forbinder analytiske, mikrobiologiske og integritetstestresultater i audit-klare dokumentationsstrukturer. Dette favoriserer udbydere med brede kapaciteter og stærke kvalitetssystemer, der kan levere standardiseret rapportering på tværs af metoder og steder. Der er også en stigende efterspørgsel efter hurtigere gennemløbstider og klarere dokumentationsstrukturer, der understøtter hurtigere gennemgangscyklusser og frigivelsesbeslutninger. Digital aktivering til sporing, trendanalyse og dokumentationskontrol bliver en praktisk differentieringsfaktor i leverandørvalg.
- For eksempel driver Eurofins BioPharma Product Testing et netværk af 46 harmoniserede GMP-laboratorier på tværs af mere end 20 lande, alle styret af en enkelt Global Quality Policy Manual og en samlet eLIMS-BPT platform, Elektroniske Laboratorie Notebooks (ELN), og en centraliseret LabAccess℠ klientportal, der spænder over 28 lokationer verden over – en konfiguration, der muliggør standardiseret dokumentation på tværs af steder og audit-klar rapportering i stor skala.
Udvidelse af engangsbrug og intensiverede procesdesign skaber muligheder for gentagelige materialekvalifikationsrammer, der kan udnyttes på tværs af flere produkter og platforme. Efterhånden som outsourcing udvides, kan CDMO’er og specialiserede testudbydere vokse ved at tilbyde end-to-end valideringsstøtte, der reducerer sponsorens arbejdsbyrde og komprimerer tidslinjer. Efterspørgslen stiger også efter harmoniserede valideringsmetoder, der letter overførsler mellem flere steder og livscyklusopdateringer. Disse trends understøtter vækst for virksomheder, der kan kombinere kapacitet med konsekvent, høj-overholdelsesudførelse.
Regionale indsigter
Nordamerika
Nordamerika repræsenterede 46,9% af indtægterne i 2025, understøttet af etableret biologisk produktion, tætte CDMO-økosystemer og høj overholdelsesintensitet. Regional efterspørgsel drives af hyppig opskalering og livscyklusstyringsaktiviteter, der udløser re-validering og metodeopdateringer. Købere har tendens til at prioritere revisionsklar dokumentation, forudsigelig gennemløbstid og konsekvent udførelse på tværs af flere faciliteter. Regionen understøtter også stærk efterspørgsel efter integritetstest og kontaminationskontrol-tilpassede valideringsarbejdsgange.
Europa
Europa tegnede sig for 22,4% af indtægterne i 2025, understøttet af en bred tilstedeværelse af reguleret produktion og grænseoverskridende produktionsnetværk. Valideringsefterspørgsel styrkes af behovet for standardiserede evidenspakker, der kan bruges på tværs af multinationale forsyningskæder. Købere lægger ofte vægt på harmoniserede procedurer, stærke kvalitetssystemer og robust ændringskontroldokumentation. Modne biologiske knudepunkter og CDMO’er understøtter stabil efterspørgsel på tværs af testtyper og proceskomponenter.
Asien og Stillehavsområdet
Asien og Stillehavsområdet bidrog med 21,3% af indtægterne i 2025, hvilket afspejler stigende kapacitet og øget deltagelse i globale outsourcing- og produktionsnetværk. Væksten understøttes af nye anlægsbyggerier, platformudvidelse og stigende adoption af standardiserede kvalitetssystemer. Sponsorer og CDMO’er i regionen søger i stigende grad skalerbare valideringsmuligheder med klare dokumentationsformater, der er tilpasset globale revisioner. Efterspørgslen er særlig stærk, hvor adoption af engangsbrug og hurtig opskalering øger behovet for materiale- og integritetsvalidering.
Latinamerika
Latinamerika stod for 5,6% af indtægterne i 2025, med efterspørgsel koncentreret omkring lokaliseret produktion, importrelaterede kvalitetsaktiviteter og regionale produktionsknudepunkter. Valideringsbehov formes ofte af projektbaserede kapacitetsforøgelser og opgradering af kvalitetssystemer. Købere fokuserer typisk på at sikre overensstemmende dokumentation og pålidelig udførelse under strammere ressourcebegrænsninger. Efterhånden som kapaciteterne udvides, forventes efterspørgslen efter outsourcet validering og standardiserede testpakker at styrkes.
Mellemøsten & Afrika
Mellemøsten & Afrika repræsenterede 3,8% af indtægterne i 2025, hvilket afspejler en mindre installeret base, men stigende interesse for lokaliseret produktion og opbygning af sterile kapaciteter. Valideringsefterspørgsel er typisk knyttet til nye projekter, anlægsopgraderinger og initiativer til at styrke reguleret produktionsinfrastruktur. Købere prioriterer grundlæggende kvalitetssystemer, gentagelige valideringsmanualer og partnerstøtte til dokumentationsberedskab. Væksten forventes at følge tempoet i produktionsinvesteringer og kapacitetsudvikling.
Konkurrencelandskab
Konkurrence formes af kapabilitetsbredde, compliance modenhed, turnaround ydeevne og evnen til at levere standardiseret, audit-klar dokumentation, der integreres i sponsorens kvalitetssystemer. Leverandører differentierer sig ved at tilbyde bundtede valideringsarbejdsgange på tværs af analytisk, mikrobiologisk og integritetstestning, sammen med konsulentstøtte til ændringskontrol og livscyklusopdateringer. Skala, geografiske laboratorienetværk og konsekvent udførelse på tværs af steder er nøglen for store biopharma-programmer og multi-site produktionsstrategier. Tjenesteudbydere konkurrerer også på specialisering i områder med høj kontrol, såsom kontaminationskontrol, materialekompatibilitet og frigivelsesstøttetestning.
Thermo Fisher Scientific Inc. er positioneret på tværs af muliggørende teknologier og tjenester, der understøtter valideret bioprocessering, med styrke i integrerede arbejdsgange, der spænder over bioproduktion, analyse og kvalitetsstøtte. Virksomhedens tilgang understreger typisk bredden af porteføljen og evnen til at understøtte standardiserede praksisser på tværs af udviklings- og produktionsmiljøer. Dette stemmer godt overens med købernes efterspørgsel efter gentagelige valideringsrammer, der kan anvendes på tværs af steder og produkter. Skala og integrationsmuligheder kan understøtte hurtigere implementering af valideringsløsninger og konsekvente dokumentationsstrukturer.
Industriens forsknings- og vækstrapport inkluderer detaljerede analyser af markedets konkurrenceprægede landskab og information om nøglevirksomheder, herunder:
Kvalitativ og kvantitativ analyse af virksomheder er blevet udført for at hjælpe kunder med at forstå det bredere forretningsmiljø samt styrker og svagheder hos nøgleaktører i branchen. Data analyseres kvalitativt for at kategorisere virksomheder som pure play, kategori-fokuseret, industri-fokuseret og diversificeret; det analyseres kvantitativt for at kategorisere virksomheder som dominerende, førende, stærk, foreløbig og svag.
Shape Your Report to Specific Countries or Regions & Enjoy 30% Off!
Seneste Udviklinger
- I april 2025 indgik Sartorius Stedim Biotech et strategisk partnerskab med Tulip Interfaces for at fremskynde digital transformation inden for biofarmaceutisk produktion. Sartorius sagde, at samarbejdet er beregnet til at reducere fejl i manuelle processer, forbedre end-to-end synlighed i bioproduktion og støtte overholdelse af regulativer i miljøer med engangsbioprocessering.
- I marts 2025 udvidede Cytiva sin Xcellerex X-platform portefølje ved at tilføje nye 500L og 2.000L bioreaktorer. Cytiva sagde, at den bredere platform hjælper forskere med at skalere mere jævnt fra 50L til 2.000L med forbedret pålidelighed, fleksibilitet og effektivitet, hvilket understøtter proceskonsistens for reguleret bioproduktion.
- I februar 2025 annoncerede Thermo Fisher Scientific en endelig aftale om at erhverve Solventums Purification & Filtration forretning for cirka 4,1 milliarder USD i kontanter. Virksomheden sagde, at opkøbet er meget komplementært til dens bioproduktionsforretning og vil styrke dens kapaciteter på tværs af upstream og downstream biologiske arbejdsgange, som er tæt forbundet med behov for bioprocesvalidering.
- I januar 2025 lancerede Repligen CTech SoloVPE PLUS System, en ny at-line UV-Vis koncentrationsmåleplatform til bioprocesseringsapplikationer. Repligen erklærede, at produktet er designet til at levere højere nøjagtighed, hastighed og brugervenlighed, hvilket hjælper kunder med at træffe hurtigere procesbeslutninger og forbedre analytisk kontrol under produktion.
Rapportens Omfang
| Rapportattribut |
Detaljer |
| Markedsstørrelse værdi i 2025 |
USD 426,54 millioner |
| Indtægtsprognose i 2032 |
USD 1093,81 millioner |
| Vækstrate (CAGR) |
14,4% (2025–2032) |
| Basisår |
2025 |
| Prognoseperiode |
2026-2032 |
| Kvantitative enheder |
USD millioner |
| Sektioner dækket |
Efter Testtype; Efter Proceskomponent; Efter Bioprocesstadie; Efter Slutbruger |
| Regionalt omfang |
Nordamerika, Europa, Asien og Stillehavsområdet, Latinamerika, Mellemøsten & Afrika |
| Nøglevirksomheder profileret |
Thermo Fisher Scientific Inc.; Merck KGaA; Sartorius AG; SGS SA; Eurofins Scientific; Pall Corporation; Charles River Laboratories; WuXi AppTec; Nelson Laboratories; TÜV SÜD |
| Antal sider |
332 |
Segmentering
Efter Testtype
- Testtjenester for ekstrakter/udvaskninger
- Mikrobiologiske testtjenester
- Fysikokemiske testtjenester
- Integritetstesttjenester
- Kompatibilitetstesttjenester
- Andre testtyper
Efter proceskomponent
- Filterelementer
- Mediebeholdere & poser
- Bioreaktorer
- Blandingssystemer
- Fryse- & optøningsposer
- Andre proceskomponenter
Efter bioprocesstadie
- Upstream bioprocessering
- Downstream bioprocessering
- Fyld-finish operationer
Efter slutbruger
- Farmaceutiske virksomheder
- Bioteknologiske virksomheder
- CDMO’er
- Andre slutbrugere
Efter region
- Nordamerika
- Europa
- Tyskland
- Frankrig
- U.K.
- Italien
- Spanien
- Resten af Europa
- Asien og Stillehavsområdet
- Kina
- Japan
- Indien
- Sydkorea
- Sydøstasien
- Resten af Asien og Stillehavsområdet
- Latinamerika
- Brasilien
- Argentina
- Resten af Latinamerika
- Mellemøsten & Afrika
- GCC-lande
- Sydafrika
- Resten af Mellemøsten og Afrika




