Panoramica del Mercato della Validazione dei Bioprocessi:
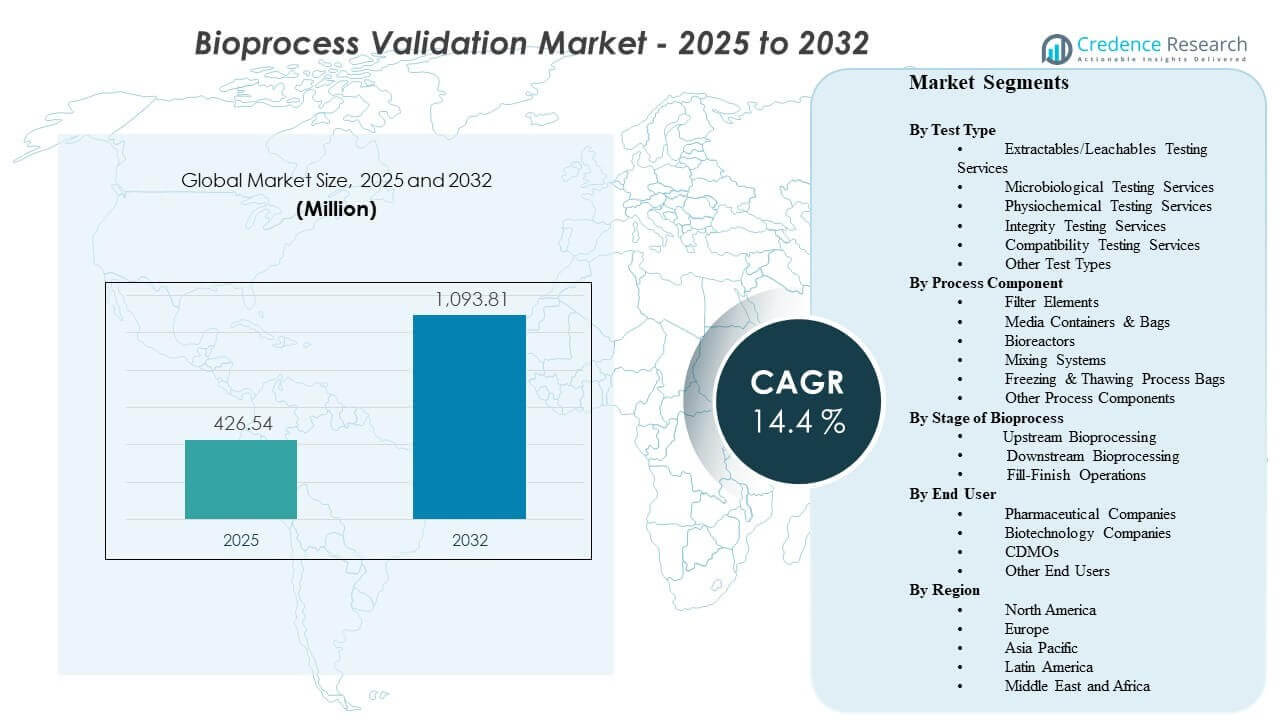
La dimensione del mercato globale della Validazione dei Bioprocessi è stata stimata a 426,54 milioni di USD nel 2025 e si prevede che raggiungerà 1093,81 milioni di USD entro il 2032, crescendo a un CAGR del 14,4% dal 2025 al 2032. La crescita è guidata principalmente da aspettative più rigorose in termini di qualità e controllo della contaminazione nella produzione di biologici, che ampliano la portata e la frequenza della validazione attraverso fasi critiche del processo e materiali di contatto. La domanda è ulteriormente supportata da aggiunte di capacità e crescita dell’outsourcing che aumentano il volume di qualificazione, validazione dei metodi e cicli di documentazione attraverso reti di produzione globali.
| ATTRIBUTO DEL RAPPORTO |
DETTAGLI |
| Periodo Storico |
2020-2024 |
| Anno Base |
2025 |
| Periodo di Previsione |
2026-2032 |
| Dimensione del Mercato della Validazione dei Bioprocessi 2025 |
426,54 milioni di USD |
| Mercato della Validazione dei Bioprocessi, CAGR |
14,4% |
| Dimensione del Mercato della Validazione dei Bioprocessi 2032 |
1093,81 milioni di USD |
Principali Tendenze e Approfondimenti del Mercato
- Il mercato è previsto espandersi da 426,54 milioni di USD (2025) a 1093,81 milioni di USD (2032) con un CAGR del 14,4% (2025–2032).
- Il Nord America ha rappresentato il 46,9% nel 2025, supportato da una produzione di biologici matura e un’elevata intensità di conformità.
- I Servizi di Test di Estraibili/Lisciviabili hanno detenuto una quota del 37,4% nel 2025, riflettendo un’ampia adozione di sistemi monouso e aspettative di controllo del rischio di impurità.
- Gli Elementi Filtranti hanno rappresentato una quota del 25,6% nel 2025, sottolineando il ruolo centrale dell’assicurazione sterile e della verifica dell’integrità nella produzione validata.
- Le Aziende Farmaceutiche e Biotecnologiche (combinato) hanno catturato una quota del 57,3% nel 2025, poiché gli sponsor mantengono una supervisione diretta delle attività di validazione critiche per la qualità e l’abilitazione al rilascio.
Analisi dei Segmenti
La validazione dei bioprocessi è sempre più trattata come un programma end-to-end che copre la validazione dei metodi, la strategia di controllo della contaminazione e la documentazione pronta per l’audit piuttosto che un insieme di test isolati. Man mano che le pipeline si diversificano e i cambiamenti di processo si verificano più frequentemente durante la scalabilità e la gestione del ciclo di vita, i pacchetti di validazione devono essere ripetibili, basati sul rischio e compatibili con tempi di sviluppo più rapidi. Questo sposta la domanda verso protocolli standardizzati, collegamenti di controllo delle modifiche più stretti e sistemi di dati che supportano la tracciabilità tra siti e partner contrattuali.
I design per l’adozione monouso e l’intensificazione dei processi stanno elevando l’importanza della compatibilità dei materiali, dei profili di estraibili/lisciviati e dei test di integrità tra i componenti a contatto con i fluidi. Parallelamente, le aspettative di produzione sterile nelle operazioni avanzate aumentano il carico di convalida nei passaggi da monte a valle e negli ambienti di riempimento e finitura. L’outsourcing continua a espandersi per motivi di test specializzati e capacità, ma gli sponsor tipicamente mantengono la governance interna sui criteri di accettazione, deviazioni e documentazione per le autorità regolatorie.
Access crucial information at unmatched prices!
Request your sample report today & start making informed decisions powered by Credence Research Inc.!
Download Sample
Per Approfondimenti sul Tipo di Test
I Servizi di Test per Esraibili/Lisciviati hanno rappresentato la quota maggiore del 37,4% nel 2025. La loro leadership riflette la necessità di caratterizzare le potenziali impurità dai materiali a contatto e garantire la compatibilità tra gli assemblaggi monouso e i percorsi di processo. I programmi di convalida richiedono sempre più profili difendibili che possano essere riferiti in caso di cambiamenti di processo, aggiornamenti dei fornitori e transizioni di scala. Con la compressione dei tempi di sviluppo, gli acquirenti preferiscono fornitori che possano combinare una copertura analitica robusta con report chiari allineati alle esigenze di documentazione di qualità.
Per Approfondimenti sui Componenti di Processo
Gli Elementi Filtranti hanno rappresentato la quota maggiore del 25,6% nel 2025. I filtri sono fondamentali per il controllo della contaminazione e l’assicurazione della sterilità, il che guida la qualificazione ricorrente, i test di integrità e la verifica batch-to-batch nella produzione convalidata. Il segmento beneficia dell’elevata frequenza d’uso dei filtri nelle operazioni a monte e a valle e della necessità di convalidare le prestazioni sotto intervalli operativi definiti. Gli acquirenti danno priorità alla coerenza, alla tracciabilità e alle affermazioni sulle prestazioni ben documentate che supportano audit e revisioni di qualità interne.
Per Approfondimenti sulla Fase del Bioprocesso
Il Bioprocesso a Monte ha rappresentato la quota maggiore del 51,6% nel 2025. Le operazioni a monte tipicamente sperimentano il più alto tasso di regolazione del processo e cambiamenti di scala, il che espande l’attività di convalida per metodi, piani di campionamento e strategie di controllo. I rischi di variabilità nelle fasi iniziali aumentano anche la dipendenza dalla convalida per dimostrare prestazioni costanti tra le esecuzioni e i siti. Man mano che le organizzazioni adottano approcci di processo intensificati e chiusi, la convalida a monte enfatizza sempre più il monitoraggio robusto, il controllo della contaminazione e pacchetti di documentazione ripetibili.
Per Approfondimenti sugli Utenti Finali
Le Aziende Farmaceutiche e le Aziende Biotecnologiche (combinati) hanno rappresentato la quota maggiore del 57,3% nel 2025. Gli sponsor spesso mantengono la governance centrale della convalida per mantenere il controllo diretto sui criteri di accettazione, le deviazioni e i pacchetti di prove per le autorità regolatorie. I team interni gestiscono anche le decisioni di trasferimento dei metodi, le considerazioni di comparabilità e gli aggiornamenti del ciclo di vita che innescano la riconvalida. Anche con un outsourcing più ampio, gli sponsor tipicamente si aspettano che i partner esterni forniscano risultati standardizzati che si integrino senza problemi nei sistemi di qualità interni e nei processi di audit.
Fattori Trainanti del Mercato della Convalida dei Bioprocessi
Espansione della Produzione di Biologici e Aggiunte di Capacità
La crescita della produzione di prodotti biologici aumenta il numero di strutture, linee e siti che devono soddisfare le aspettative di stato convalidato. Ogni espansione introduce cicli di qualificazione e convalida su attrezzature, utilities e fasi critiche del processo. Le strategie di fornitura multi-sito aumentano ulteriormente la domanda di pacchetti di convalida standardizzati e documentazione coerente. Man mano che le organizzazioni si espandono più rapidamente, si affidano a quadri di convalida ripetibili e basati sul rischio per ridurre i ritardi ed evitare interruzioni dei lotti.
- Ad esempio, Samsung Biologics ha completato la costruzione dell’Impianto 5 nell’aprile 2025, aggiungendo 180.000 litri di capacità di bioproduzione e portando la capacità produttiva globale totale dell’azienda a 845.000 litri nel sito di Songdo e nella nuova struttura acquisita da 60.000 litri a Rockville, Maryland — rendendola la più grande CDMO al mondo per capacità installata.
Aumento delle Aspettative di Conformità per il Controllo della Contaminazione e la Garanzia di Sterilità
I requisiti di sterilità e basso carico microbico aumentano l’intensità della convalida nei controlli di processo, nella verifica dell’integrità e nelle strategie ambientali. I team di qualità si aspettano sempre più prove che i rischi di contaminazione siano controllati lungo l’intero percorso del processo, non solo nelle fasi finali. Questo amplia le esigenze di test in microbiologia, test di integrità e controlli di compatibilità che supportano i programmi di controllo della contaminazione. Una forte documentazione e tracciabilità sono fondamentali per soddisfare le aspettative di audit.
Adozione di Sistemi Monouso che Guidano la Convalida di Materiali e Compatibilità
Il passaggio verso assemblaggi monouso aumenta la necessità di convalidare i materiali a contatto, il rischio di sostanze estraibili e la compatibilità del processo in condizioni operative. La convalida deve affrontare la variazione dei fornitori, i cambiamenti nella configurazione degli assemblaggi e gli aggiornamenti del ciclo di vita. Gli acquirenti cercano metodi di test e reportistica che possano essere riutilizzati tra prodotti e linee dove possibile per ridurre lo sforzo ripetuto. Questa dinamica supporta una domanda sostenuta per servizi di test di estraibili/lisciviabili e compatibilità.
- Ad esempio, FUJIFILM Diosynth Biotechnologies ha replicato con successo la sua piattaforma di bioproduzione monouso dalla Carolina del Nord, USA, alla sua struttura di Billingham, Regno Unito, in soli 14 mesi, consegnando la prima struttura di produzione monouso cGMP del Regno Unito e avviando le operazioni tre mesi prima del programma originale del progetto, grazie a pacchetti di qualificazione standardizzati e trasferimento di conoscenze tra i siti.
Crescita dell’Esternalizzazione e Necessità di Capacità di Convalida Scalabile
Gli sponsor utilizzano sempre più partner esterni per gestire i vincoli di capacità, i metodi specializzati e le esigenze di tempi di consegna. L’esternalizzazione può ridurre i colli di bottiglia nello sviluppo e nel supporto commerciale, specialmente durante l’espansione e le transizioni di prodotto. Tuttavia, le organizzazioni di qualità degli sponsor richiedono ancora deliverable standardizzati che si adattino alla governance interna e alle esigenze di audit. Questo spinge i fornitori di servizi a differenziarsi sulla maturità della conformità, la qualità della documentazione e l’esecuzione coerente.
Sfide del Mercato della Validazione dei Bioprocessi
I programmi di validazione possono diventare intensivi in termini di risorse man mano che i menu dei test si espandono e i requisiti di documentazione aumentano tra siti e partner. Le organizzazioni spesso faticano ad allineare i criteri di accettazione, il controllo delle modifiche e i pacchetti di evidenze tra team interni e laboratori esternalizzati, il che può creare rifacimenti e ritardi. I trasferimenti di metodi e i cambiamenti di fornitori introducono ulteriori cicli di verifica difficili da standardizzare su impronte manifatturiere eterogenee. Gestire le tempistiche senza compromettere la qualità rimane una tensione operativa persistente.
La complessità aumenta anche con la diversificazione delle pipeline e l’evoluzione dei processi attraverso cambiamenti nel ciclo di vita, aumentando la frequenza degli aggiornamenti che possono innescare una parziale ri-validazione. Le aspettative di integrità e tracciabilità dei dati richiedono sistemi più robusti, registri controllati e prontezza agli audit, il che aumenta i costi generali sia per gli sponsor che per i fornitori di servizi. La variabilità nelle aspettative normative regionali e l’attenzione alle ispezioni possono ulteriormente complicare la standardizzazione globale. Queste pressioni aumentano la necessità di governance, modelli e manuali di validazione ripetibili.
- Ad esempio, Bristol Myers Squibb ha affrontato la diretta conseguenza operativa della frammentazione del sistema quando ha dovuto consolidare un sistema di gestione delle sperimentazioni cliniche (CTMS) legacy di Celgene e un CTMS legacy di BMS, due piattaforme separate con architetture di documentazione distinte, in un unico sistema di gestione delle sperimentazioni cliniche unificato a livello globale; l’implementazione completa nelle operazioni globali dell’azienda è stata completata in meno di 20 mesi.
Tendenze e Opportunità del Mercato della Validazione dei Bioprocessi
Le organizzazioni si stanno muovendo verso pacchetti di validazione integrati che collegano i risultati dei test analitici, microbiologici e di integrità in strutture di evidenze pronte per l’audit. Questo favorisce i fornitori con ampie capacità e sistemi di qualità robusti che possono fornire report standardizzati attraverso metodi e siti. C’è anche una crescente domanda di tempi di risposta più rapidi e strutture di documentazione più chiare che supportano cicli di revisione più veloci e decisioni di rilascio. L’abilitazione digitale per il tracciamento, la tendenza e il controllo della documentazione sta diventando un differenziatore pratico nella selezione dei fornitori.
- Ad esempio, Eurofins BioPharma Product Testing gestisce una rete di 46 laboratori GMP armonizzati in più di 20 paesi, tutti governati da un unico Manuale di Politica della Qualità Globale e da una piattaforma unificata eLIMS-BPT, Quaderni di Laboratorio Elettronici (ELN) e un portale client centralizzato LabAccess℠ che copre 28 sedi in tutto il mondo, una configurazione che consente documentazione standardizzata tra i siti e report pronti per l’audit su larga scala.
L’espansione dell’uso singolo e i progetti di elaborazione intensificata stanno creando opportunità per quadri di qualificazione dei materiali ripetibili che possono essere sfruttati su più prodotti e piattaforme. Con l’espansione dell’outsourcing, i CDMO e i fornitori di test specializzati possono crescere offrendo supporto di validazione end-to-end che riduce il carico di lavoro degli sponsor e comprime le tempistiche. La domanda sta anche aumentando per approcci di validazione armonizzati che facilitano i trasferimenti multi-sito e gli aggiornamenti del ciclo di vita. Queste tendenze supportano la crescita per le aziende che possono combinare capacità con un’esecuzione coerente e ad alta conformità.
Approfondimenti Regionali
Nord America
Il Nord America ha rappresentato il 46,9% delle entrate nel 2025, supportato dalla produzione consolidata di biologici, ecosistemi CDMO densi e alta intensità di conformità. La domanda regionale è guidata da frequenti attività di scale-up e gestione del ciclo di vita che richiedono ri-validazione e aggiornamenti dei metodi. Gli acquirenti tendono a dare priorità a documentazione pronta per l’audit, tempi di consegna prevedibili ed esecuzione coerente in più strutture. La regione supporta anche una forte domanda di test di integrità e flussi di lavoro di validazione allineati al controllo della contaminazione.
Europa
L’Europa ha rappresentato il 22,4% delle entrate nel 2025, supportata da una vasta presenza di produzione regolamentata e reti di produzione transfrontaliere. La domanda di validazione è rafforzata dalla necessità di pacchetti di prove standardizzati che possano essere utilizzati in catene di fornitura multi-paese. Gli acquirenti spesso enfatizzano procedure armonizzate, sistemi di qualità forti e documentazione di controllo dei cambiamenti robusta. I centri di biologici maturi e i CDMO sostengono una domanda costante attraverso tipi di test e componenti di processo.
Asia Pacifico
L’Asia Pacifico ha contribuito al 21,3% delle entrate nel 2025, riflettendo una capacità in espansione e una crescente partecipazione alle reti globali di outsourcing e produzione. La crescita è supportata dalla costruzione di nuove strutture, espansione delle piattaforme e crescente adozione di sistemi di qualità standardizzati. Sponsor e CDMO nella regione cercano sempre più capacità di validazione scalabili con formati di documentazione chiari che si allineano agli audit globali. La domanda è particolarmente forte dove l’adozione monouso e il rapido scale-up aumentano le esigenze di validazione dei materiali e dell’integrità.
America Latina
L’America Latina ha detenuto il 5,6% delle entrate nel 2025, con domanda concentrata attorno alla produzione localizzata, attività di qualità legate all’importazione e hub di produzione regionali. Le esigenze di validazione sono spesso modellate da aggiunte di capacità basate su progetti e aggiornamento dei sistemi di qualità. Gli acquirenti si concentrano tipicamente sull’assicurare documentazione conforme ed esecuzione affidabile sotto vincoli di risorse più stretti. Con l’espansione delle capacità, si prevede che la domanda di validazione esternalizzata e pacchetti di test standardizzati si rafforzi.
Medio Oriente & Africa
Il Medio Oriente & Africa ha rappresentato il 3,8% delle entrate nel 2025, riflettendo una base installata più piccola ma un interesse crescente nella produzione localizzata e nello sviluppo di capacità sterili. La domanda di validazione è tipicamente legata a nuovi progetti, aggiornamenti delle strutture e iniziative per rafforzare l’infrastruttura di produzione regolamentata. Gli acquirenti danno priorità a sistemi di qualità fondamentali, manuali di validazione ripetibili e supporto dei partner per la prontezza della documentazione. Si prevede che la crescita segua il ritmo degli investimenti nella produzione e dello sviluppo delle capacità.
Panoramica Competitiva
La competizione è modellata dalla ampiezza delle capacità, dalla maturità della conformità, dalle prestazioni di turnaround e dalla capacità di fornire documentazione standardizzata, pronta per l’audit, che si integra nei sistemi di qualità del committente. I fornitori si differenziano offrendo flussi di lavoro di convalida integrati tra test analitici, microbiologici e di integrità, insieme al supporto di consulenza per il controllo delle modifiche e gli aggiornamenti del ciclo di vita. La scala, le reti di laboratori geografici e l’esecuzione coerente tra i siti sono fondamentali per i grandi programmi biofarmaceutici e le strategie di produzione multi-sito. I fornitori di servizi competono anche sulla specializzazione in aree ad alta sorveglianza come il controllo della contaminazione, la compatibilità dei materiali e i test di supporto al rilascio.
Thermo Fisher Scientific Inc. è posizionata su tecnologie e servizi abilitanti che supportano la bioprocessazione convalidata, con forza nei flussi di lavoro integrati che coprono la bioproduzione, l’analitica e il supporto alla qualità. L’approccio dell’azienda solitamente enfatizza l’ampiezza del portafoglio e la capacità di supportare pratiche standardizzate in ambienti di sviluppo e produzione. Questo si allinea bene con la domanda degli acquirenti per quadri di convalida ripetibili che possono essere applicati tra siti e prodotti. Le capacità di scala e integrazione possono supportare un dispiegamento più rapido delle soluzioni di convalida e strutture documentali coerenti.
Il rapporto di ricerca e crescita del settore include analisi dettagliate del panorama competitivo del mercato e informazioni sulle aziende chiave, tra cui:
È stata condotta un’analisi qualitativa e quantitativa delle aziende per aiutare i clienti a comprendere l’ambiente aziendale più ampio, nonché i punti di forza e di debolezza dei principali attori del settore. I dati sono analizzati qualitativamente per classificare le aziende come pure play, focalizzate su categorie, focalizzate sull’industria e diversificate; sono analizzati quantitativamente per classificare le aziende come dominanti, leader, forti, tentennanti e deboli.
Shape Your Report to Specific Countries or Regions & Enjoy 30% Off!
Sviluppi Recenti
- Ad aprile 2025, Sartorius Stedim Biotech ha avviato una partnership strategica con Tulip Interfaces per accelerare la trasformazione digitale nella produzione biofarmaceutica. Sartorius ha dichiarato che la collaborazione è destinata a ridurre gli errori nei processi manuali, migliorare la visibilità end-to-end nella bioproduzione e supportare la conformità normativa negli ambienti di bioprocessing monouso.
- A marzo 2025, Cytiva ha ampliato il suo portafoglio Xcellerex X-platform aggiungendo nuovi bioreattori da 500L e 2.000L. Cytiva ha affermato che la piattaforma più ampia aiuta gli scienziati a scalare più agevolmente da 50L a 2.000L con maggiore affidabilità, flessibilità ed efficienza, supportando la coerenza dei processi per la bioproduzione regolamentata.
- A febbraio 2025, Thermo Fisher Scientific ha annunciato un accordo definitivo per acquisire il business di Purificazione & Filtrazione di Solventum per circa 4,1 miliardi di dollari in contanti. L’azienda ha dichiarato che l’acquisizione è altamente complementare al suo business di bioproduzione e rafforzerà le sue capacità nei flussi di lavoro biologici a monte e a valle, strettamente legati alle esigenze di validazione dei bioprocessi.
- A gennaio 2025, Repligen ha lanciato il sistema CTech SoloVPE PLUS, una nuova piattaforma di misurazione della concentrazione UV-Vis in linea per applicazioni di bioprocessing. Repligen ha affermato che il prodotto è progettato per offrire maggiore precisione, velocità e facilità d’uso, aiutando i clienti a prendere decisioni di processo più rapide e migliorare il controllo analitico durante la produzione.
Ambito del Rapporto
| Attributo del Rapporto |
Dettagli |
| Valore della dimensione del mercato nel 2025 |
USD 426,54 milioni |
| Previsione dei ricavi nel 2032 |
USD 1093,81 milioni |
| Tasso di crescita (CAGR) |
14,4% (2025–2032) |
| Anno base |
2025 |
| Periodo di previsione |
2026-2032 |
| Unità quantitative |
Milioni di USD |
| Segmenti coperti |
Per Tipo di Test; Per Componente di Processo; Per Fase del Bioprocesso; Per Utente Finale |
| Ambito regionale |
Nord America, Europa, Asia Pacifico, America Latina, Medio Oriente & Africa |
| Aziende chiave profilate |
Thermo Fisher Scientific Inc.; Merck KGaA; Sartorius AG; SGS SA; Eurofins Scientific; Pall Corporation; Charles River Laboratories; WuXi AppTec; Nelson Laboratories; TÜV SÜD |
| Numero di pagine |
332 |
Segmentazione
Per Tipo di Test
- Servizi di Test per Estraibili/Percolabili
- Servizi di Test Microbiologici
- Servizi di Test Fisico-chimici
- Servizi di Test di Integrità
- Servizi di Test di Compatibilità
- Altri Tipi di Test
Per Componente di Processo
- Elementi Filtranti
- Contenitori & Sacche per Media
- Bioreattori
- Sistemi di Miscelazione
- Sacche per Processi di Congelamento & Scongelamento
- Altri Componenti di Processo
Per Fase del Bioprocesso
- Bioprocessing Upstream
- Bioprocessing Downstream
- Operazioni di Riempimento-Finitura
Per Utente Finale
- Aziende Farmaceutiche
- Aziende Biotecnologiche
- CDMO
- Altri Utenti Finali
Per Regione
- Nord America
- Europa
- Germania
- Francia
- Regno Unito
- Italia
- Spagna
- Resto d’Europa
- Asia Pacifico
- Cina
- Giappone
- India
- Corea del Sud
- Sud-est Asiatico
- Resto dell’Asia Pacifico
- America Latina
- Brasile
- Argentina
- Resto dell’America Latina
- Medio Oriente & Africa
- Paesi del GCC
- Sud Africa
- Resto del Medio Oriente e Africa




