Visão Geral do Mercado de Validação de Bioprocessos:
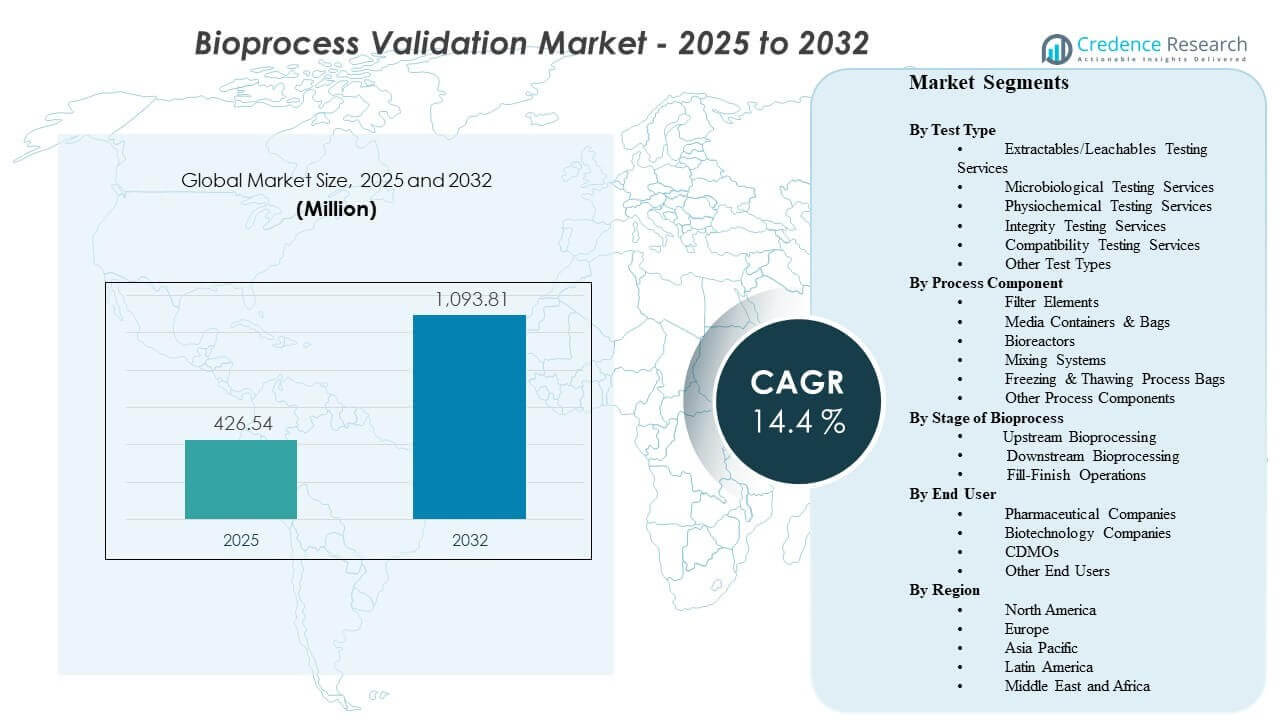
O tamanho do mercado global de Validação de Bioprocessos foi estimado em USD 426,54 milhões em 2025 e espera-se que alcance USD 1093,81 milhões até 2032, crescendo a uma CAGR de 14,4% de 2025 a 2032. O crescimento é impulsionado principalmente por expectativas mais rigorosas de qualidade e controle de contaminação na fabricação de biológicos, que ampliam o escopo e a frequência da validação em etapas críticas do processo e materiais de contato. A demanda é ainda apoiada por adições de capacidade e crescimento de terceirização que aumentam o volume de qualificação, validação de métodos e ciclos de documentação em redes de fabricação globais.
| ATRIBUTO DO RELATÓRIO |
DETALHES |
| Período Histórico |
2020-2024 |
| Ano Base |
2025 |
| Período de Previsão |
2026-2032 |
| Tamanho do Mercado de Validação de Bioprocessos 2025 |
USD 426,54 milhões |
| Mercado de Validação de Bioprocessos, CAGR |
14,4% |
| Tamanho do Mercado de Validação de Bioprocessos 2032 |
USD 1093,81 milhões |
Tendências e Insights Principais do Mercado
- O mercado está projetado para expandir de USD 426,54 milhões (2025) para USD 1093,81 milhões (2032) a uma CAGR de 14,4% (2025–2032).
- A América do Norte representou 46,9% em 2025, apoiada por uma fabricação de biológicos madura e alta intensidade de conformidade.
- Os Serviços de Teste de Extraíveis/Lixiviáveis detiveram 37,4% de participação em 2025, refletindo a ampla adoção de sistemas descartáveis e expectativas de controle de risco de impurezas.
- Elementos de Filtro representaram 25,6% de participação em 2025, sublinhando o papel central da garantia estéril e verificação de integridade na produção validada.
- Empresas Farmacêuticas & de Biotecnologia (combinadas) capturaram 57,3% de participação em 2025, à medida que os patrocinadores mantêm supervisão direta das atividades críticas de qualidade e validação que permitem a liberação.
Análise de Segmento
A validação de bioprocessos é cada vez mais tratada como um programa de ponta a ponta abrangendo validação de métodos, estratégia de controle de contaminação e documentação pronta para auditoria, em vez de um conjunto de testes isolados. À medida que os pipelines se diversificam e as mudanças de processo ocorrem com mais frequência ao longo da ampliação e gestão do ciclo de vida, os pacotes de validação devem ser repetíveis, baseados em risco e compatíveis com cronogramas de desenvolvimento mais rápidos. Isso desloca a demanda para protocolos padronizados, ligações mais rigorosas de controle de mudanças e sistemas de dados que apoiam a rastreabilidade em sites e parceiros contratuais.
Os designs de adoção de uso único e processamento intensificado estão elevando a importância da compatibilidade de materiais, perfis de extraíveis/lixiviáveis e testes de integridade em componentes de contato com fluidos. Paralelamente, as expectativas de fabricação estéril em operações de estágio avançado aumentam o ônus de validação em transferências de upstream para downstream e ambientes de preenchimento e acabamento. A terceirização continua a se expandir por razões de testes especializados e capacidade, mas os patrocinadores geralmente mantêm a governança interna sobre critérios de aceitação, desvios e documentação voltada para regulamentação.
Access crucial information at unmatched prices!
Request your sample report today & start making informed decisions powered by Credence Research Inc.!
Download Sample
Por Tipo de Teste
Os Serviços de Teste de Extraíveis/Lixiviáveis representaram a maior participação de 37,4% em 2025. Sua liderança reflete a necessidade de caracterizar potenciais impurezas de materiais de contato e garantir compatibilidade em montagens de uso único e caminhos de processo. Os programas de validação exigem cada vez mais perfis defensáveis que possam ser referenciados em mudanças de processo, atualizações de fornecedores e transições de escala. À medida que os cronogramas de desenvolvimento se comprimem, os compradores preferem fornecedores que possam combinar uma cobertura analítica robusta com relatórios claros alinhados às necessidades de documentação de qualidade.
Por Componente de Processo
Os Elementos de Filtro representaram a maior participação de 25,6% em 2025. Os filtros são centrais para o controle de contaminação e garantia estéril, o que impulsiona a qualificação recorrente, testes de integridade e verificação de lote a lote em fabricação validada. O segmento se beneficia da alta frequência de uso de filtros em operações upstream e downstream e da necessidade de validar o desempenho sob faixas operacionais definidas. Os compradores priorizam consistência, rastreabilidade e reivindicações de desempenho bem documentadas que suportam auditorias e revisões internas de qualidade.
Por Estágio do Processo Biológico
O Processamento Biológico Upstream representou a maior participação de 51,6% em 2025. As operações upstream geralmente experimentam a maior taxa de ajuste de processo e mudança de escala, o que expande a atividade de validação para métodos, planos de amostragem e estratégias de controle. Os riscos de variabilidade nas etapas iniciais também aumentam a dependência da validação para demonstrar desempenho consistente entre execuções e locais. À medida que as organizações adotam abordagens de processamento intensificado e fechado, a validação upstream enfatiza cada vez mais o monitoramento robusto, controle de contaminação e pacotes de documentação repetíveis.
Por Usuário Final
As Empresas Farmacêuticas e Empresas de Biotecnologia (combinadas) representaram a maior participação de 57,3% em 2025. Os patrocinadores frequentemente mantêm a governança central de validação para manter controle direto sobre critérios de aceitação, desvios e pacotes de evidências voltados para regulamentação. As equipes internas também gerenciam decisões de transferência de métodos, considerações de comparabilidade e atualizações de ciclo de vida que desencadeiam revalidação. Mesmo com uma terceirização mais ampla, os patrocinadores geralmente esperam que parceiros externos entreguem resultados padronizados que se integrem suavemente aos sistemas de qualidade internos e processos de auditoria.
Fatores de Impulso do Mercado de Validação de Processos Biológicos
Expansão da Fabricação de Biológicos e Adições de Capacidade
O crescimento da produção de biológicos aumenta o número de instalações, linhas e locais que devem atender às expectativas de estado validado. Cada expansão introduz ciclos de qualificação e validação em equipamentos, utilidades e etapas críticas do processo. Estratégias de fornecimento em múltiplos locais aumentam ainda mais a demanda por pacotes de validação padronizados e documentação consistente. À medida que as organizações escalam mais rapidamente, elas dependem de estruturas de validação repetíveis e baseadas em risco para reduzir atrasos e evitar interrupções de lotes.
- Por exemplo, a Samsung Biologics concluiu a construção da Planta 5 em abril de 2025, adicionando 180.000 litros de capacidade de bioprodução e elevando a capacidade total de produção global da empresa para 845.000 litros em seu local em Songdo e na recém-adquirida instalação de 60.000 litros em Rockville, Maryland — tornando-se a maior CDMO do mundo por capacidade instalada.
Aumento das Expectativas de Conformidade para Controle de Contaminação e Garantia de Esterilidade
Requisitos de esterilidade e baixa carga biológica aumentam a intensidade da validação em controles de processo, verificação de integridade e estratégias ambientais. As equipes de qualidade esperam cada vez mais evidências de que os riscos de contaminação são controlados em todo o caminho do processo, não apenas nas etapas finais. Isso amplia as necessidades de testes em microbiologia, testes de integridade e verificações de compatibilidade que apoiam programas de controle de contaminação. Documentação forte e rastreabilidade são centrais para atender às expectativas de auditoria.
Adoção de Uso Único Impulsionando a Validação de Materiais e Compatibilidade
A mudança para montagens de uso único aumenta a necessidade de validar materiais de contato, risco de lixiviáveis e compatibilidade do processo em condições operacionais. A validação deve abordar variações de fornecedores, mudanças na configuração da montagem e atualizações de ciclo de vida. Os compradores buscam métodos de teste e relatórios que possam ser reutilizados em produtos e linhas, quando viável, para reduzir o esforço repetido. Essa dinâmica apoia a demanda sustentada por serviços de teste de extratáveis/lixiviáveis e compatibilidade.
- Por exemplo, a FUJIFILM Diosynth Biotechnologies replicou com sucesso sua plataforma de bioprodução de uso único da Carolina do Norte, EUA, para sua instalação em Billingham, Reino Unido, em apenas 14 meses, entregando a primeira instalação de fabricação de uso único cGMP do Reino Unido e iniciando operações três meses antes do cronograma original do projeto, possibilitado por pacotes de qualificação padronizados e transferência de conhecimento entre locais.
Crescimento da Terceirização e a Necessidade de Capacidade de Validação Escalável
Os patrocinadores utilizam cada vez mais parceiros externos para gerenciar restrições de capacidade, métodos especializados e demandas de tempo de resposta. A terceirização pode reduzir gargalos no desenvolvimento e suporte comercial, especialmente durante a ampliação e transições de produtos. No entanto, as organizações de qualidade dos patrocinadores ainda exigem entregáveis padronizados que se ajustem às necessidades internas de governança e auditoria. Isso leva os provedores de serviços a se diferenciarem na maturidade da conformidade, qualidade da documentação e execução consistente.
Desafios do Mercado de Validação de Bioprocessos
Os programas de validação podem se tornar intensivos em recursos à medida que os menus de teste se expandem e os requisitos de documentação aumentam em locais e parceiros. As organizações muitas vezes enfrentam dificuldades para alinhar critérios de aceitação, controle de mudanças e pacotes de evidências entre equipes internas e laboratórios terceirizados, o que pode gerar retrabalho e atrasos. Transferências de métodos e mudanças de fornecedores introduzem ciclos adicionais de verificação que são difíceis de padronizar em plantas de fabricação heterogêneas. Gerenciar cronogramas sem comprometer a qualidade continua sendo uma tensão operacional persistente.
A complexidade também aumenta à medida que os pipelines se diversificam e os processos evoluem através de mudanças no ciclo de vida, aumentando a frequência de atualizações que podem desencadear revalidações parciais. As expectativas de integridade e rastreabilidade de dados exigem sistemas mais robustos, registros controlados e prontidão para auditorias, o que aumenta os custos gerais tanto para patrocinadores quanto para prestadores de serviços. A variabilidade nas expectativas regulatórias regionais e no foco das inspeções pode complicar ainda mais a padronização global. Essas pressões aumentam a necessidade de governança, modelos e manuais de validação repetíveis.
- Por exemplo, a Bristol Myers Squibb enfrentou a consequência operacional direta da fragmentação do sistema quando precisou consolidar um CTMS legado da Celgene e um CTMS legado da BMS – duas plataformas separadas com arquiteturas de documentação distintas – em um único sistema de gerenciamento de ensaios globalmente unificado; a implementação completa nas operações globais da empresa foi concluída em menos de 20 meses.
Tendências e Oportunidades do Mercado de Validação de Bioprocessos
As organizações estão se movendo em direção a pacotes de validação integrados que vinculam saídas de testes analíticos, microbiológicos e de integridade em estruturas de evidências prontas para auditoria. Isso favorece fornecedores com amplas capacidades e sistemas de qualidade robustos que podem fornecer relatórios padronizados entre métodos e locais. Há também uma demanda crescente por tempos de resposta mais rápidos e estruturas de documentação mais claras que apoiem ciclos de revisão mais rápidos e decisões de liberação. A habilitação digital para rastreamento, tendências e controle de documentação está se tornando um diferencial prático na seleção de fornecedores.
- Por exemplo, a Eurofins BioPharma Product Testing opera uma rede de 46 laboratórios GMP harmonizados em mais de 20 países, todos regidos por um único Manual de Política de Qualidade Global e uma plataforma unificada eLIMS-BPT, Cadernos de Laboratório Eletrônicos (ELN) e um portal centralizado LabAccess℠ para clientes abrangendo 28 locais em todo o mundo – uma configuração que permite documentação padronizada entre locais e relatórios prontos para auditoria em escala.
A expansão de uso único e os designs de processamento intensificado estão criando oportunidades para estruturas de qualificação de materiais repetíveis que podem ser aproveitadas em vários produtos e plataformas. À medida que a terceirização se expande, CDMOs e fornecedores de testes especializados podem crescer oferecendo suporte de validação de ponta a ponta que reduz a carga de trabalho dos patrocinadores e comprime cronogramas. A demanda também está aumentando por abordagens de validação harmonizadas que facilitem transferências entre vários locais e atualizações de ciclo de vida. Essas tendências apoiam o crescimento de empresas que podem combinar capacidade com execução consistente e de alta conformidade.
Insights Regionais
América do Norte
A América do Norte representou 46,9% da receita em 2025, apoiada pela fabricação de biológicos estabelecida, ecossistemas densos de CDMO e alta intensidade de conformidade. A demanda regional é impulsionada por frequentes atividades de aumento de escala e gestão do ciclo de vida que desencadeiam revalidação e atualizações de métodos. Os compradores tendem a priorizar documentação pronta para auditoria, prazos de entrega previsíveis e execução consistente em várias instalações. A região também apoia uma forte demanda por testes de integridade e fluxos de trabalho de validação alinhados ao controle de contaminação.
Europa
A Europa representou 22,4% da receita em 2025, apoiada por uma ampla presença de fabricação regulamentada e redes de produção transfronteiriças. A demanda por validação é fortalecida pela necessidade de pacotes de evidências padronizados que podem ser usados em cadeias de suprimento de vários países. Os compradores frequentemente enfatizam procedimentos harmonizados, sistemas de qualidade fortes e documentação robusta de controle de mudanças. Centros maduros de biológicos e CDMOs sustentam uma demanda constante por tipos de testes e componentes de processo.
Ásia-Pacífico
A Ásia-Pacífico contribuiu com 21,3% da receita em 2025, refletindo a expansão da capacidade e o aumento da participação em redes globais de terceirização e fabricação. O crescimento é apoiado por novas construções de instalações, expansão de plataformas e crescente adoção de sistemas de qualidade padronizados. Patrocinadores e CDMOs na região buscam cada vez mais capacidades de validação escaláveis com formatos de documentação claros que se alinhem às auditorias globais. A demanda é particularmente forte onde a adoção de uso único e o rápido aumento de escala aumentam as necessidades de validação de materiais e integridade.
América Latina
A América Latina deteve 5,6% da receita em 2025, com a demanda concentrada em torno da fabricação local, atividades de qualidade vinculadas à importação e centros de produção regionais. As necessidades de validação são frequentemente moldadas por adições de capacidade baseadas em projetos e atualização de sistemas de qualidade. Os compradores normalmente se concentram em garantir documentação em conformidade e execução confiável sob restrições de recursos mais apertadas. À medida que as capacidades se expandem, espera-se que a demanda por validação terceirizada e pacotes de teste padronizados se fortaleça.
Médio Oriente e África
O Médio Oriente e África representaram 3,8% da receita em 2025, refletindo uma base instalada menor, mas um interesse crescente em fabricação local e desenvolvimento de capacidade estéril. A demanda por validação está tipicamente ligada a novos projetos, atualizações de instalações e iniciativas para fortalecer a infraestrutura de produção regulamentada. Os compradores priorizam sistemas de qualidade fundamentais, manuais de validação repetíveis e suporte de parceiros para prontidão de documentação. Espera-se que o crescimento acompanhe o ritmo do investimento em fabricação e desenvolvimento de capacidades.
Paisagem Competitiva
A competição é moldada pela amplitude de capacidade, maturidade de conformidade, desempenho de retorno e a capacidade de entregar documentação padronizada, pronta para auditoria, que se integra aos sistemas de qualidade do patrocinador. Os fornecedores se diferenciam ao oferecer fluxos de trabalho de validação agrupados em testes analíticos, microbiológicos e de integridade, juntamente com suporte de consultoria para controle de mudanças e atualizações de ciclo de vida. Escala, redes de laboratórios geográficos e execução consistente em vários locais são fundamentais para grandes programas biofarmacêuticos e estratégias de fabricação em vários locais. Os prestadores de serviços também competem em especialização em áreas de alta escrutínio, como controle de contaminação, compatibilidade de materiais e testes de suporte à liberação.
Thermo Fisher Scientific Inc. está posicionada em tecnologias e serviços que apoiam o bioprocessamento validado, com força em fluxos de trabalho integrados que abrangem bioprodução, análises e suporte de qualidade. A abordagem da empresa geralmente enfatiza a amplitude do portfólio e a capacidade de apoiar práticas padronizadas em ambientes de desenvolvimento e fabricação. Isso se alinha bem com a demanda dos compradores por estruturas de validação repetíveis que podem ser aplicadas em vários locais e produtos. Capacidades de escala e integração podem apoiar uma implantação mais rápida de soluções de validação e estruturas de documentação consistentes.
O relatório de pesquisa e crescimento da indústria inclui análises detalhadas do cenário competitivo do mercado e informações sobre empresas-chave, incluindo:
Análises qualitativas e quantitativas das empresas foram conduzidas para ajudar os clientes a entender o ambiente de negócios mais amplo, bem como os pontos fortes e fracos dos principais atores da indústria. Os dados são analisados qualitativamente para categorizar as empresas como pure play, focadas em categorias, focadas na indústria e diversificadas; são analisados quantitativamente para categorizar as empresas como dominantes, líderes, fortes, tentativas e fracas.
Shape Your Report to Specific Countries or Regions & Enjoy 30% Off!
Desenvolvimentos Recentes
- Em abril de 2025, a Sartorius Stedim Biotech entrou em uma parceria estratégica com a Tulip Interfaces para acelerar a transformação digital na fabricação biofarmacêutica. A Sartorius afirmou que a colaboração visa reduzir erros de processos manuais, melhorar a visibilidade do bioprocessamento de ponta a ponta e apoiar a conformidade regulatória em ambientes de bioprocessamento de uso único.
- Em março de 2025, a Cytiva expandiu seu portfólio Xcellerex X-platform adicionando novos biorreatores de 500L e 2.000L. A Cytiva afirmou que a plataforma mais ampla ajuda os cientistas a escalarem mais suavemente de 50L para 2.000L com maior confiabilidade, flexibilidade e eficiência, o que apoia a consistência do processo para a fabricação biofarmacêutica regulamentada.
- Em fevereiro de 2025, a Thermo Fisher Scientific anunciou um acordo definitivo para adquirir o negócio de Purificação & Filtração da Solventum por aproximadamente $4,1 bilhões em dinheiro. A empresa afirmou que a aquisição é altamente complementar ao seu negócio de bioprodução e fortalecerá suas capacidades em fluxos de trabalho biológicos upstream e downstream, que estão intimamente ligados às necessidades de validação de bioprocessos.
- Em janeiro de 2025, a Repligen lançou o Sistema CTech SoloVPE PLUS, uma nova plataforma de medição de concentração UV-Vis em linha para aplicações de bioprocessamento. A Repligen afirmou que o produto é projetado para oferecer maior precisão, velocidade e facilidade de uso, ajudando os clientes a tomarem decisões de processo mais rápidas e a melhorarem o controle analítico durante a fabricação.
Escopo do Relatório
| Atributo do Relatório |
Detalhes |
| Valor do tamanho do mercado em 2025 |
USD 426,54 milhões |
| Previsão de receita em 2032 |
USD 1093,81 milhões |
| Taxa de crescimento (CAGR) |
14,4% (2025–2032) |
| Ano base |
2025 |
| Período de previsão |
2026-2032 |
| Unidades quantitativas |
USD milhões |
| Segmentos cobertos |
Por Tipo de Teste; Por Componente do Processo; Por Estágio do Bioprocesso; Por Usuário Final |
| Escopo regional |
América do Norte, Europa, Ásia-Pacífico, América Latina, Oriente Médio & África |
| Principais empresas perfiladas |
Thermo Fisher Scientific Inc.; Merck KGaA; Sartorius AG; SGS SA; Eurofins Scientific; Pall Corporation; Charles River Laboratories; WuXi AppTec; Nelson Laboratories; TÜV SÜD |
| Número de Páginas |
332 |
Segmentação
Por Tipo de Teste
- Serviços de Testes de Extraíveis/Lixiviáveis
- Serviços de Testes Microbiológicos
- Serviços de Testes Fisicoquímicos
- Serviços de Testes de Integridade
- Serviços de Testes de Compatibilidade
- Outros Tipos de Testes
Por Componente do Processo
- Elementos de Filtro
- Recipientes e Sacos de Meio
- Biorreatores
- Sistemas de Mistura
- Sacos de Processo de Congelamento e Descongelamento
- Outros Componentes do Processo
Por Etapa do Bioprocesso
- Bioprocessamento Upstream
- Bioprocessamento Downstream
- Operações de Enchimento e Acabamento
Por Usuário Final
- Empresas Farmacêuticas
- Empresas de Biotecnologia
- CDMOs
- Outros Usuários Finais
Por Região
- América do Norte
- Europa
- Alemanha
- França
- Reino Unido
- Itália
- Espanha
- Resto da Europa
- Ásia-Pacífico
- China
- Japão
- Índia
- Coreia do Sul
- Sudeste Asiático
- Resto da Ásia-Pacífico
- América Latina
- Brasil
- Argentina
- Resto da América Latina
- Médio Oriente & África
- Países do GCC
- África do Sul
- Resto do Médio Oriente e África




