生物工艺验证市场概况:
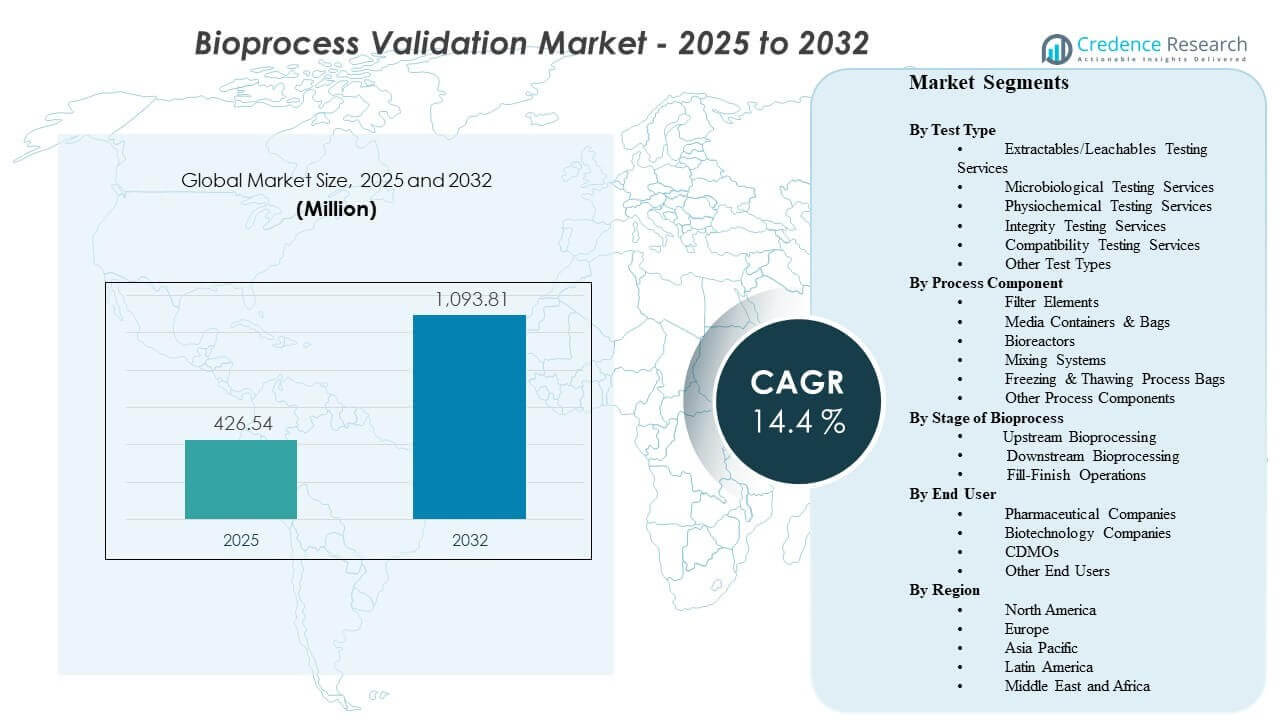
全球生物工艺验证市场规模预计在2025年达到4.2654亿美元,并预计到2032年将达到10.9381亿美元,2025年至2032年的复合年增长率为14.4%。增长主要由生物制品制造过程中更严格的质量和污染控制期望驱动,这扩大了关键工艺步骤和接触材料的验证范围和频率。需求进一步受到产能增加和外包增长的支持,这增加了全球制造网络中资格认证、方法验证和文档周期的数量。
| 报告属性 |
详情 |
| 历史时期 |
2020-2024 |
| 基准年 |
2025 |
| 预测期 |
2026-2032 |
| 2025年生物工艺验证市场规模 |
4.2654亿美元 |
| 生物工艺验证市场,复合年增长率 |
14.4% |
| 2032年生物工艺验证市场规模 |
10.9381亿美元 |
主要市场趋势与见解
- 市场预计将从4.2654亿美元(2025年)扩展到10.9381亿美元(2032年),复合年增长率为14.4%(2025-2032年)。
- 2025年北美占46.9%,得益于成熟的生物制品制造和高合规强度。
- 可提取物/浸出物测试服务在2025年占37.4%的份额,反映了一次性系统的广泛采用和杂质风险控制期望。
- 过滤元件在2025年占25.6%的份额,强调了无菌保证和完整性验证在验证生产中的核心作用。
- 制药和生物技术公司(合计)在2025年占57.3%的份额,因为赞助商保留对关键质量和释放启用验证活动的直接监督。
细分市场分析
生物工艺验证越来越被视为一个涵盖方法验证、污染控制策略和审核准备文档的端到端程序,而不是一组孤立的测试。随着管道多样化和工艺变更在扩大和生命周期管理中更频繁地发生,验证包必须是可重复的、基于风险的,并与更快的开发时间表兼容。这将需求转向标准化协议、更严格的变更控制链接和支持跨站点和合同伙伴可追溯性的数据系统。
一次性使用的采用和强化的处理设计正在提升材料兼容性、可提取物/浸出物特性以及流体接触组件完整性测试的重要性。同时,后期操作中的无菌制造期望提高了上游到下游交接和灌装环境的验证负担。由于专业测试和产能原因,外包继续扩大,但赞助商通常保持对验收标准、偏差和面向监管的文件的内部管理。
Access crucial information at unmatched prices!
Request your sample report today & start making informed decisions powered by Credence Research Inc.!
Download Sample
按测试类型洞察
可提取物/浸出物测试服务在2025年占据了37.4%的最大份额。其领先地位反映了对接触材料中潜在杂质进行表征的需求,并确保在一次性组件和工艺路径中的兼容性。验证程序越来越需要可以在工艺变更、供应商更新和规模转换中引用的可靠特性。随着开发时间表的压缩,买家更倾向于选择能够结合稳健分析覆盖和与质量文件需求一致的清晰报告的供应商。
按工艺组件洞察
过滤元件在2025年占据了25.6%的最大份额。过滤器是污染控制和无菌保证的核心,这推动了经过验证的制造中反复的资格认证、完整性测试和批次验证。该部分受益于上游和下游操作中过滤器使用的高频率以及在定义的操作范围内验证性能的需求。买家优先考虑一致性、可追溯性和支持审计和内部质量审查的完善性能声明。
按生物工艺阶段洞察
上游生物加工在2025年占据了51.6%的最大份额。上游操作通常经历最高的工艺调整和规模扩展变化率,这扩大了方法、采样计划和控制策略的验证活动。早期阶段步骤中的变异性风险也增加了对验证的依赖,以证明跨运行和站点的一致性能。随着组织采用强化和封闭的处理方法,上游验证越来越强调稳健的监控、污染控制和可重复的文件包。
按终端用户洞察
制药公司和生物技术公司(合计)在2025年占据了57.3%的最大份额。赞助商通常保留核心验证管理,以保持对验收标准、偏差和面向监管的证据包的直接控制。内部团队还管理方法转移决策、可比性考虑和触发重新验证的生命周期更新。即使在更广泛的外包情况下,赞助商通常也期望外部合作伙伴提供标准化的输出,能够顺利整合到内部质量系统和审计流程中。
生物工艺验证市场驱动因素
扩大的生物制品制造和产能增加
生物制剂生产的增长增加了必须满足验证状态期望的设施、生产线和站点的数量。每次扩展都会在设备、公用设施和关键工艺步骤中引入资格和验证周期。多站点供应策略进一步提高了对标准化验证包和一致性文件的需求。随着组织加速扩展,他们依赖可重复的、基于风险的验证框架来减少延迟并避免批次中断。
- 例如,三星生物制剂于2025年4月完成了5号工厂的建设,增加了18万升的生物制造能力,使公司在松岛站点及新收购的位于马里兰州罗克维尔的6万升设施的全球总生产能力达到84.5万升,成为全球按安装容量计算最大的CDMO。
对污染控制和无菌保证的合规期望上升
无菌和低生物负荷要求增加了对过程控制、完整性验证和环境策略的验证强度。质量团队越来越期望有证据表明污染风险在整个过程路径中得到控制,而不仅仅是在最终步骤。这扩大了支持污染控制计划的微生物学、完整性测试和兼容性检查的测试需求。强有力的文件和可追溯性是满足审计期望的核心。
一次性使用推动材料和兼容性验证
向一次性组件的转变增加了在操作条件下验证接触材料、可浸出物风险和工艺兼容性的需求。验证必须解决供应商差异、组件配置变化和生命周期更新。买家寻求可在产品和生产线中重复使用的测试方法和报告,以减少重复工作。这种动态支持了对可提取物/浸出物和兼容性测试服务的持续需求。
- 例如,富士胶片迪奥森生物技术公司成功地将其一次性生物制造平台从美国北卡罗来纳州复制到英国比灵汉姆设施,仅用14个月就交付了英国首个cGMP一次性制造设施,并在原项目计划提前三个月开始运营,这得益于标准化的资格包和跨站点的知识转移。
外包增长与可扩展验证能力的需求
发起方越来越多地使用外部合作伙伴来管理产能限制、专业方法和周转时间需求。外包可以减少开发和商业支持中的瓶颈,特别是在扩大规模和产品过渡期间。然而,发起方的质量组织仍然需要符合内部治理和审计需求的标准化交付物。这推动服务提供商在合规成熟度、文件质量和一致执行方面进行差异化。
生物工艺验证市场挑战
随着测试菜单的扩展和文档要求在各个站点和合作伙伴之间增加,验证程序可能会变得资源密集。组织通常在对齐验收标准、变更控制和证据包方面遇到困难,这可能导致内部团队和外包实验室之间的返工和延误。方法转移和供应商更改引入了额外的验证周期,这些周期很难在异构制造环境中标准化。在不影响质量的情况下管理时间表仍然是一个持续的运营紧张点。
随着管道的多样化和流程通过生命周期变化而演变,复杂性也在增加,这增加了可能触发部分重新验证的更新频率。数据完整性和可追溯性期望需要更强的系统、受控记录和审计准备,这增加了赞助商和服务提供商的开销。区域监管期望和检查重点的差异可能进一步使全球标准化复杂化。这些压力增加了对治理、模板和可重复验证手册的需求。
- 例如,百时美施贵宝在需要将传统的Celgene CTMS和传统的BMS CTMS两个具有不同文档架构的独立平台整合为一个全球统一的试验管理系统时,面临系统碎片化的直接运营后果;该公司全球运营的全面实施在不到20个月内完成。
生物工艺验证市场趋势和机会
组织正在转向集成验证包,将分析、微生物和完整性测试输出链接到审计准备就绪的证据结构中。这有利于那些具有广泛能力和强大质量系统的提供商,他们可以在方法和站点之间提供标准化报告。对更快的周转和更清晰的文档结构的需求也在增长,这支持更快的审查周期和发布决策。用于跟踪、趋势分析和文档控制的数字化使能正在成为供应商选择中的实际差异化因素。
- 例如,Eurofins生物制药产品测试在超过20个国家运营着一个由46个统一的GMP实验室组成的网络,所有这些都由单一的全球质量政策手册和统一的eLIMS-BPT平台、电子实验室笔记本(ELN)以及覆盖全球28个地点的集中LabAccess℠客户端门户管理,这种配置能够在大规模上实现标准化的跨站点文档和审计准备就绪的报告。
一次性扩展和强化处理设计正在为可重复的材料资格框架创造机会,这些框架可以在多个产品和平台上利用。随着外包的扩大,CDMO和专业测试提供商可以通过提供端到端验证支持来减少赞助商的工作量并压缩时间表,从而实现增长。对简化多站点转移和生命周期更新的统一验证方法的需求也在增加。这些趋势支持能够将产能与一致的高合规执行相结合的公司的增长。
区域见解
北美
北美在2025年的收入中占46.9%,得益于成熟的生物制剂制造、密集的CDMO生态系统和高合规强度。区域需求由频繁的规模扩大和生命周期管理活动驱动,这些活动会触发重新验证和方法更新。买家倾向于优先考虑审核准备就绪的文件、可预测的周转时间以及多个设施之间的一致执行。该地区还支持对完整性测试和污染控制对齐验证工作流程的强劲需求。
欧洲
欧洲在2025年的收入中占22.4%,得益于广泛的受监管制造和跨境生产网络。验证需求因需要标准化的证据包而得到加强,这些证据包可以在多国供应链中使用。买家通常强调协调的程序、强大的质量体系和稳健的变更控制文件。成熟的生物制剂中心和CDMO支持了对测试类型和工艺组件的稳定需求。
亚太地区
亚太地区在2025年的收入中贡献了21.3%,反映了产能的扩张和在全球外包和制造网络中参与度的增加。增长得益于新设施建设、平台扩展和标准化质量体系的日益采用。该地区的赞助商和CDMO越来越寻求可扩展的验证能力,具有与全球审核对齐的清晰文件格式。在一次性使用的采用和快速规模扩大增加材料和完整性验证需求的情况下,需求尤其强劲。
拉丁美洲
拉丁美洲在2025年的收入中占5.6%,需求集中在本地化制造、与进口相关的质量活动和区域生产中心。验证需求通常由基于项目的产能增加和质量体系升级所塑造。买家通常专注于在资源限制更紧的情况下确保合规文件和可靠执行。随着能力的扩展,对外包验证和标准化测试包的需求预计将增强。
中东和非洲
中东和非洲在2025年的收入中占3.8%,反映了较小的安装基础,但对本地化制造和无菌能力建设的兴趣增加。验证需求通常与新项目、设施升级以及加强受监管生产基础设施的举措相关。买家优先考虑基础质量体系、可重复的验证手册以及合作伙伴对文件准备的支持。增长预计将跟随制造投资和能力发展的步伐。
竞争格局
竞争由能力广度、合规成熟度、周转绩效以及提供标准化、审核就绪的文档并能整合到赞助商质量系统中的能力所塑造。供应商通过在分析、微生物和完整性测试中提供捆绑验证工作流程以及变更控制和生命周期更新的咨询支持来实现差异化。规模、地理实验室网络以及跨地点的一致执行对于大型生物制药项目和多地点制造策略至关重要。服务提供商还在污染控制、材料兼容性和发布支持测试等高审查领域的专业化方面展开竞争。
赛默飞世尔科技公司在支持验证生物加工的技术和服务方面处于领先地位,具有跨生物生产、分析和质量支持的集成工作流程的优势。该公司的方法通常强调产品组合的广度以及在开发和制造环境中支持标准化实践的能力。这与买家对可重复验证框架的需求很好地契合,这些框架可以应用于不同地点和产品。规模和集成能力可以支持更快的验证解决方案部署和一致的文档结构。
行业研究和增长报告包括对市场竞争格局的详细分析以及关于主要公司的信息,包括:
- 赛默飞世尔科技公司
- 默克集团
- 赛多利斯股份公司
- SGS集团
- 欧陆科学
- 颇尔公司
- 查尔斯河实验室
- 药明康德
- 纳尔逊实验室
- 德国南德意志集团
对公司的定性和定量分析已进行,以帮助客户了解更广泛的商业环境以及主要行业参与者的优劣势。数据通过定性分析将公司分类为纯粹型、类别聚焦型、行业聚焦型和多元化型;通过定量分析将公司分类为主导型、领先型、强势型、暂定型和弱势型。
Shape Your Report to Specific Countries or Regions & Enjoy 30% Off!
最新动态
- 2025年4月,Sartorius Stedim Biotech与Tulip Interfaces达成战略合作伙伴关系,以加速生物制药制造的数字化转型。Sartorius表示,此次合作旨在减少手动流程错误,提高端到端生物制造的可视性,并支持一次性生物加工环境中的合规性。
- 2025年3月,Cytiva通过新增500L和2000L生物反应器扩展了其Xcellerex X平台产品组合。Cytiva表示,扩展的平台帮助科学家更顺利地从50L扩展到2000L,并提高了可靠性、灵活性和效率,从而支持受监管生物制造的过程一致性。
- 2025年2月,Thermo Fisher Scientific宣布达成最终协议,以约41亿美元现金收购Solventum的纯化和过滤业务。公司表示,此次收购与其生物生产业务高度互补,将增强其在上游和下游生物制品工作流程中的能力,这些流程与生物工艺验证需求密切相关。
- 2025年1月,Repligen推出了CTech SoloVPE PLUS系统,这是一种用于生物加工应用的新的在线UV-Vis浓度测量平台。Repligen表示,该产品旨在提供更高的准确性、速度和易用性,帮助客户更快地做出工艺决策,并在制造过程中提高分析控制。
报告范围
| 报告属性 |
详细信息 |
| 2025年市场规模价值 |
4.2654亿美元 |
| 2032年收入预测 |
10.9381亿美元 |
| 增长率(CAGR) |
14.4%(2025–2032) |
| 基准年 |
2025 |
| 预测期 |
2026-2032 |
| 定量单位 |
百万美元 |
| 涵盖的细分市场 |
按测试类型;按工艺组件;按生物工艺阶段;按最终用户 |
| 区域范围 |
北美、欧洲、亚太地区、拉丁美洲、中东和非洲 |
| 重点公司简介 |
Thermo Fisher Scientific Inc.; Merck KGaA; Sartorius AG; SGS SA; Eurofins Scientific; Pall Corporation; Charles River Laboratories; WuXi AppTec; Nelson Laboratories; TÜV SÜD |
| 页数 |
332 |
细分
按测试类型
- 可提取物/浸出物测试服务
- 微生物测试服务
- 理化测试服务
- 完整性测试服务
- 兼容性测试服务
- 其他测试类型
按工艺组件
- 过滤元件
- 介质容器和袋
- 生物反应器
- 混合系统
- 冷冻和解冻工艺袋
- 其他工艺组件
按生物工艺阶段
按终端用户
- 制药公司
- 生物技术公司
- 合同开发和制造组织 (CDMOs)
- 其他终端用户
按地区




