Обзор рынка контрактного производства биофармацевтических препаратов:
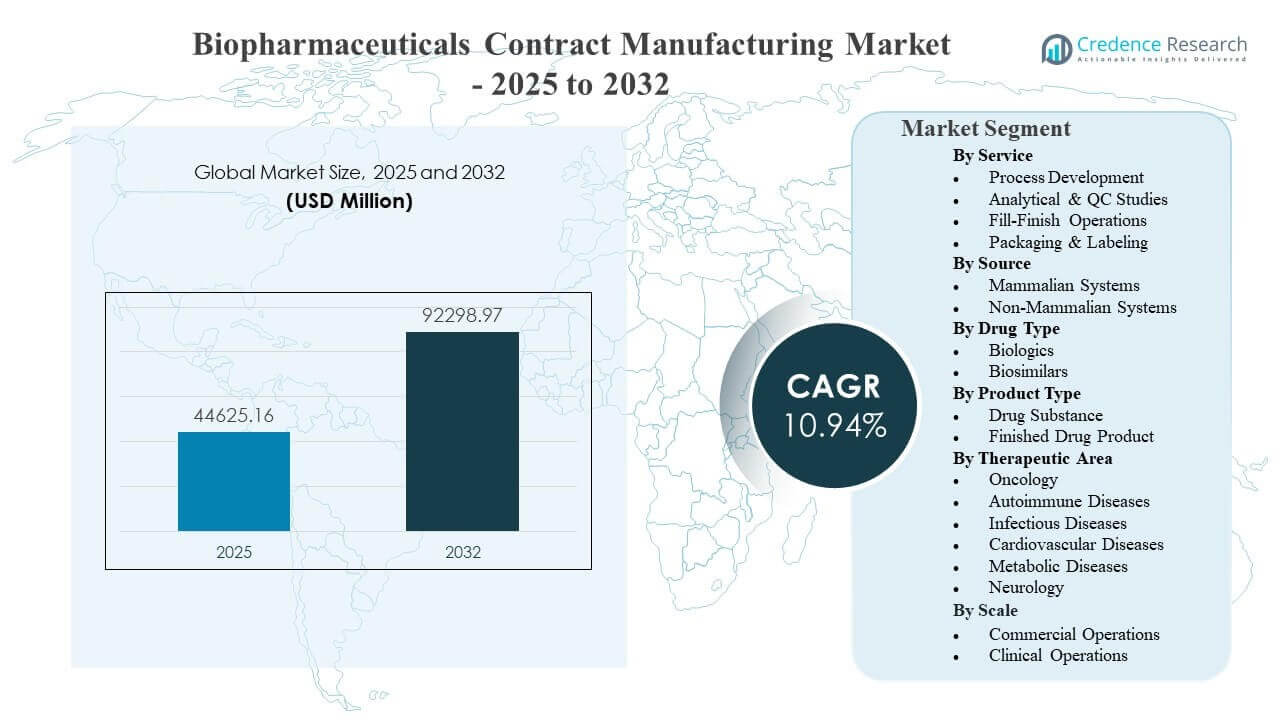
Глобальный размер рынка контрактного производства биофармацевтических препаратов был оценен в 44,625.16 млн долларов США в 2025 году и, по прогнозам, достигнет 92,298.97 млн долларов США к 2032 году, увеличиваясь с совокупным годовым темпом роста (CAGR) 10.94% с 2025 по 2032 год. Спрос в основном обусловлен увеличением аутсорсинга со стороны спонсоров биофармацевтики для ускорения разработки и масштабирования, управления капиталоемкостью, соблюдения нормативных требований и рисков выхода на рынок в сложных биологических модальностях. Расширение мощностей в крупномасштабном производстве биопрепаратов и растущее предпочтение к полным партнерствам с CDMO дополнительно укрепляют рост рынка, при этом решения об аутсорсинге все чаще связаны со скоростью передачи технологий, глубиной аналитики и надежным выполнением коммерческих поставок.
| АТРИБУТ ОТЧЕТА |
ДЕТАЛИ |
| Исторический период |
2020-2024 |
| Базовый год |
2025 |
| Прогнозируемый период |
2026-2032 |
| Размер рынка контрактного производства биофармацевтических препаратов 2025 |
44,625.16 млн долларов США |
| Рынок контрактного производства биофармацевтических препаратов, CAGR |
10.94% |
| Размер рынка контрактного производства биофармацевтических препаратов 2032 |
92,298.97 млн долларов США |
Ключевые рыночные тенденции и инсайты
- Разработка процессов составила наибольшую долю в 37.8% в 2025 году, отражая высокий спрос на услуги по передаче технологий, масштабированию и устойчивости процессов.
- Системы млекопитающих занимали 58.3% доли в 2025 году, поддерживаемые широким использованием в сложных биопрепаратах, требующих посттрансляционных модификаций, подобных человеческим.
- Онкология представляла 32.4% доли в 2025 году, обусловленную устойчивой активностью в области биопрепаратов и высокой интенсивностью производства в процессе разработки и поставок.
- Северная Америка внесла 35.80% доли в 2025 году, поддерживаемая глубокой базой инноваторов и высокими требованиями к коммерческому производству биопрепаратов.
- Ожидается, что биосимиляры будут расширяться с CAGR 12.25% в прогнозируемый период, отражая экономически обоснованное внедрение и расширяющиеся потребности в выполнении проектов.
Анализ сегментов
Рынок продолжает смещаться в сторону моделей аутсорсинга, которые снижают постоянные производственные нагрузки, улучшая скорость и гибкость в клинических и коммерческих программах. Спонсоры все чаще предпочитают поставщиков, которые могут предоставить интегрированные рабочие процессы, охватывающие разработку, аналитику и передачу производства с минимальными трениями, особенно там, где производительность процессов и регуляторная согласованность строго контролируются. Это усиливает спрос на пакеты услуг, которые объединяют проектирование процессов, стратегии аналитического контроля и готовность к выполнению масштабирования.
Принятие оперативных решений также формируется доступом к мощностям, качественной репутацией и способностью управлять изменчивостью в сложных биологических продуктах. Покупатели придают большое значение надежным аналитическим и QC структурам, которые поддерживают уверенность в выпуске и сопоставимость, особенно при переходе от клинических к коммерческим операциям. По мере расширения трубопроводов и увеличения разнообразия молекул, CDMO получают выгоду от спроса на модульные мощности, стандартизированные платформы и упрощенные пути передачи технологий.
Access crucial information at unmatched prices!
Request your sample report today & start making informed decisions powered by Credence Research Inc.!
Download Sample
По Инсайтам Услуг
Разработка процессов составила наибольшую долю 37,8% в 2025 году. Это лидерство поддерживается необходимостью определения масштабируемых, воспроизводимых процессов на ранних стадиях, чтобы снизить риски на последующих этапах и предотвратить дорогостоящие неудачи. Спонсоры все чаще полагаются на CDMO для экспертного знания платформенных процессов, устранения проблем с масштабированием и оптимизации, которая улучшает выходы и контроль примесей. Интегрированные пути от разработки до производства также сокращают задержки, уменьшая передачу между лабораторной работой и выполнением GMP производства.
По Инсайтам Источников
Млекопитающие системы составили наибольшую долю 58,3% в 2025 году. Платформы на основе млекопитающих остаются предпочтительными для многих биопрепаратов, где сложная экспрессия белков и гликозилирование, подобное человеческому, критически важны для эффективности и безопасности. Высокие объемы моноклональных антител и рекомбинантных белков поддерживают высокую загрузку мощностей на основе млекопитающих как в клинических, так и в коммерческих операциях. CDMO с проверенными платформами на основе млекопитающих и глубокой аналитической базой лучше подготовлены для заключения долгосрочных соглашений на поставку и многопродуктовых портфелей.
По Инсайтам Типа Лекарств
Биопрепараты продолжают представлять собой основную объемную базу для контрактного производства, поскольку значительная часть клинических трубопроводов и коммерческих портфелей зависит от надежных возможностей производства биопрепаратов. Спонсоры все чаще ищут партнеров, которые могут поддерживать несколько типов молекул с постоянными системами качества и воспроизводимой производственной производительностью. Биоаналоги добавляют импульс через программы, ориентированные на стоимость, которые требуют эффективного выполнения производства, сильного планирования сопоставимости и дисциплинированных стратегий аналитического контроля. Конкурентное позиционирование в этом измерении часто зависит от способности обеспечивать как эффективность затрат, так и постоянное соблюдение требований при переходах масштаба.
По Инсайтам Типа Продукта
Аутсорсинг лекарственного вещества остается тесно связанным со спросом на мощности биореакторов, экспертизу в области upstream и downstream, а также дисциплины контроля процессов, которые трудно воспроизвести внутри компании с сопоставимой скоростью. Требования к готовым лекарственным продуктам усиливают спрос на стерильные операции, целостность контейнера и процессы обеспечения качества с высокими последствиями, которые поддерживают готовность к коммерческому распространению. Многие спонсоры отдают приоритет партнерам, которые могут координировать рабочие процессы от лекарственного вещества до заполнения, чтобы снизить риск передачи, улучшить надежность графика и укрепить уверенность в выпуске. Стремление к интегрированным предложениям также поддерживает более простые модели управления и меньшее количество операционных передач по всей цепочке поставок.
По Инсайтам Терапевтической Области
Онкология составила наибольшую долю, 32,4% в 2025 году. Высокий уровень активности в разработке биопрепаратов в области онкологии поддерживает спрос на сложные производственные программы с жесткими аналитическими и качественными требованиями. Программы часто требуют гибкого планирования мощностей из-за множества показаний, изменяющихся требований к дозировке и изменяющихся сроков на различных этапах испытаний. CDMO, которые могут быстро масштабироваться и поддерживать стабильное качество, пользуются спросом, особенно там, где спонсорам необходима стабильная поставка в рамках многострановой разработки и ранних коммерческих запусков.
По данным о масштабах
Коммерческие операции обычно поддерживаются долгосрочными контрактами на аутсорсинг, где решающими критериями покупки являются обеспечение поставок, проверенные процессы и готовность к регулированию. Рост клинических операций подкрепляется широтой активов в разработке, требующих гибкого размера партий, быстрого выполнения и адаптируемого планирования. Спонсоры все чаще структурируют стратегии аутсорсинга, чтобы зарезервировать мощности для ожидаемого продвижения программы, избегая при этом чрезмерных обязательств на ранних этапах клинических рисков. Решения о масштабе также зависят от сочетания модальностей, причем специализированные биопрепараты часто требуют индивидуального выполнения и более высокой интенсивности услуг.
Драйверы рынка контрактного производства биофармацевтических препаратов
Расширение биологических конвейеров и сложность производства
Биофармацевтические конвейеры продолжают расширяться за счет моноклональных антител и других сложных биологических форматов, требующих сложных производственных контролей и дисциплины соблюдения. Операционная нагрузка на разработку процессов, проектирование аналитической стратегии и выполнение масштабирования приводит к аутсорсингу специализированным партнерам. CDMO выигрывают, когда они могут стандартизировать выполнение через платформенные процессы, поддерживая при этом специфические для молекулы требования. Эта комбинация улучшает скорость, снижает риск отказов и поддерживает повторяемое качество в рамках нескольких программ.
- Например, WuXi Biologics заявила, что ее платформа клеточных линий 4-го поколения WuXia TrueSite TI достигает средних титров моноклональных антител выше 8,0 г/л, поддерживает стабильную экспрессию в более чем 99% клонированных клеточных линий после 60 пассажей и поддерживает масштабирование свыше 20 000 л, демонстрируя, как платформенные системы могут справляться со сложными молекулярными требованиями в промышленных масштабах.
Необходимость ускорения сроков разработки и передачи технологий
Спонсоры все чаще отдают приоритет скорости выхода на клинику и рынок, что повышает ценность опытных партнеров, способных быстро выполнять передачу технологий и масштабирование. CDMO, предлагающие интегрированную разработку, аналитику и GMP-производство, сокращают задержки передачи и сложность управления. Быстрые переходы между этапами также улучшают пропускную способность портфеля и позволяют спонсорам выделять внутренние ресурсы на приоритеты НИОКР. Этот драйвер усиливается, когда клинические сроки конкурентоспособны, а дифференциация продукта зависит от скорости выполнения.
Требования к качеству, соблюдению и аналитическому контролю
Производство биопрепаратов требует строгого контроля за примесями, изменчивостью процесса и сопоставимостью продукции, что усиливает спрос на сильные аналитические и QC возможности. Аутсорсинг поддерживает доступ к установленным системам качества, проверенным методам и опыту в области готовности к регулированию. Спонсоры также предпочитают партнеров с доказанной эффективностью в управлении отклонениями, строгой документацией и готовностью к аудитам. Акцент на постоянное качество поддерживает повторные заказы и долгосрочные коммерческие отношения по поставкам.
Доступ к мощностям и обеспечение масштабируемых коммерческих поставок
Коммерческие биопрепараты требуют надежного доступа к крупномасштабным мощностям и стабильной производительности. Создание или расширение внутренних мощностей требует значительных капитальных вложений и времени, что побуждает спонсоров передавать производство проверенным поставщикам с гибкими производственными возможностями. CDMO, которые расширяют мощности и модернизируют объекты, укрепляют свою способность поддерживать долгосрочные контракты. Этот фактор подкрепляется необходимостью управления непрерывностью поставок и снижения риска задержек запуска или нехватки запасов.
- Например, Samsung Biologics сообщила, что завод 4 добавляет 240 000 литров мощности и увеличивает общую мощность на Bio Campus I до 604 000 литров, иллюстрируя, как расширение крупномасштабных возможностей укрепляет поддержку долгосрочных коммерческих поставок. CDMO, которые расширяют мощности и модернизируют объекты, укрепляют свою способность поддерживать долгосрочные контракты.
Проблемы рынка контрактного производства биофармацевтических препаратов
Ограничения по мощности и длительные сроки остаются проблемой, так как спонсоры конкурируют за квалифицированные места для производства биопрепаратов и проверенные возможности заполнения и завершения. Даже при наличии мощности согласование графиков с этапами программы может быть сложным из-за изменчивости клинических результатов и изменяющихся профилей спроса. Эти ограничения могут увеличить ценовое давление и усложнить управление аутсорсингом, особенно для средних спонсоров. Риск выполнения увеличивается, когда происходит несколько технологических трансферов на разных площадках или когда производственные сети перераспределяются.
- Например, расширение FUJIFILM Diosynth Biotechnologies в Хиллерёде, которое удвоило мощность по производству лекарственных веществ до 12 × 20 000L биореакторов, только запланировало начало производства заполнения и завершения на середину 2025 года как отдельную фазу, подчеркивая, как проверенные возможности заполнения и завершения отстают от добавления мощности на начальных этапах и увеличивают разрыв в графике для спонсоров, требующих комплексных слотов.
Регуляторная и качественная сложность также создает проблемы, особенно когда спонсоры требуют постоянного соответствия по всей многоуровневой цепочке поставок. Изменчивость в ожиданиях по документации, готовности к инспекциям и процессах управления изменениями может замедлить сроки и увеличить операционные накладные расходы. Отклонения в процессе или проблемы с аналитической сопоставимостью могут привести к переработке, задержкам или дополнительным исследованиям. Поддержание постоянного качества при быстром масштабировании остается центральным операционным и репутационным риском как для спонсоров, так и для CDMO.
Тенденции и возможности рынка контрактного производства биофармацевтических препаратов
Рынок движется в сторону интегрированных, комплексных партнерств с CDMO, где спонсоры отдают предпочтение меньшему количеству поставщиков и более упрощенному выполнению цепочки поставок. Растет спрос на поставщиков, которые могут связать разработку процессов, аналитический контроль, производство по стандартам GMP и операции по заполнению и окончательной обработке в рамках единой системы качества. Это снижает трения при передаче и поддерживает предсказуемые переходы масштаба. Поставщики с сильным управлением проектами и стандартизированными моделями передачи технологий получают преимущество.
- Например, Mabion, CDMO, ориентированная на биопрепараты, продемонстрировала ощутимый эффект этой интегрированной модели, когда полностью согласованный, комплексный подход к производству, охватывающий разработку процессов на начальных этапах до выпуска партии по стандартам GMP в рамках единой системы качества, сократил предполагаемое время выпуска первой партии GMP на 40%, при этом достигнув трехкратного снижения отклонений благодаря более строгому контролю за критическими атрибутами качества и аналитикой в процессе на всем протяжении от разработки до выпуска.
Возможности также увеличиваются в области передовой аналитики, цифрового мониторинга процессов и модернизации производства, что улучшает согласованность партий и видимость операций. Спонсоры ценят партнеров, которые могут сократить расследования, поддержать более быстрое принятие решений о выпуске и обеспечить более сильную поддержку управления жизненным циклом. Модульные объекты и гибкие конфигурации производства расширяют адресные программы, позволяя быстрее проводить изменения и лучше использовать ресурсы. Эти тенденции поддерживают дифференциацию за счет скорости, прозрачности и согласованного выполнения.
Региональные особенности
Северная Америка
Северная Америка составила 35,80% доли в 2025 году, поддерживаемая высокой плотностью инноваций в области биопрепаратов и сильными коммерческими требованиями к производству. Регион выигрывает от установленных регуляторных и качественных экосистем, которые усиливают аутсорсинг для программ с высоким уровнем соответствия. Покупатели часто отдают предпочтение опыту, гарантии масштаба и интегрированным возможностям обслуживания в области разработки и производства. Сильный спрос со стороны крупных спонсоров и широкая клиническая линия поддерживают использование мощностей и долгосрочные контракты.
Европа
Европа заняла 26,70% доли в 2025 году, поддерживаемая зрелыми CDMO, сильными возможностями GMP и установленными кластерами производства биопрепаратов. Региональная сила подкрепляется высокими стандартами в системах качества, опытными регуляторными операциями и сильными техническими кадровыми ресурсами. Спрос на аутсорсинг поддерживается как в клинических, так и в коммерческих программах, особенно там, где требуются специализированные возможности. Конкурентное позиционирование часто зависит от надежности, производительности в области соответствия и многообъектных производственных сетей.
Азиатско-Тихоокеанский регион
Азиатско-Тихоокеанский регион представил 29,10% доли в 2025 году, поддерживаемый расширяющимися крупномасштабными мощностями и увеличением импульса аутсорсинга как для разработки, так и для производства. Регион выигрывает от продолжающихся инвестиций в современные объекты, стандартизацию процессов и интеграцию цепочки поставок. Спонсоры используют Азиатско-Тихоокеанский регион для улучшения масштабируемости и доступа к мощностям, сохраняя при этом высокие ожидания по качеству. Рост подкрепляется увеличением мощностей, конкурентной экономикой и расширением активности в области биопрепаратов по региональным центрам.
Латинская Америка
Латинская Америка составила 5,40% доли в 2025 году, отражая меньшую, но растущую роль в поддержке регионального производства и удовлетворении потребностей в упаковке или наполнении. Рост спроса связан с локализованными стратегиями поставок, региональными требованиями доступа и постепенным расширением возможностей. Спонсоры могут привлекать региональных партнеров, где близость и преимущества регионального распределения имеют значение. Продолжение инвестиций в качество и готовность к соблюдению норм остается критически важным для масштабирования работ с более высокой стоимостью биопрепаратов.
Ближний Восток и Африка
Ближний Восток и Африка захватили 3,00% доли в 2025 году, поддерживаемые избирательным развитием мощностей и увеличением внимания к укреплению региональных цепочек поставок здравоохранения. Спрос на аутсорсинг возникает в целевых областях, таких как упаковка, маркировка и локализованная поддержка производства. Рост обусловлен инвестициями, управляемыми политикой, расширением инфраструктуры и улучшением систем качества. Масштабирование производства биопрепаратов более высокой сложности будет зависеть от продолжения наращивания возможностей и развития рабочей силы.
Конкурентная среда
Конкуренция формируется способностью обеспечивать надежные мощности, высокую производительность в области соблюдения норм и широкий спектр интегрированных услуг в разработке, аналитике и производстве. Поставщики выделяются за счет масштаба, технологических платформ, скорости передачи технологий и последовательности выполнения в мультисайтовых сетях. Долгосрочные контракты часто отражают сочетание обеспечения коммерческих поставок и возможностей управления жизненным циклом. CDMO, которые могут согласовать управление, прозрачность и операционную дисциплину с ожиданиями спонсоров, лучше позиционируются для привлечения повторного бизнеса.
Lonza Group остается видным участником с сильным акцентом на масштабируемое производство биопрепаратов и интегрированные услуги от разработки до коммерциализации. Позиционирование компании выигрывает от глубоких знаний процессов, зрелости системы качества и способности поддерживать сложные программы биопрепаратов на различных этапах. Подход компании укрепляется дисциплиной планирования мощностей и акцентом на операционную надежность для долгосрочных отношений поставок. Этот профиль хорошо соответствует спросу спонсоров на предсказуемое выполнение и снижение рисков цепочки поставок.
Отчет об исследовании и росте отрасли включает детализированные анализы конкурентной среды рынка и информацию о ключевых компаниях, включая:
- Lonza Group
- Thermo Fisher Scientific, Inc.
- Samsung Biologics
- WuXi Biologics
- Boehringer Ingelheim GmbH
- Catalent, Inc.
- FUJIFILM Diosynth Biotechnologies
- AGC Biologics
- Rentschler Biotechnologie GmbH
- AbbVie Inc.
- Merck KGaA
- Inno Biologics Sdn Bhd
Качественный и количественный анализ компаний был проведен, чтобы помочь клиентам понять более широкую бизнес-среду, а также сильные и слабые стороны ключевых игроков отрасли. Данные качественно анализируются для классификации компаний как чисто игровых, ориентированных на категорию, ориентированных на отрасль и диверсифицированных; они количественно анализируются для классификации компаний как доминирующих, ведущих, сильных, временных и слабых.
Shape Your Report to Specific Countries or Regions & Enjoy 30% Off!
Последние события
- В марте 2026 года Catalent заключила глобальное партнерство с GelMEDIX для разработки и клинического производства терапий, полученных из индуцированных плюрипотентных стволовых клеток (iPSC), при этом Catalent также предоставляет линии iPSC, соответствующие требованиям GMP, и поддержку в разработке процессов, аналитическом развитии, масштабировании и производстве по стандартам GMP на клинических стадиях.
- В феврале 2026 года Samsung Biologics заключила партнерство с CEPI для укрепления производства вакцин, готовых к вспышкам, и соглашение включало начальный бюджет до 20 миллионов долларов США для создания масштабируемого процесса быстрого реагирования на производство рекомбинантных белковых вакцин с использованием инфраструктуры на основе клеток млекопитающих Samsung Biologics.
- В феврале 2026 года Catalent и S.Biomedics объявили о стратегическом партнерстве для поддержки разработки и производства TED-A9, который в объявлении описывается как программа аллогенной терапии плюрипотентными стволовыми клетками S.Biomedics.
- В декабре 2025 года AGC Biologics заключила партнерство с ATUM для интеграции платформы экспрессии Leap-In Transposase в свои предложения по разработке клеточных линий, что направлено на увеличение выхода и сокращение сроков разработки для моноклональных антител, мультиспецификов и других сложных биопрепаратов.
Объем отчета
| Атрибут отчета |
Детали |
| Название рынка |
Рынок контрактного производства биофармацевтических препаратов |
| Базовый год и размер |
2025; 44,625.16 миллионов долларов США |
| Прогнозируемый год и размер |
2032; 92,298.97 миллионов долларов США |
| Среднегодовой темп роста и период |
10.94% (2025–2032) |
| Единицы измерения |
миллионы долларов США |
| Охват сегментов |
Услуга, Источник, Тип лекарства, Тип продукта, Терапевтическая область, Масштаб |
| Региональный охват |
Северная Америка; Европа; Азиатско-Тихоокеанский регион; Латинская Америка; Ближний Восток и Африка |
| Компании, охваченные отчетом |
Lonza Group; Thermo Fisher Scientific, Inc.; Samsung Biologics; WuXi Biologics; Boehringer Ingelheim GmbH; Catalent, Inc.; FUJIFILM Diosynth Biotechnologies; AGC Biologics; Rentschler Biotechnologie GmbH; AbbVie Inc.; Merck KGaA; Inno Biologics Sdn Bhd |
| Оценочные страницы |
340 |
Сегментация
По услуге
- Разработка процессов
- Аналитические и QC исследования
- Операции по заполнению и окончательной обработке
- Упаковка и маркировка
По источнику
- Млекопитающие системы
- Немлекопитающие системы
По типу лекарственного средства
По типу продукта
- Активное вещество
- Готовый лекарственный продукт
По терапевтической области
- Онкология
- Аутоиммунные заболевания
- Инфекционные заболевания
- Сердечно-сосудистые заболевания
- Метаболические заболевания
- Неврология
По масштабу
- Коммерческие операции
- Клинические операции
По региону
- Северная Америка
- Европа
- Германия
- Франция
- Великобритания
- Италия
- Испания
- Остальная часть Европы
- Азиатско-Тихоокеанский регион
- Китай
- Япония
- Индия
- Южная Корея
- Юго-Восточная Азия
- Остальная часть Азиатско-Тихоокеанского региона
- Латинская Америка
- Бразилия
- Аргентина
- Остальная часть Латинской Америки
- Ближний Восток и Африка
- Страны ССАГПЗ
- Южная Африка
- Остальная часть Ближнего Востока и Африки




