Обзор рынка валидации биопроцессов:
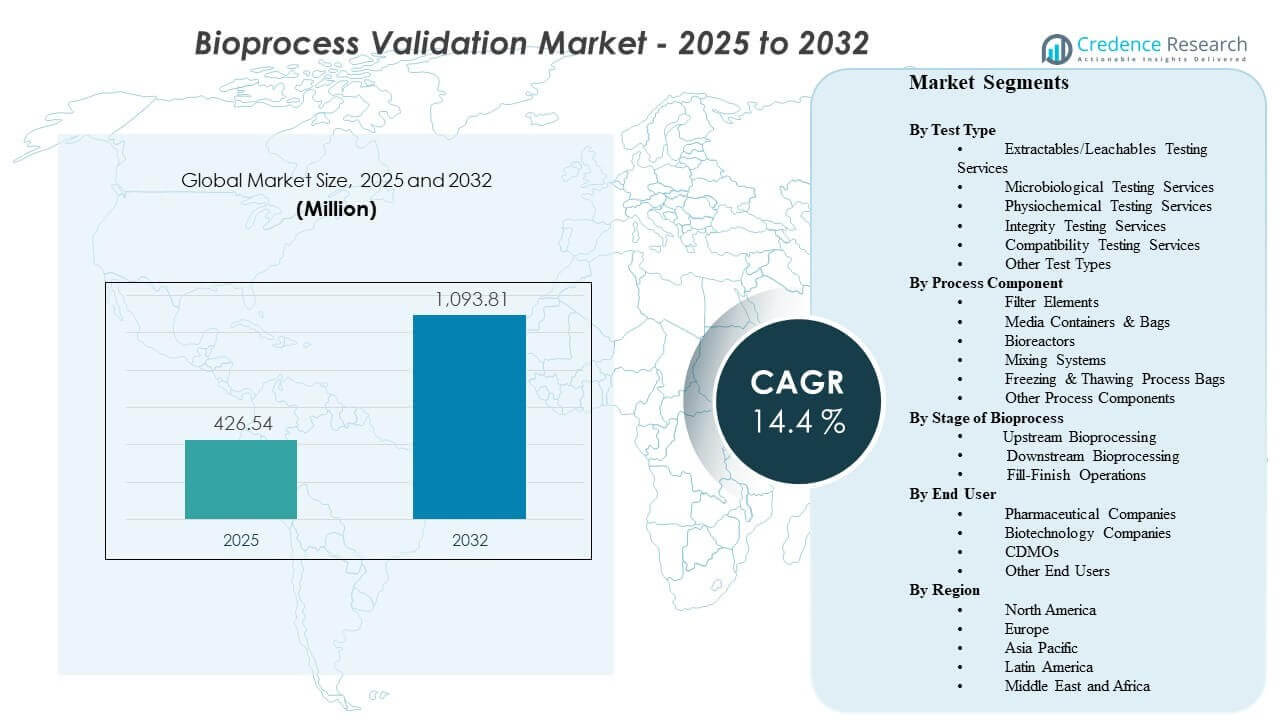
Размер глобального рынка валидации биопроцессов был оценен в 426,54 миллиона долларов США в 2025 году и ожидается, что он достигнет 1093,81 миллиона долларов США к 2032 году, увеличиваясь с совокупным годовым темпом роста (CAGR) 14,4% с 2025 по 2032 год. Рост обусловлен в первую очередь более жесткими ожиданиями по качеству и контролю загрязнений в производстве биопрепаратов, что расширяет объем и частоту валидации на критических этапах процесса и контактных материалах. Спрос также поддерживается увеличением мощностей и ростом аутсорсинга, что увеличивает объем квалификации, валидации методов и циклов документации в глобальных производственных сетях.
| АТРИБУТ ОТЧЕТА |
ДЕТАЛИ |
| Исторический период |
2020-2024 |
| Базовый год |
2025 |
| Прогнозируемый период |
2026-2032 |
| Размер рынка валидации биопроцессов 2025 |
426,54 миллиона долларов США |
| Рынок валидации биопроцессов, CAGR |
14,4% |
| Размер рынка валидации биопроцессов 2032 |
1093,81 миллиона долларов США |
Ключевые тенденции и инсайты рынка
- Ожидается, что рынок расширится с 426,54 миллиона долларов США (2025) до 1093,81 миллиона долларов США (2032) с CAGR 14,4% (2025–2032).
- Северная Америка составила 46,9% в 2025 году, поддерживаемая зрелым производством биопрепаратов и высокой интенсивностью соблюдения норм.
- Услуги по тестированию экстрагируемых/выщелачиваемых веществ заняли 37,4% доли в 2025 году, отражая широкое применение одноразовых систем и ожидания контроля риска загрязнений.
- Элементы фильтров составили 25,6% доли в 2025 году, подчеркивая центральную роль стерильной гарантии и проверки целостности в валидированном производстве.
- Фармацевтические и биотехнологические компании (вместе) захватили 57,3% доли в 2025 году, поскольку спонсоры сохраняют прямой контроль над критическими качественными и валидационными действиями, обеспечивающими выпуск.
Анализ сегмента
Валидация биопроцессов все чаще рассматривается как комплексная программа, охватывающая валидацию методов, стратегию контроля загрязнений и документацию, готовую к аудиту, а не как набор изолированных тестов. По мере того как трубопроводы диверсифицируются и изменения в процессах происходят чаще в ходе масштабирования и управления жизненным циклом, пакеты валидации должны быть повторяемыми, основанными на рисках и совместимыми с более быстрыми сроками разработки. Это смещает спрос в сторону стандартизированных протоколов, более жестких связей управления изменениями и систем данных, поддерживающих прослеживаемость на всех площадках и у контрактных партнеров.
Одноразовое использование и усиленные процессы проектирования повышают важность совместимости материалов, профилей экстрагируемых/вымываемых веществ и тестирования целостности компонентов, контактирующих с жидкостями. Параллельно ожидания в отношении стерильного производства на поздних стадиях операций увеличивают нагрузку на валидацию при передаче от этапа к этапу и в средах заполнения и завершения. Аутсорсинг продолжает расширяться по причинам специализированного тестирования и емкости, но спонсоры обычно сохраняют внутреннее управление критериями приемлемости, отклонениями и документацией для регуляторов.
Access crucial information at unmatched prices!
Request your sample report today & start making informed decisions powered by Credence Research Inc.!
Download Sample
По типу тестирования
Услуги тестирования экстрагируемых/вымываемых веществ составили крупнейшую долю в 37,4% в 2025 году. Их лидерство отражает необходимость характеризовать потенциальные примеси из контактных материалов и обеспечивать совместимость в одноразовых сборках и процессах. Программы валидации все чаще требуют защитимых профилей, которые могут быть использованы при изменениях процессов, обновлениях поставщиков и переходах масштаба. По мере сжатия сроков разработки покупатели предпочитают поставщиков, которые могут сочетать надежное аналитическое покрытие с ясной отчетностью, соответствующей требованиям документации по качеству.
По компонентам процесса
Фильтрующие элементы составили крупнейшую долю в 25,6% в 2025 году. Фильтры являются центральными для контроля загрязнений и обеспечения стерильности, что стимулирует повторяющуюся квалификацию, тестирование целостности и проверку от партии к партии в валидационном производстве. Сегмент выигрывает от высокой частоты использования фильтров в операциях на начальных и конечных этапах и необходимости валидации производительности в определенных рабочих диапазонах. Покупатели отдают приоритет последовательности, отслеживаемости и хорошо документированным заявлениям о производительности, которые поддерживают аудиты и внутренние проверки качества.
По этапу биопроцесса
Начальный биопроцессинг составил крупнейшую долю в 51,6% в 2025 году. Начальные операции обычно испытывают наибольшую частоту настройки процессов и изменений масштаба, что расширяет активность валидации для методов, планов отбора проб и стратегий контроля. Риски изменчивости на ранних стадиях также увеличивают зависимость от валидации для демонстрации стабильной производительности в разных запусках и на разных площадках. По мере того как организации принимают усиленные и закрытые подходы к обработке, валидация на начальных этапах все больше подчеркивает надежный мониторинг, контроль загрязнений и повторяемые пакеты документации.
По конечным пользователям
Фармацевтические компании и биотехнологические компании (вместе) составили крупнейшую долю в 57,3% в 2025 году. Спонсоры часто сохраняют основное управление валидацией, чтобы поддерживать прямой контроль над критериями приемлемости, отклонениями и пакетами доказательств для регуляторов. Внутренние команды также управляют решениями о передаче методов, вопросами сопоставимости и обновлениями жизненного цикла, которые вызывают повторную валидацию. Даже при более широком аутсорсинге спонсоры обычно ожидают, что внешние партнеры будут предоставлять стандартизированные результаты, которые плавно интегрируются во внутренние системы качества и процессы аудита.
Драйверы рынка валидации биопроцессов
Расширение производства биопрепаратов и увеличение мощностей
Рост производства биопрепаратов увеличивает количество объектов, линий и площадок, которые должны соответствовать ожиданиям валидации состояния. Каждое расширение вводит циклы квалификации и валидации для оборудования, коммуникаций и критических этапов процесса. Стратегии многоплощадочного снабжения дополнительно повышают спрос на стандартизированные пакеты валидации и согласованную документацию. По мере того как организации масштабируются быстрее, они полагаются на повторяемые, основанные на рисках рамки валидации, чтобы уменьшить задержки и избежать сбоев в партиях.
- Например, Samsung Biologics завершила строительство завода 5 в апреле 2025 года, добавив 180 000 литров мощности биопроизводства и доведя общую мировую производственную мощность компании до 845 000 литров на своем объекте в Сонгдо и недавно приобретенном объекте на 60 000 литров в Роквилле, штат Мэриленд — что делает ее крупнейшей в мире CDMO по установленной мощности.
Повышение ожиданий по соблюдению требований для контроля загрязнений и обеспечения стерильности
Требования к стерильности и низкой бионагрузке увеличивают интенсивность валидации в процессах контроля, проверки целостности и экологических стратегиях. Команды по качеству все чаще ожидают доказательств того, что риски загрязнения контролируются на всем пути процесса, а не только на конечных этапах. Это расширяет потребности в тестировании в области микробиологии, тестирования целостности и проверок совместимости, которые поддерживают программы контроля загрязнений. Сильная документация и прослеживаемость являются ключевыми для соответствия ожиданиям аудита.
Внедрение одноразовых систем стимулирует валидацию материалов и совместимости
Переход к одноразовым сборкам увеличивает необходимость валидации контактных материалов, рисков вымывания и совместимости процессов в различных условиях эксплуатации. Валидация должна учитывать вариации поставщиков, изменения конфигурации сборок и обновления жизненного цикла. Покупатели ищут методы тестирования и отчеты, которые могут быть повторно использованы для различных продуктов и линий, где это возможно, чтобы уменьшить повторные усилия. Эта динамика поддерживает устойчивый спрос на услуги по тестированию экстрагируемых/вымываемых веществ и совместимости.
- Например, FUJIFILM Diosynth Biotechnologies успешно воспроизвела свою платформу одноразового биопроизводства из Северной Каролины, США, на своем объекте в Биллингеме, Великобритания, всего за 14 месяцев, предоставив первую в Великобритании cGMP одноразовую производственную площадку и начав операции на три месяца раньше первоначального графика проекта, что стало возможным благодаря стандартизированным пакетам квалификации и передаче знаний между площадками.
Рост аутсорсинга и необходимость в масштабируемой валидационной мощности
Спонсоры все чаще используют внешних партнеров для управления ограничениями по мощности, специализированными методами и требованиями к срокам выполнения. Аутсорсинг может уменьшить узкие места в разработке и коммерческой поддержке, особенно в период масштабирования и перехода продукта. Однако организации по качеству спонсоров по-прежнему требуют стандартизированных результатов, которые соответствуют внутреннему управлению и потребностям аудита. Это побуждает поставщиков услуг выделяться на фоне зрелости в соблюдении требований, качества документации и последовательности выполнения.
Проблемы рынка валидации биопроцессов
Программы валидации могут стать ресурсоемкими, поскольку меню тестов расширяется, а требования к документации увеличиваются на различных площадках и у партнеров. Организации часто сталкиваются с трудностями в согласовании критериев приемки, управления изменениями и пакетов доказательств между внутренними командами и аутсорсинговыми лабораториями, что может привести к переделкам и задержкам. Передача методов и изменения поставщиков вводят дополнительные циклы проверки, которые сложно стандартизировать в условиях разнородных производственных площадок. Управление сроками без ущерба для качества остается постоянным операционным напряжением.
Сложность также возрастает по мере диверсификации трубопроводов и изменения процессов в течение жизненного цикла, увеличивая частоту обновлений, которые могут вызвать частичную повторную валидацию. Ожидания в отношении целостности данных и прослеживаемости требуют более сильных систем, контролируемых записей и готовности к аудиту, что увеличивает накладные расходы как для спонсоров, так и для поставщиков услуг. Вариативность региональных нормативных ожиданий и акцентов инспекций может дополнительно усложнить глобальную стандартизацию. Эти давления увеличивают необходимость в управлении, шаблонах и повторяемых сценариях валидации.
- Например, компания Bristol Myers Squibb столкнулась с прямыми операционными последствиями фрагментации системы, когда ей нужно было объединить наследственную систему управления клиническими испытаниями Celgene и наследственную систему BMS, две отдельные платформы с различными архитектурами документации, в единую глобально унифицированную систему управления испытаниями; полная реализация по всем глобальным операциям компании была завершена менее чем за 20 месяцев.
Тенденции и возможности рынка валидации биопроцессов
Организации движутся к интегрированным пакетам валидации, которые связывают аналитические, микробиологические и выходные данные тестирования на целостность в структуры доказательств, готовые к аудиту. Это благоприятствует поставщикам с широкими возможностями и сильными системами качества, которые могут предоставлять стандартизированную отчетность по методам и площадкам. Также растет спрос на более быстрое выполнение и более четкие структуры документации, которые поддерживают более быстрые циклы обзора и принятия решений о выпуске. Цифровое обеспечение для отслеживания, анализа тенденций и контроля документации становится практическим отличием при выборе поставщика.
- Например, Eurofins BioPharma Product Testing управляет сетью из 46 гармонизированных лабораторий GMP более чем в 20 странах, все из которых регулируются единым Глобальным руководством по качеству и единой платформой eLIMS-BPT, электронными лабораторными журналами (ELN) и централизованным клиентским порталом LabAccess℠, охватывающим 28 местоположений по всему миру — конфигурация, которая позволяет стандартизированную документацию и отчетность, готовую к аудиту, в масштабах.
Расширение одноразовых технологий и усиленные проектные решения создают возможности для повторяемых рамок квалификации материалов, которые могут быть использованы для множества продуктов и платформ. По мере расширения аутсорсинга, CDMO и специализированные поставщики тестирования могут расти, предлагая комплексную поддержку валидации, которая снижает нагрузку на спонсоров и сокращает сроки. Также увеличивается спрос на гармонизированные подходы к валидации, которые облегчают межплощадочные передачи и обновления жизненного цикла. Эти тенденции поддерживают рост компаний, которые могут сочетать мощность с последовательным, высоко соответствующим выполнением.
Региональные особенности
Северная Америка
Северная Америка представляла 46,9% дохода в 2025 году, поддерживаемая развитым производством биопрепаратов, плотными экосистемами CDMO и высокой интенсивностью соблюдения норм. Региональный спрос обусловлен частыми масштабированиями и деятельностью по управлению жизненным циклом, которые требуют повторной валидации и обновления методов. Покупатели, как правило, отдают приоритет документации, готовой к аудиту, предсказуемым срокам выполнения и последовательному исполнению на нескольких объектах. Регион также поддерживает высокий спрос на тестирование целостности и валидационные рабочие процессы, согласованные с контролем загрязнений.
Европа
Европа составила 22,4% дохода в 2025 году, поддерживаемая широкой сетью регулируемого производства и трансграничных производственных сетей. Спрос на валидацию усиливается необходимостью стандартизированных пакетов доказательств, которые можно использовать в многострановых цепочках поставок. Покупатели часто подчеркивают важность гармонизированных процедур, сильных систем качества и надежной документации по управлению изменениями. Зрелые центры биопрепаратов и CDMO поддерживают стабильный спрос на различные виды тестирования и компоненты процессов.
Азиатско-Тихоокеанский регион
Азиатско-Тихоокеанский регион внес 21,3% дохода в 2025 году, отражая расширяющиеся мощности и растущее участие в глобальных сетях аутсорсинга и производства. Рост поддерживается строительством новых объектов, расширением платформ и увеличением внедрения стандартизированных систем качества. Спонсоры и CDMO в регионе все чаще ищут масштабируемые возможности валидации с четкими форматами документации, которые соответствуют глобальным аудитам. Спрос особенно высок там, где внедрение одноразовых технологий и быстрое масштабирование увеличивают потребности в валидации материалов и целостности.
Латинская Америка
Латинская Америка занимала 5,6% дохода в 2025 году, с концентрацией спроса вокруг локализованного производства, качественных мероприятий, связанных с импортом, и региональных производственных центров. Потребности в валидации часто формируются проектными добавлениями мощностей и модернизацией систем качества. Покупатели обычно сосредотачиваются на обеспечении соответствующей документации и надежном выполнении в условиях ограниченных ресурсов. По мере расширения возможностей ожидается усиление спроса на аутсорсинговую валидацию и стандартизированные тестовые пакеты.
Ближний Восток и Африка
Ближний Восток и Африка представляли 3,8% дохода в 2025 году, что отражает меньшую установленную базу, но растущий интерес к локализованному производству и созданию стерильных мощностей. Спрос на валидацию обычно связан с новыми проектами, модернизацией объектов и инициативами по укреплению регулируемой производственной инфраструктуры. Покупатели отдают приоритет основным системам качества, повторяемым валидационным схемам и поддержке партнеров в готовности документации. Ожидается, что рост будет соответствовать темпам инвестиций в производство и развитию возможностей.
Конкурентная среда
Конкуренция формируется широтой возможностей, зрелостью соблюдения требований, производительностью оборота и способностью предоставлять стандартизированную, готовую к аудиту документацию, интегрирующуюся в системы качества спонсоров. Поставщики выделяются, предлагая комплексные рабочие процессы валидации в аналитическом, микробиологическом и тестировании на целостность, а также консультативную поддержку для управления изменениями и обновления жизненного цикла. Масштаб, географические сети лабораторий и последовательное выполнение на всех площадках являются ключевыми для крупных биофармацевтических программ и стратегий многоплощадочного производства. Поставщики услуг также конкурируют в специализации на областях с высоким уровнем контроля, таких как контроль загрязнений, совместимость материалов и тестирование поддержки выпуска.
Thermo Fisher Scientific Inc. занимает позиции в области технологий и услуг, поддерживающих валидацию биопроцессов, с акцентом на интегрированные рабочие процессы, охватывающие биопроизводство, аналитику и поддержку качества. Подход компании обычно подчеркивает широту портфеля и способность поддерживать стандартизированные практики в средах разработки и производства. Это хорошо соответствует спросу покупателей на повторяемые рамки валидации, которые могут применяться на различных площадках и для различных продуктов. Масштаб и возможности интеграции могут поддерживать более быстрое развертывание решений по валидации и последовательные структуры документации.
Отчет об исследовании и росте отрасли включает подробные анализы конкурентной среды рынка и информацию о ключевых компаниях, включая:
Качественный и количественный анализ компаний был проведен, чтобы помочь клиентам понять более широкую бизнес-среду, а также сильные и слабые стороны ключевых игроков отрасли. Данные качественно анализируются для классификации компаний как чисто игровых, ориентированных на категорию, ориентированных на отрасль и диверсифицированных; они количественно анализируются для классификации компаний как доминирующих, ведущих, сильных, неуверенных и слабых.
Shape Your Report to Specific Countries or Regions & Enjoy 30% Off!
Последние события
- В апреле 2025 года Sartorius Stedim Biotech заключила стратегическое партнерство с Tulip Interfaces для ускорения цифровой трансформации в производстве биофармацевтической продукции. Sartorius заявила, что сотрудничество направлено на снижение ошибок ручных процессов, улучшение видимости биопроизводства от начала до конца и поддержку соблюдения нормативных требований в средах одноразового биопроцессинга.
- В марте 2025 года Cytiva расширила свое портфолио Xcellerex X-platform, добавив новые биореакторы объемом 500 л и 2000 л. Cytiva заявила, что более широкая платформа помогает ученым более плавно масштабироваться с 50 л до 2000 л с улучшенной надежностью, гибкостью и эффективностью, что поддерживает согласованность процессов для регулируемого биопроизводства.
- В феврале 2025 года Thermo Fisher Scientific объявила о заключении окончательного соглашения о приобретении бизнеса Solventum по очистке и фильтрации за приблизительно 4,1 миллиарда долларов наличными. Компания заявила, что приобретение высоко дополняет ее бизнес по биопроизводству и усилит ее возможности в области как верхних, так и нижних потоков биологических процессов, которые тесно связаны с потребностями валидации биопроцессов.
- В январе 2025 года Repligen запустила систему CTech SoloVPE PLUS, новую платформу измерения концентрации UV-Vis для приложений биопроцессинга. Repligen заявила, что продукт предназначен для обеспечения более высокой точности, скорости и простоты использования, помогая клиентам быстрее принимать решения по процессам и улучшать аналитический контроль во время производства.
Объем отчета
| Атрибут отчета |
Детали |
| Размер рынка в 2025 году |
426,54 миллиона долларов США |
| Прогноз доходов в 2032 году |
1093,81 миллиона долларов США |
| Темп роста (CAGR) |
14,4% (2025–2032) |
| Базовый год |
2025 |
| Период прогноза |
2026-2032 |
| Количественные единицы |
Миллионы долларов США |
| Охваченные сегменты |
По типу теста; По компоненту процесса; По этапу биопроцесса; По конечному пользователю |
| Региональный охват |
Северная Америка, Европа, Азиатско-Тихоокеанский регион, Латинская Америка, Ближний Восток и Африка |
| Ключевые компании, представленные в отчете |
Thermo Fisher Scientific Inc.; Merck KGaA; Sartorius AG; SGS SA; Eurofins Scientific; Pall Corporation; Charles River Laboratories; WuXi AppTec; Nelson Laboratories; TÜV SÜD |
| Количество страниц |
332 |
Сегментация
По типу теста
- Услуги по тестированию экстрагируемых/выщелачиваемых веществ
- Микробиологические услуги тестирования
- Физико-химические услуги тестирования
- Услуги тестирования целостности
- Услуги тестирования совместимости
- Другие виды тестов
По компоненту процесса
- Фильтрующие элементы
- Контейнеры и пакеты для среды
- Биореакторы
- Системы смешивания
- Пакеты для замораживания и оттаивания
- Другие компоненты процесса
По этапу биопроцесса
- Верхний уровень биопроцессинга
- Нижний уровень биопроцессинга
- Операции по наполнению и завершению
По конечному пользователю
- Фармацевтические компании
- Биотехнологические компании
- CDMO
- Другие конечные пользователи
По региону
- Северная Америка
- Европа
- Германия
- Франция
- Великобритания
- Италия
- Испания
- Остальная часть Европы
- Азиатско-Тихоокеанский регион
- Китай
- Япония
- Индия
- Южная Корея
- Юго-Восточная Азия
- Остальная часть Азиатско-Тихоокеанского региона
- Латинская Америка
- Бразилия
- Аргентина
- Остальная часть Латинской Америки
- Ближний Восток и Африка
- Страны ССЗ
- Южная Африка
- Остальная часть Ближнего Востока и Африки




