Översikt över marknaden för bioprocessvalidering:
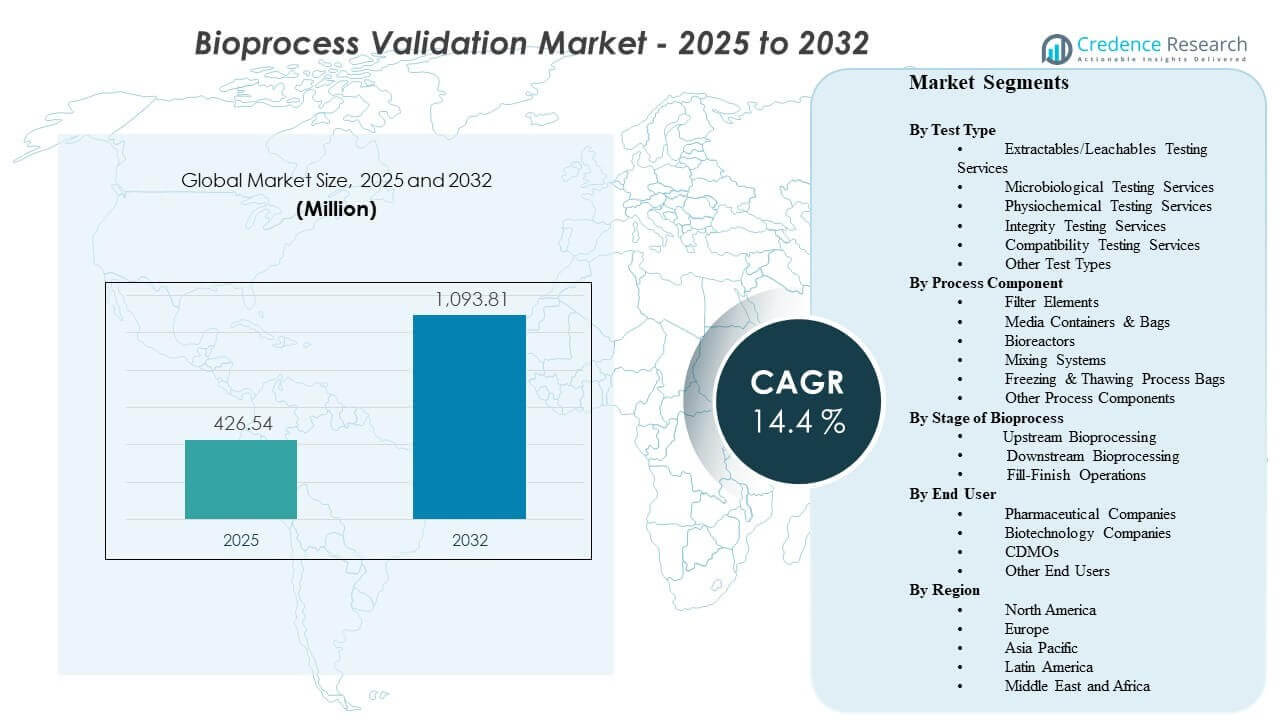
Den globala marknaden för bioprocessvalidering uppskattades till 426,54 miljoner USD år 2025 och förväntas nå 1093,81 miljoner USD år 2032, med en årlig tillväxttakt (CAGR) på 14,4% från 2025 till 2032. Tillväxten drivs främst av strängare kvalitets- och kontaminationskontrollförväntningar inom biologisk tillverkning, vilket utökar omfattningen och frekvensen av validering över kritiska processsteg och kontaktmaterial. Efterfrågan stöds ytterligare av kapacitetstillägg och tillväxt inom outsourcing som ökar volymen av kvalificering, metodvalidering och dokumentationscykler över globala tillverkningsnätverk.
| RAPPORTATTRIBUT |
DETALJER |
| Historisk period |
2020-2024 |
| Basår |
2025 |
| Prognosperiod |
2026-2032 |
| Marknadsstorlek för bioprocessvalidering 2025 |
426,54 miljoner USD |
| Marknadens CAGR för bioprocessvalidering |
14,4% |
| Marknadsstorlek för bioprocessvalidering 2032 |
1093,81 miljoner USD |
Viktiga marknadstrender och insikter
- Marknaden förväntas expandera från 426,54 miljoner USD (2025) till 1093,81 miljoner USD (2032) med en årlig tillväxttakt (CAGR) på 14,4% (2025–2032).
- Nordamerika stod för 46,9% år 2025, stödd av mogen biologisk tillverkning och hög efterlevnadsintensitet.
- Testtjänster för extraherbara/läckbara ämnen hade en andel på 37,4% år 2025, vilket återspeglar bred adoption av engångssystem och förväntningar på kontaminationsriskkontroll.
- Filterelement representerade 25,6% andel år 2025, vilket understryker den centrala rollen för steril säkerhet och integritetsverifiering i validerad produktion.
- Läkemedels- och bioteknikföretag (kombinerat) fångade 57,3% andel år 2025, eftersom sponsorer behåller direkt tillsyn över kritiska kvalitets- och frisläppningsmöjliggörande valideringsaktiviteter.
Segmentanalys
Bioprocessvalidering behandlas i allt högre grad som ett helhetsprogram som omfattar metodvalidering, kontaminationskontrollstrategi och revisionsklar dokumentation snarare än en uppsättning isolerade tester. När pipelines diversifieras och processförändringar sker oftare över uppskalning och livscykelhantering, måste valideringspaket vara upprepbara, riskbaserade och kompatibla med snabbare utvecklingstidslinjer. Detta skiftar efterfrågan mot standardiserade protokoll, stramare förändringskontrollkopplingar och datasystem som stöder spårbarhet över platser och kontraktspartners.
Engångsanvändning och intensifierade bearbetningsdesigner ökar vikten av materialkompatibilitet, profiler för extraherbara/läckbara ämnen och integritetstestning över komponenter i kontakt med vätskor. Parallellt höjer förväntningarna på steril tillverkning i sena skeden valideringsbördan kring överlämningar från uppströms till nedströms och miljöer för fyllning och avslutning. Outsourcing fortsätter att expandera av specialiserade test- och kapacitetsskäl, men sponsorer behåller vanligtvis intern styrning över acceptanskriterier, avvikelser och dokumentation för regulatoriska ändamål.
Access crucial information at unmatched prices!
Request your sample report today & start making informed decisions powered by Credence Research Inc.!
Download Sample
Insikter efter testtyp
Tjänster för testning av extraherbara/läckbara ämnen stod för den största andelen på 37,4% år 2025. Dess ledarskap återspeglar behovet av att karakterisera potentiella föroreningar från kontaktmaterial och säkerställa kompatibilitet över engångsmonteringar och processvägar. Valideringsprogram kräver i allt högre grad försvarbara profiler som kan refereras över processändringar, leverantörsuppdateringar och skalövergångar. När utvecklingstidslinjer komprimeras föredrar köpare leverantörer som kan kombinera robust analytisk täckning med tydlig rapportering anpassad till kvalitetsdokumentationsbehov.
Insikter efter processkomponent
Filterelement stod för den största andelen på 25,6% år 2025. Filter är centrala för kontaminationskontroll och steril säkerhet, vilket driver återkommande kvalificering, integritetstestning och batch-till-batch-verifiering i validerad tillverkning. Segmentet drar nytta av den höga frekvensen av filteranvändning över uppströms och nedströms operationer och behovet av att validera prestanda under definierade driftområden. Köpare prioriterar konsistens, spårbarhet och väl dokumenterade prestandakrav som stödjer revisioner och interna kvalitetsgranskningar.
Insikter efter bioprocessens skede
Uppströms bioprocessering stod för den största andelen på 51,6% år 2025. Uppströms operationer upplever vanligtvis den högsta graden av processtuning och skalningsförändringar, vilket utökar valideringsaktiviteten för metoder, provtagningsplaner och kontrollstrategier. Variabilitetsrisker i tidiga steg ökar också beroendet av validering för att visa konsekvent prestanda över körningar och platser. När organisationer antar intensifierade och slutna bearbetningsmetoder betonar uppströmsvalidering i allt högre grad robust övervakning, kontaminationskontroll och repeterbara dokumentationspaket.
Insikter efter slutanvändare
Läkemedelsföretag och bioteknikföretag (kombinerat) stod för den största andelen på 57,3% år 2025. Sponsorer behåller ofta kärnvalideringsstyrning för att upprätthålla direkt kontroll över acceptanskriterier, avvikelser och bevispaket för regulatoriska ändamål. Interna team hanterar också beslut om metodöverföring, jämförbarhetsöverväganden och livscykeluppdateringar som utlöser omvalidering. Även med bredare outsourcing förväntar sig sponsorer vanligtvis att externa partners levererar standardiserade resultat som smidigt integreras i interna kvalitetssystem och revisionsprocesser.
Drivkrafter för bioprocessvalideringsmarknaden
Expanderande biologisk tillverkning och kapacitetstillägg
Tillväxten inom produktion av biologiska läkemedel ökar antalet anläggningar, linjer och platser som måste uppfylla förväntningarna på ett validerat tillstånd. Varje expansion introducerar kvalificerings- och valideringscykler för utrustning, verktyg och kritiska processsteg. Strategier för leverans från flera platser ökar ytterligare efterfrågan på standardiserade valideringspaket och konsekvent dokumentation. När organisationer skalar upp snabbare, förlitar de sig på repeterbara, riskbaserade valideringsramverk för att minska förseningar och undvika störningar i batcher.
- Till exempel slutförde Samsung Biologics byggandet av Anläggning 5 i april 2025, vilket lade till 180 000 liter bioproduktionskapacitet och ökade företagets totala globala produktionskapacitet till 845 000 liter över dess Songdo-anläggning och den nyligen förvärvade 60 000-liters anläggningen i Rockville, Maryland — vilket gör det till världens största CDMO baserat på installerad kapacitet.
Ökande efterlevnadsförväntningar för kontaminationskontroll och steril säkerhet
Sterila och låga biobördeförhållanden ökar valideringsintensiteten över processkontroller, integritetsverifiering och miljöstrategier. Kvalitetsteam förväntar sig i allt högre grad bevis på att kontaminationsrisker kontrolleras över hela processvägen, inte bara vid slutstegen. Detta breddar testbehoven inom mikrobiologi, integritetstestning och kompatibilitetskontroller som stöder program för kontaminationskontroll. Stark dokumentation och spårbarhet är centrala för att uppfylla revisionsförväntningar.
Adoption av engångsbruk driver material- och kompatibilitetsvalidering
Övergången till engångsmonteringar ökar behovet av att validera kontaktmaterial, risk för utlakning och processkompatibilitet över driftsförhållanden. Validering måste hantera leverantörsvariation, förändringar i monteringskonfiguration och livscykeluppdateringar. Köpare söker testmetoder och rapportering som kan återanvändas över produkter och linjer där det är möjligt för att minska upprepad ansträngning. Denna dynamik stöder en fortsatt efterfrågan på extraherbara/utlaknings- och kompatibilitetstesttjänster.
- Till exempel replikerade FUJIFILM Diosynth Biotechnologies framgångsrikt sin plattform för engångsbiotillverkning från North Carolina, USA, till sin anläggning i Billingham, Storbritannien, på bara 14 månader och levererade Storbritanniens första cGMP-anläggning för engångstillverkning och påbörjade verksamheten tre månader före den ursprungliga projektplanen, möjliggjord av standardiserade kvalificeringspaket och kunskapsöverföring mellan platser.
Outsourcingtillväxt och behovet av skalbar valideringskapacitet
Sponsorer använder i allt högre grad externa partners för att hantera kapacitetsbegränsningar, specialiserade metoder och krav på ledtider. Outsourcing kan minska flaskhalsar i utveckling och kommersiellt stöd, särskilt under uppskalning och produktövergångar. Dock kräver sponsorkvalitetsorganisationer fortfarande standardiserade leveranser som passar interna styrnings- och revisionsbehov. Detta pressar tjänsteleverantörer att differentiera sig på efterlevnadsmognad, dokumentationskvalitet och konsekvent genomförande.
Utmaningar på marknaden för bioprocessvalidering
Valideringsprogram kan bli resurskrävande när testmenyer expanderar och dokumentationskraven ökar över olika platser och partners. Organisationer kämpar ofta med att anpassa acceptanskriterier, ändringskontroll och bevispaket mellan interna team och externa laboratorier, vilket kan skapa omarbetningar och förseningar. Metodöverföringar och leverantörsbyten introducerar ytterligare verifieringscykler som är svåra att standardisera över heterogena tillverkningsstrukturer. Att hantera tidslinjer utan att kompromissa med kvaliteten förblir en ihållande operativ spänning.
Komplexiteten ökar också när pipelines diversifieras och processer utvecklas genom livscykeländringar, vilket ökar frekvensen av uppdateringar som kan utlösa delvis omvalidering. Förväntningar på dataintegritet och spårbarhet kräver starkare system, kontrollerade register och beredskap för revisioner, vilket ökar overhead för både sponsorer och tjänsteleverantörer. Variabilitet i regionala regleringsförväntningar och inspektionsfokus kan ytterligare komplicera global standardisering. Dessa påtryckningar ökar behovet av styrning, mallar och upprepbara valideringsmanualer.
- Till exempel stod Bristol Myers Squibb inför den direkta operativa konsekvensen av systemfragmentering när de behövde konsolidera en äldre Celgene CTMS och en äldre BMS CTMS två separata plattformar med distinkta dokumentationsarkitekturer till ett enda globalt enhetligt prövningshanteringssystem; den fullständiga implementeringen över företagets globala verksamhet slutfördes på mindre än 20 månader.
Trender och möjligheter på marknaden för bioprocessvalidering
Organisationer rör sig mot integrerade valideringspaket som länkar analytiska, mikrobiologiska och integritetstestresultat till revisionsklara bevisstrukturer. Detta gynnar leverantörer med breda kapaciteter och starka kvalitetssystem som kan leverera standardiserad rapportering över metoder och platser. Det finns också en växande efterfrågan på snabbare genomloppstider och tydligare dokumentationsstrukturer som stödjer snabbare granskningscykler och beslut om frisläppning. Digital möjliggörande för spårning, trendanalys och dokumentationskontroll blir en praktisk differentierare vid leverantörsval.
- Till exempel driver Eurofins BioPharma Product Testing ett nätverk av 46 harmoniserade GMP-laboratorier i mer än 20 länder, alla styrda av en enda Global Quality Policy Manual och en enhetlig eLIMS-BPT-plattform, elektroniska laboratorieböcker (ELN) och en centraliserad LabAccess℠-klientportal som sträcker sig över 28 platser världen över en konfiguration som möjliggör standardiserad dokumentation över platser och revisionsklara rapporter i stor skala.
Expansion av engångsbruk och intensifierade bearbetningsdesigner skapar möjligheter för upprepbara materialkvalificeringsramverk som kan utnyttjas över flera produkter och plattformar. När outsourcing expanderar kan CDMO:er och specialiserade testleverantörer växa genom att erbjuda end-to-end valideringsstöd som minskar sponsorers arbetsbelastning och komprimerar tidslinjer. Efterfrågan ökar också på harmoniserade valideringsmetoder som underlättar överföringar mellan flera platser och livscykeluppdateringar. Dessa trender stödjer tillväxt för företag som kan kombinera kapacitet med konsekvent, hög efterlevnad i utförandet.
Regionala insikter
Nordamerika
Nordamerika representerade 46,9% av intäkterna år 2025, stödd av etablerad tillverkning av biologiska läkemedel, täta CDMO-ekosystem och hög efterlevnadsintensitet. Regional efterfrågan drivs av frekvent uppskalning och livscykelhanteringsaktiviteter som utlöser omvalidering och metoduppdateringar. Köpare tenderar att prioritera revisionsklar dokumentation, förutsägbar leveranstid och konsekvent genomförande över flera anläggningar. Regionen stöder också stark efterfrågan på integritetstestning och valideringsarbetsflöden inriktade på kontaminationskontroll.
Europa
Europa stod för 22,4% av intäkterna år 2025, stödd av ett brett fotavtryck av reglerad tillverkning och gränsöverskridande produktionsnätverk. Valideringsefterfrågan stärks av behovet av standardiserade bevispaket som kan användas i multinationella leveranskedjor. Köpare betonar ofta harmoniserade procedurer, starka kvalitetssystem och robust dokumentation för förändringskontroll. Mogna biologiska läkemedelsnav och CDMO:er stöder stadig efterfrågan över testtyper och processkomponenter.
Asien och Stillahavsområdet
Asien och Stillahavsområdet bidrog med 21,3% av intäkterna år 2025, vilket speglar ökande kapacitet och ökat deltagande i globala outsourcing- och tillverkningsnätverk. Tillväxten stöds av nya anläggningsbyggen, plattformsutvidgning och ökande antagande av standardiserade kvalitetssystem. Sponsorer och CDMO:er i regionen söker i allt högre grad skalbara valideringsmöjligheter med tydliga dokumentationsformat som överensstämmer med globala revisioner. Efterfrågan är särskilt stark där adoption av engångsartiklar och snabb uppskalning ökar behovet av material- och integritetsvalidering.
Latinamerika
Latinamerika stod för 5,6% av intäkterna år 2025, med efterfrågan koncentrerad kring lokaliserad tillverkning, importrelaterade kvalitetsaktiviteter och regionala produktionsnav. Valideringsbehov formas ofta av projektbaserade kapacitetstillägg och uppgradering av kvalitetssystem. Köpare fokuserar vanligtvis på att säkerställa efterlevande dokumentation och tillförlitligt genomförande under stramare resursbegränsningar. När kapaciteten expanderar förväntas efterfrågan på outsourcad validering och standardiserade testpaket stärkas.
Mellanöstern & Afrika
Mellanöstern & Afrika representerade 3,8% av intäkterna år 2025, vilket återspeglar en mindre installerad bas men ett ökande intresse för lokaliserad tillverkning och utbyggnad av steril kapacitet. Valideringsefterfrågan är vanligtvis kopplad till nya projekt, anläggningsuppgraderingar och initiativ för att stärka reglerad produktionsinfrastruktur. Köpare prioriterar grundläggande kvalitetssystem, repeterbara valideringsmanualer och partnersupport för dokumentationsberedskap. Tillväxten förväntas följa takten i tillverkningsinvesteringar och kapacitetsutveckling.
Konkurrenslandskap
Konkurrens formas av kapacitetsbredd, efterlevnadsmognad, prestation vid omställning och förmågan att leverera standardiserad, revisionsklar dokumentation som integreras i sponsorns kvalitetssystem. Leverantörer särskiljer sig genom att erbjuda paketerade valideringsarbetsflöden inom analytisk, mikrobiologisk och integritetstestning, tillsammans med konsultstöd för förändringskontroll och livscykeluppdateringar. Skala, geografiska labbnätverk och konsekvent genomförande över platser är avgörande för stora biopharmaprogram och tillverkningsstrategier på flera platser. Tjänsteleverantörer konkurrerar också genom specialisering inom områden med hög granskning, såsom kontaminationskontroll, materialkompatibilitet och testning för frisläppningsstöd.
Thermo Fisher Scientific Inc. är positionerat inom möjliggörande teknologier och tjänster som stödjer validerad bioprocessing, med styrka i integrerade arbetsflöden som sträcker sig över bioproduktion, analys och kvalitetsstöd. Företagets strategi betonar vanligtvis portföljens bredd och förmågan att stödja standardiserade metoder över utvecklings- och tillverkningsmiljöer. Detta stämmer väl överens med köparens efterfrågan på repeterbara valideringsramverk som kan tillämpas över platser och produkter. Skala och integrationsmöjligheter kan stödja snabbare implementering av valideringslösningar och konsekventa dokumentationsstrukturer.
Branschforskningen och tillväxtrapporten inkluderar detaljerade analyser av marknadens konkurrenslandskap och information om nyckelföretag, inklusive:
Kvalitativ och kvantitativ analys av företag har genomförts för att hjälpa kunder att förstå den bredare affärsmiljön samt styrkor och svagheter hos nyckelaktörer i branschen. Data analyseras kvalitativt för att kategorisera företag som renodlade, kategorifokuserade, branschfokuserade och diversifierade; det analyseras kvantitativt för att kategorisera företag som dominerande, ledande, starka, osäkra och svaga.
Shape Your Report to Specific Countries or Regions & Enjoy 30% Off!
Senaste Utvecklingen
- I april 2025 ingick Sartorius Stedim Biotech ett strategiskt partnerskap med Tulip Interfaces för att påskynda den digitala omvandlingen inom biopharmaceutisk tillverkning. Sartorius sa att samarbetet är avsett att minska manuella processfel, förbättra end-to-end synlighet inom biotillverkning och stödja regelefterlevnad i miljöer för engångsbioprocesser.
- I mars 2025 utökade Cytiva sin Xcellerex X-plattformsportfölj genom att lägga till nya 500L och 2,000L bioreaktorer. Cytiva sa att den bredare plattformen hjälper forskare att skala smidigare från 50L till 2,000L med förbättrad tillförlitlighet, flexibilitet och effektivitet, vilket stöder processkonsistens för reglerad biotillverkning.
- I februari 2025 tillkännagav Thermo Fisher Scientific ett definitivt avtal om att förvärva Solventums renings- och filtreringsverksamhet för cirka 4,1 miljarder dollar i kontanter. Företaget sa att förvärvet är mycket komplementärt till dess bioproduktionsverksamhet och kommer att stärka dess kapacitet över både uppströms och nedströms biologiska arbetsflöden, som är nära kopplade till behov av bioprocessvalidering.
- I januari 2025 lanserade Repligen CTech SoloVPE PLUS System, en ny at-line UV-Vis koncentrationsmätningsplattform för bioprocessapplikationer. Repligen uppgav att produkten är utformad för att leverera högre noggrannhet, snabbhet och användarvänlighet, vilket hjälper kunder att fatta snabbare processbeslut och förbättra analytisk kontroll under tillverkning.
Rapportomfattning
| Rapportattribut |
Detaljer |
| Marknadsvärde 2025 |
USD 426,54 miljoner |
| Intäktsprognos 2032 |
USD 1093,81 miljoner |
| Tillväxttakt (CAGR) |
14,4% (2025–2032) |
| Basår |
2025 |
| Prognosperiod |
2026-2032 |
| Kvantitativa enheter |
USD miljoner |
| Segment som omfattas |
Efter Testtyp; Efter Processkomponent; Efter Bioprocessens Steg; Efter Slutanvändare |
| Regional omfattning |
Nordamerika, Europa, Asien och Stillahavsområdet, Latinamerika, Mellanöstern & Afrika |
| Profil av nyckelföretag |
Thermo Fisher Scientific Inc.; Merck KGaA; Sartorius AG; SGS SA; Eurofins Scientific; Pall Corporation; Charles River Laboratories; WuXi AppTec; Nelson Laboratories; TÜV SÜD |
| Antal sidor |
332 |
Segmentering
Efter Testtyp
- Testtjänster för extraherbara/läckbara ämnen
- Mikrobiologiska testtjänster
- Fysikalisk-kemiska testtjänster
- Integritetstesttjänster
- Kompatibilitetstesttjänster
- Andra testtyper
Efter processkomponent
- Filterelement
- Mediebehållare & påsar
- Bioreaktorer
- Blandningssystem
- Frysnings- & upptiningsprocesspåsar
- Andra processkomponenter
Efter bioprocessens steg
- Upstream bioprocessing
- Downstream bioprocessing
- Fyll-slutför operationer
Efter slutanvändare
- Läkemedelsföretag
- Bioteknikföretag
- CDMO:er
- Andra slutanvändare
Efter region
- Nordamerika
- Europa
- Tyskland
- Frankrike
- Storbritannien
- Italien
- Spanien
- Resten av Europa
- Asien och Stillahavsområdet
- Kina
- Japan
- Indien
- Sydkorea
- Sydostasien
- Resten av Asien och Stillahavsområdet
- Latinamerika
- Brasilien
- Argentina
- Resten av Latinamerika
- Mellanöstern & Afrika
- GCC-länder
- Sydafrika
- Resten av Mellanöstern och Afrika




